Что изучает химия каковы ее важнейшие задачи и значение назовите какие продукты химической
Химия как наука изучает вещества, их свойства, как и почему вещества соединяются или разделяются, образуя другие вещества, и как они взаимодействуют с энергией.
Многие люди думают, что химики – это научные люди в белых халатах, которые смешивают странные жидкости в лаборатории, но на самом деле мы все химики. Понимание основных понятий химии как науки важно практически для каждой профессии.
Химия-это часть всего в нашей жизни.
Каждый существующий материал состоит из материи — даже наши собственные организмы. Химия участвует во всем, что делает человек, от выращивания и приготовления пищи до уборки дома и запуска космического аппарата.
Химия – это одна из основополагающих наук, которая помогает нам описывать и объяснять наш мир.
Разделы науки химии
Существует пять основных разделов химии, каждый из которых имеет много областей изучения.
- Аналитическая
- Органическая
- Неорганическая
- Биохимия
- Физическая
Аналитическая
Аналитическая химия как наука развивает теорию химического анализа веществ и материалов, разрабатывает методы идентификации и обнаружения. Проводит анализ и определяет химические элементы веществ с целью получения информации о природе вещества.
Анализ аналитических методов необходим для поиска возможностей практического применения теории.
Аналитическая химия использует качественные и количественные наблюдения для выявления и измерения физических и химических свойств веществ.  В определенном смысле вся химия аналитична.
В определенном смысле вся химия аналитична.
Неорганическая
Неорганическая химия изучает такие вещества и газы в состав которых не входит углерод.
Раздел науки изучает металлы и неметаллы, оксиды и соли, гидроксиды и кислоты, нитриды и гидриды, а также технологии применения в производстве, защите и использовании сельскохозяйственных культур и скота.
Химическая технология
Инженеры-химики исследуют и разрабатывают новые материалы или процессы, связанные с химическими реакциями. Химическая инженерия сочетает в себе основы науки с инженерными и экономическими концепциями для решения технологических проблем.
Химическое машиностроение представляет базовую отрасль экономики как химическая и нефтехимическая промышленность и делится на две основные группы: промышленное применение и разработка новых продуктов.
Отрасли промышленности требуют от инженеров-химиков разработки новых способов сделать производство своей продукции более легким и экономически эффективным. Ученые-химики участвуют в проектировании и эксплуатации перерабатывающих предприятий, разрабатывают процедуры безопасности при обращении с опасными материалами и контролируют производство почти каждого продукта, который мы используем. Ученые-химики работают над разработкой новых продуктов и процессов в любой области-от фармацевтики до топлива и компьютерных компонентов.
Геохимия
Геохимики объединяют химию и геологию для изучения состава и взаимодействия между веществами, находящимися в земле.
Геохимики могут тратить больше времени на полевые исследования, чем другие ученые. Многие работают в службах по охране окружающей среды, определяя, как горнодобывающие операции и отходы могут повлиять на качество воды и окружающую среду. Они могут направляться в отдаленные заброшенные шахты для сбора проб и проведения грубых полевых оценок, а затем следовать за потоком через его водосбор, чтобы оценить, как загрязняющие вещества перемещаются через систему. Ученые раздела нефтяной геологии занимаются вопросами химического изучения состава нефти и связанных с ней природных образований. Они работают в нефтегазовых компаниях, чтобы помочь найти новые запасы энергии. Ученые этой науки также могут работать на трубопроводах и нефтяных вышках, чтобы предотвратить химические реакции, которые могут вызвать взрывы или разливы.
Судебная химия
Судебно-медицинские химики собирают и анализируют вещественные доказательства, оставленные на месте происшествия, чтобы помочь установить личности причастных лиц, а также ответить на другие жизненно важные вопросы, касающиеся того, как и почему было совершено событие. Судебно-медицинские химики используют широкий спектр методов анализа, таких как хроматография, спектрометрия и спектроскопия.
Например, химики разработали систему, которая выходит за рамки идентификации отпечатков пальцев. Этот метод может захватывать молекулы, содержащиеся в отпечатке пальца, включая липиды, белки, генетический материал или даже следовые количества взрывчатых веществ, которые могут быть дополнительно проанализированы. Новый инструмент по существу снимает тайну с определения химического состава отпечатков пальцев на местах событий.
Агрохимия
Агрохимия как неорганическая наука связана с веществами и химическими реакциями, которые участвуют в производстве, защите и использовании сельскохозяйственных культур и скота. Это междисциплинарная область которая опирается на связи со многими другими науками. Сельскохозяйственные химики необходимы в сельском хозяйстве, агентствах по охране окружающей среды, управлениях по контролю за продуктами питания и лекарствами или в частном секторе.
Агрохимия как наука разрабатывает удобрения, инсектициды и гербициды, необходимые для крупномасштабного растениеводства. Ученые занимающиеся этой наукой следят за тем, как используются продукты и как они влияют на окружающую среду. Они также разрабатывают пищевые добавки для повышения продуктивности мясных и молочных стад.
Сельскохозяйственная биотехнология является быстро растущим направлением в науке. Генетически манипулирующие культуры, чтобы быть устойчивыми к гербицидам, используемым для борьбы с сорняками на полях, требуют детального понимания как самих растений, так и химических веществ на молекулярном уровне. Биохимия как наука должна понимать генетику и потребности бизнеса в разработке культур, которые легче транспортировать или которые имеют более длительный срок хранения.
Органическая
Органическая химия специально изучает соединения, содержащие элемент углерод.
Углерод обладает многими уникальными свойствами, которые позволяют ему образовывать сложные химические связи и очень крупные молекулы.
Органическая химия известна как “химия жизни”, потому что все молекулы живой ткани, имеют углерод в своем составе.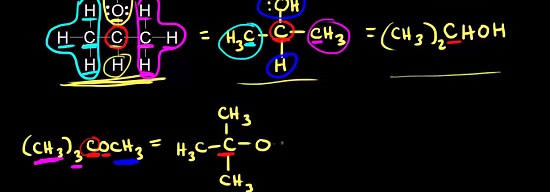
Органических соединений теоретически может быть бесчисленное множество, а их строение более сложное, чем минеральные (неорганические) вещества.
Ученые, занимающиеся вопросами неорганической химии, разделились на множество самостоятельных наук.
Биохимия
Биохимия-это изучение химических процессов, происходящих внутри живых организмов.
В рамках этих широких категорий находятся бесчисленные области исследований, многие из которых оказывают важное влияние на нашу повседневную жизнь. Химики улучшают многие продукты, начиная с пищи, которую мы едим, и одежды, которую мы носим, и заканчивая материалами, из которых мы строим наши дома.  Биохимия помогает защитить нашу окружающую среду и ищет новые источники энергии.
Биохимия помогает защитить нашу окружающую среду и ищет новые источники энергии.
Пищевая
Пищевая наука имеет дело с тремя биологическими компонентами пищи — углеводами, липидами и белками.
- Углеводы – это сахар и крахмал, химическое топливо, необходимое для функционирования наших клеток.
- Липиды – это жиры и масла, которые являются существенными частями клеточных мембран и служат для смазывания и смягчения внутренних органов организма. Поскольку жиры содержат в 2 раза больше энергии на грамм, чем углеводы или белки, многие люди стараются ограничить их потребление, чтобы избежать избыточного веса.
- Белки – это сложные молекулы, состоящие из от 100 до 500 или более аминокислот, которые соединяются вместе и складываются в трехмерные формы, необходимые для структуры и функционирования каждой клетки.
Наш организм может синтезировать некоторые аминокислоты, однако восемь из них, незаменимые аминокислоты, должны быть приняты в качестве части нашей пищи. Ученые-пищевики также занимаются неорганическими компонентами продуктов питания, такими как содержание в них воды, минералов, витаминов и ферментов.
Ученые-химики улучшают качество, безопасность, хранение и вкус наших продуктов. Они создают качественные продовольственные изделия и методы анализа пищевых производств. Они также работают в учреждениях по улучшению переработки и контролю за продуктами питания и лекарствами, чтобы проверять пищевые продукты и защищают нас от загрязнения или вредных практик.
Ученые-химики тестируют продукты, чтобы предоставить информацию, используемую для этикеток пищевых продуктов, или определить, как упаковка и хранение влияют на безопасность и качество продуктов питания. Ученые создают пищевые ароматизаторы и работают с химическими веществами, чтобы изменить вкус пищи.
Химики могут также работать над другими способами улучшения сенсорной привлекательности, такими как улучшение цвета, запаха или текстуры.
Химия окружающей среды
Химики-экологи изучают, как химические вещества взаимодействуют с окружающей средой.
Экологическая химия-это междисциплинарная наука, которая включает в себя как аналитическую химию, так и понимание науки об окружающей среде. Химики-экологи должны изучать химические вещества и химические реакции, присутствующие в естественных процессах в почве, воде и воздухе. Отбор проб и анализ показать, не загрязняла ли человеческая деятельность окружающую среду или не вызывала ли она вредных реакций.
Качество воды является важной областью химии окружающей среды. “Чистой” воды в природе не существует, в ней всегда растворены какие-либо минералы или другие вещества. Химики проверяют качество воды в реках, озерах и океанах на такие характеристики, как растворенный кислород, соленость, мутность, взвешенные осадки и водородный показатель РН. Вода, предназначенная для потребления человеком, должна быть свободна от вредных примесей и может быть обработана такими добавками, как фтор и хлор, чтобы повысить ее безопасность.
Физическая химия
Физическая химия как наука изучает общие законы и закономерности, определяющие строение и физикохимические свойства веществ, механизм и динамику их химических превращений при различных природных условиях.
Это активно развивающаяся наука которая решает множество прикладных задач по получению количественных и качественных данных о о свойствах соединений. В этой части развиваются новые направления связанные с пониманием свойств наноразмерных объектов и выяснением влияния биологически активных сред.
Роль физической химии в понимании фундаментальных. основ химии как науки на современном этапе является определяющей.
Источник
ЛЕКЦИЯ
“Предмет и задачи химии. Основные понятия химии”
План:
1. Предмет изучения химии.
2. Задачи и значение химии.
3. Основные понятия химии.
1. Предмет изучения химии.
Химия – относится к естественным наукам и изучает состав, строение, свойства и превращения веществ, а также явления, сопровождающие эти превращения.
Химия изучает окружающий мир, т. е. материю, которая проявляется в двух формах: вещества и поля.
Вещество – форма материи состоящая из частиц, которые имеют массу покоя (собственную массу), занимающая часть пространства и существующая за счет сил притяжения и отталкивания. К веществам относятся макротела, микротела и элементарные частицы (ē,p, n). Число природных синтезированных веществ составляет более 10 млн.
Поле – это такая форма существования материи, которая прежде всего характеризуется энергией. Посредством поля осуществляется взаимодействие между частицами вещества. Пример: электромагнитные и гравитационные поля.
Неотъемлемым свойством материи является движение.
Движение материи – это любое изменение. Материя находится в непрерывном движении. Формы движения очень разнообразны – тепловая, химическая, механическая. Формы движения материи изучаются разными естественными науками: химией, физикой, биологией и др.
Предмет изучения химии: химия изучает химическую форму движения материи, под которой понимают качественное изменение веществ, т. е. разрушение одних химических связей и образование других. В результате химических процессов возникают новые вещества с новыми химическими и физическими свойствами.
Свойствами материи являются:
– масса – это мера её инертности; – энергия – это мера её движения.
Объектом изучения в химии являются химические элементы и их соединения.
2. Задачи и значение химии.
Задачи химии:
1. Получение веществ с заранее заданными свойствами (для развития новой техники необходимы материалы с особыми свойствами, которых нет в природе: сверхчистые, сверхтвердые, жаростойкие, сверхпроводящие).
2. Повышение эффективности производства и качества продукции.
3. Создание безвредных, безотходных технологий.
4. Рациональное использование энергии химических превращений (в настоящее время электрическую и механическую энергию получают в основном преобразованием химической энергии природного топлива).
Значение химии для с/х:
1. Удобрения (макро – и микро-).
2. Химические средства защиты растений.
3. Лекарственные препараты.
3. Основные понятия химии.
Атомно–молекулярное учение
Атомно-молекулярное учение развил и впервые применил в химии великий русский ученый (1741 г.). Атомно-молекулярное учение позволяет объяснить основные понятия и законы химии.
Основные положения:
1. Все вещества состоят из молекул.
2. Молекулы состоят из атомов.
3. Частицы – молекулы и атомы – находятся в непрерывном движении.
4. Молекулы простых веществ состоят из одинаковых атомов, молекулы сложных веществ из различных атомов.
Атом – это электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов.
Элемент – вид атомов с одинаковым зарядом ядра. Каждый элемент имеет своё название и символ. В настоящее время известно 109 химических элементов периодической системы (ПС). Из них в природе существует 88 и более 20-ти получены искусственным путем в процессах ядерных превращений элементов.
Символы элементов состоят из одной или двух букв латинского названия элементов и являются интернациональными. Названия элементов в каждом языке различны.
Пример: элемент с русским названием водород имеет символ “Н” (аш), который является первой буквой латинского названия этого элемента”Hydrogenium”.
Все элементы делятся на металлы и неметаллы. Если провести диагональ от бора (В) к астату (At), то к металлам будут относиться все элементы слева от диагонали + элементы побочных подгрупп, справа неметаллы.
Молекула – наименьшая частица вещества, которая сохраняет его химические свойства.
Состав любой молекулы можно выразить молекулярной химической формулой – показывает качественный и количественный состав молекулы.
H2SO4 качественный состав: молекула состоит из атомов H, S, O
количественный: 2 атома Н, 1 атом S, 4 атома О.
– графическая формула – отображает структуру молекулы:
Н-О-Н графическая формула молекулы воды
черта – обозначает общую электронную пару, т. е. одну химическую связь, число связей определяется валентностью данного элемента.
Все вещества делятся на простые и сложные:
Простые вещества – это вещества, состоящие из атомов одного элемента.
Простые вещества делятся на два класса:
– металлы – образованы элементами Ме, металлы одноатомные
– неметаллы – образованы элементами неметаллами:
H2, O2, Cl2 I2 ,S, P He, Ar
газообразные тв. в-ва свободные несвязанные атомы
двухатомные благородные газы
Число существующих простых веществ (≈ 400) больше числа химических элементов, что объясняется явлением аллотропии.
Аллотропия – это явление образования нескольких простых веществ одним элементом.
Простые вещества, образованные одним и тем же элементом, называются аллотропными модификациями. Они могут отличатся
O2 – кислород
составом: O
O3 – озон
алмаз
или структурой: С графит
Сложные вещества – это вещества, состоящие из атомов разных элементов. Сложные неорганические вещества классифицируются на основные 4 класса:
– оксиды: CaO, SO3
– основания: NaOH, Cu(OH)2
– кислоты: H2SO4, HCl
– соли: Na2CO3, CaCl2
Ионы – частицы имеющие заряд. Ионы делятся на простые и сложные.
Простые ионы – состоят из атомов одного элемента (Na+, Cl-).
Сложные ионы – состоят из атомов нескольких элементов (OH-, SO42-).
Положительно заряженные ионы называются катионами.
Отрицательно заряженные – анионами.
Заряд простого иона – равен степени окисления элемента в соединении.
Необходимо помнить, что постоянные степени окисления в сложных соединениях проявляют следующие элементы:
– кислород О-2 (исключения Н2О2-1, О+2F2)
– водород Н+1 (искл. гидриды NaH-1)
– щелочные Ме+1: Na+, К+
– щелочно-земельные Ме+2: Ca2+, Mg2+, Ba2+
– все металлы имеют только положительную степень окисления (max-е значение = № группы)
– F-, Al+3
Переменные степени окисления: Fe2+, Fe3+, Cu+, Cu2+
Заряд сложного иона: NH4+ – катион аммония
-3 +1*4 = +1
OH – – гидроксильная группа
-2 +1 = -1
Кислотный остаток – это все то, что остается от молекулы кислоты после отнятия катиона Н+.
Заряд кислотного остатка – всегда отрицательный (анион) и равен числу катионов водорода, которые необходимо отнять от молекулы кислоты, чтобы получить данный остаток:
H3PO4 (H2PO4)- дигидрофосфат
обр-т кислые соли
H3PO4 (HPO4)2- гидрофосфат
H3PO4 (PO4)3- фосфат средние соли
Название: гидро (Н), числительное ди – (Н2….)
Остаток от основания – все то, что остается от молекулы основания после отнятия гироксильной группы.
Заряд остатка от основания – всегда положительный (катион) и равен числу гидроксильных групп, которые необходимо отнять, чтобы получить данный остаток:
Al (OH)3 [Al (OH)2 ]+ ион дигидроксоалюминия
Al (OH)3 [Al OH]2+ ион гидроксоалюминия
Al (OH)3 Al3+ ион алюминия
OH – – гидроксо
Составление молекулярных формул веществ.
В основе составления молекулярной формулы лежит принцип электронейтральности – алгебраическая сумма степеней окисления атомов в соединении всегда равна нулю, а в сложном ионе заряду иона. Так как сложное вещество состоит из ионов, то общий заряд катиона (произведение числа иона на его заряд с учетом знака) + общий заряд аниона (Х число иона на его заряд) =0.
Ca3+2 (PO4)2-3
общ. зар. катиона: 3 (+2) = +6
общ. зар. аниона: 2 (-3) = -6
сумма: +6 – 6 =0
Последовательность составления молекулярной формулы:
1. По названию определить класс соединения; записать ионы: на первом месте катион, затем анион.
2. Определить заряд катиона и заряд аниона.
3. Если заряды численно равны, то индексы =1, они не ставятся.
Если заряды не равны, то их уравнивают: находят общее кратное заряда катиона и аниона и делят его на заряд катиона (получают индекс для катиона) и на заряд аниона (получают индекс для аниона)
4. Осуществляется проверка: ∑ общ. зарядов катиона и аниона = 0
ПРИМЕР: Привести молекулярную формулу оксида фосфора (V)
1) оксид => PO; (V) => С. О. = +5
2) P+5 O-2
3) общ. кратное = 10
4) 10:5 = 2 индекс для (Р)
10:2 = 5 индекс для (О)
P2+5O5-2 проверка: 2 (+5) = +10 +10 -10 =0
5 (-2) = -10
Источник
