Какие физические свойства металлов используют в технике примеры
ГлавнаяРазноеКакие физические свойства металлов используют в технике примеры
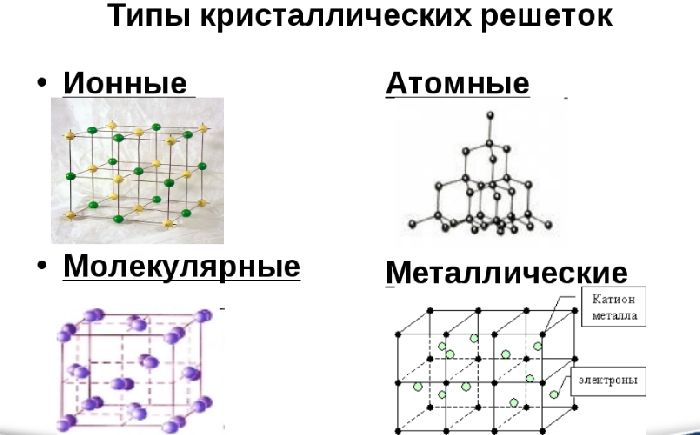
Физические свойства металлов
Особенностями строения металлов определяются их характерные физические свойства.
Пластичность. При деформации (изменении формы куска металла) ионы лишь смещаются относительно друг друга, но разрыва не происходит, так как связывающие их электроны, соответственно переместившись, продолжают осуществлять связь между сместившимися ионами. На практике пластичность проявляется в том, что под ударами молота металлы не дробятся на куски, а расплющиваются – они ковки. Самый пластичный металл – золото: его можно вытягивать в тонкие золотые нити, невидимые человеческому глазу или раскатывать в тончайшие полупрозрачные листы.
Электрическая проводимость объясняется способностью электронов легко перемещаться по всему куску металла.
Высокая теплопроводность также обусловлена движением электронов, так как именно они передают теплоту в разные участки куска металла, благодаря электронам металлы обладают характерными оптическими свойствами непрозрачности и металлического блеска. Металлы блестят потому, что отражают от своей поверхности световые лучи, а не пропускают их, как стекло, и не поглощают их как сажа.
Различные свойства проявляются в металлах в неодинаковой степени. Самой лучшей проводимостью обладает серебро, второе место по электронной проводимости занимает медь, далее следует алюминий. С помощью этих металлов можно передавать электрическую энергию на большие расстояния . Но в электротехнике в качестве материала для проводки используются алюминий и медь, так они значительно дешевле серебра.
В таком же порядке металлы располагаются и по теплопроводности: серебро, медь, алюминий.
Из более важных свойств металла стоит обратить внимание на плотность, твёрдость, прочность и температуру плавления. Плотность металла тем больше, чем больше его относительная атомная масса и чем меньше радиус атома и наоборот. Например, у лития – 534 кг/м3, а у осмия – 22500 кг/м3. Металлы с плотностью ниже 5000 кг/м3 называют лёгкими: магний, алюминий, титан. Металлы с большой плотностью: свинец, осмий.
Такие свойства металлов, как прочность, твёрдость и температура плавления зависят от прочности металлической связи. Особенно сильна эта связь у тяжёлых металлов с достраивающимся предпоследним электронным слоем атома: тантала, вольфрама и др. Эти металлы и отличаются высокой твёрдостью и низкой плавкостью.
Температура плавления металлов изменяется от 39˚ С (ртуть) до 3410˚ С (вольфрам). Ртуть является единственным жидким металлом.
Твёрдость металлов изменяется в широких пределах: щелочные металлы достаточны мягкие, а саамы твёрдые металлы не поддаются обработке напильником.
© blog.tutoronline.ru,
при полном или частичном копировании материала ссылка на первоисточник обязательна.
blog.tutoronline.ru
45. Физические свойства металлов
Все металлы имеют ряд общих, характерных для них свойств. Общими свойствами считаются: высокая электропроводность и теплопроводность, пластичность.
Разброс параметров у металлов очень велик, например, температура плавления может варьировать от 38,87 °C (Hg – ртуть) до 3380 °C (W – вольфрам), плотность – от 0,531 г/см3(Li – литий) до 22,5 г/см3(Os – осмий).
Коэффициент электропроводности металлов храктеризует их способность к проведению электричества. Коэффициент зависит от строения и свойств металла, у каждого металла он индивидуальный. Теория электропроводности состоит в том, что фактором электрического сопротивления металлов являются потери на излучение. Пользуясь теорией, можно вычислить коэффициент для любого металла.
Металлы способны испускать электроны при высокой температуре, это явление называется термоэлектронной эмиссией, возникающее также под воздействием других факторов (электро-магнитое поле, воздействие УФ и др.). Перепад температуры провоцирует в металлах появление электрического тока. Движения электронов в металлах обуславливают их теплопроводность. Отношение теплопроводности металлов и их электрической проводимости является постоянной величиной для всех металлов.
По магнитной восприимчивости металлы делятся на диамагнетики и парамагнетики.
Металлы непрозрачны, обладают металлическим блеском, сочетают в себе такие качества как: пластичность, вязкость, прочность, твердость и упругость. Все эти свойства зависят от целостности кристаллической решетки и состава.
Пластичность металлов находит большое практическое применение. Благодаря ей металлы можно подвергать различным воздействиям – ковке, вытягиванию, прокатке, штамповке. Это свойство можно объяснить специфическими свойствами металлической связи, которая связывает атомы металлов в кристаллической решетке.
Механические свойства реальных металлов характеризуются присутствием дефектов, в первую очередь дислокаций, потому что перемещение дислокаций по плоскостям кристаллической решетки с наиболее плотной упаковкой считается основным механизмом пластической деформации металлов. При взаимодействии дислокаций с другими дефектами вызывается увеличение сопротивления пластической деформации. Во время деформации количество дислокаций растет, одновременно с ними растет сопротивление деформации (деформационное упрочнение или наклеп). Подобные дефекты металла можно устранить при отжиге. В локализациях «сгущения» рост напряжений способен привести к образованию трещин, являющихся очагами разрушения металла.
46. Химические свойства металлов
Металлы обладают низким потенциалом ионизации и сродством к электрону, поэтому в химических реакциях выступают в качестве восстановителей, в растворах образуют катионы. Электроотрицательность у металлов ниже, чем у неметаллов. Могут входить в состав сложных анионов или комплексов, но при этом являются центрами положительного заряда. Лишь у амфотерных металлов (проявляющих как окислительные, так и восстановительные свойства) – Sn олово, Po полоний, Sb сурьма и др. – существуют соединения с отрицательной степенью окисления. Во всех химических соединениях у металлов химическая ковалентная полярная связь.
Сильно варьируется способность металлов к окислению. Основная часть металлов взаимодействует с кислородом воздуха при комнатной температуре, но скорость и механизм протекания реакции зависят от состава и чистоты металла (чаще образуются оксиды, у щелочных металлов – пероксиды). Некоторые металлы на воздухе образуют оксидную пленку, которая предохраняет металл от дальнейшего окисления (Al – алюминий, Ti – титан, Сr – хром).
Металлы, имеющие стандартный электродный потенциал отрицательнее -0,413 В, окисляются водой, выделяя при этом Н2. Щелочные и щелочноземельные металлы вступают во взаимодействие с водой при комнатной температуре, другие (Zn – цинк, Fe – железо и др.) – при высоких температурах. Растворимые анионные комплексы бериллия, цинка, алюминия, галлия, олова вступают в реакцию с растворами щелочей.
Основная часть металлов окисляется определенными кислотами. Металлы, стоящие в ряду напряжений до водорода, окисляются ионом водорода, входящего в состав кислот и образуют раствор соли, если не происходит образования нерастворимых продуктов реакции. С азотной кислотой в зависимости от ее концентрации металлы взаимодействуют по-разному. Концентрированная азотная кислота пассивирует некоторые металлы, например, железо, а разбавленная вступает во взаимодействие с ними, образуя катионные комплексы. Чтобы получить раствор малоактивных металлов, например, золота или платины, используют смеси, содержащие окислитель и поставщика лигандов, такие как царская водка или смесь HNO3 и HF.
Важным характерным свойством металлов является способность образовывать основные оксиды и гидроксиды. В главных подгруппах периодической системы основность оксидов и гидроксидов идет на возрастание сверху вниз, а в побочных подгруппах (исключение составляют I–III) – наоборот – снизу вверх. С ростом порядкового номера в периодах и рядах основность металла убывает. Металлы, имеющие несколько степеней окисления, имеют кислотные оксиды.
studfiles.net
Общие физические свойства металлов
Металлические элементы занимают преимущественно левую нижнюю часть Периодической системы химических элементов Д. И. Менделеева. К металлических элементов относятся те элементы, в чьих атомах на внешнем электронном уровне находится небольшое (от одного до четырех) число электронов, атомы могут легко отдавать.
Металлы имеют ряд общих физических свойств:
– Хорошую электропроводность;
– Хорошую теплопроводность;
– Металлический блеск;
– Хорошую пластичность (ковкость)
– Обычно высокую твердость;
– Чаще всего находятся в твердом агрегатном состоянии.
О принадлежности вещества к металлам нельзя судить только по одному признаку. Так, некоторые неметаллы могут проводить электрический ток (графит), имеют металлический блеск (йод), имеют пластичность (пластическая сера). Таким образом, относить ту или иную простое вещество к металлам или неметаллов можно только по совокупности признаков. Общие физические свойства металлов (электропроводность, теплопроводность, блеск и т.д.) объясняются наличием подвижных электронов, иначе говоря, особым характером металлического связи. 0днако различные металлы все-таки имеют различные физические свойства, такие как температура плавления, плотность и т.д.. Эти свойства во многом зависят от кристаллических структур металлов.
Благодаря металлической связи отдельные слои в кристаллах металлов могут смещаться относительно друг друга. Это придает металлам пластичности (ковкости) – способности изменять свою форму без разрыва химических связей. Например, наиболее ковкой металлом является золото – с 1 г золота можно вытянуть проволоку длиной 2,4 км и толщиной в несколько раз меньше толщины волоса. Вместе металл труба очень хрупкий – его даже можно растирать в порошок в ступке.
0скилькы различные металлы имеют сходные металлические связи, а в ряде случаев образуют подобные металлические кристаллы, то многие из них при переходе в расплавленное состояние могут смешиваться друг с другом, образуя сплавы. Сплавы имеют более разнообразные свойства по сравнению с металлами, поэтому в промышленности редко используют чистые металлы. В большинстве случаев для изготовления деталей различных машин и приборов применяют сплавы. Так, медь, олово и цинк – это мягкие металлы, тогда как сплав на их основе – бронза – очень твердый, поэтому бронзу люди издавна использовали для изготовления оружия, плугов и других изделий, где требуется повышенная жесткость. Сплав олова со свинцом (третник) применяют при пайке, так как он имеет сравнительно низкую температуру плавления. Наиболее распространенными из сплавов является чугун и сталь – сплав железа с углеродом и другими неметаллами.
worldofscience.ru
УРОК НА ТЕМУ: “ФИЗИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ”
ФИЗИЧЕСКИЕ СВОЙСТВА МЕТАЛОВ
Ход урока
Организационный этап – приветствие преподавателя, подготовка рабочих мест и проверка готовности к уроку.
Мотивация учебной деятельности, постановка темы и целей урока
Ребята, сегодня мы с вами продолжим изучать тему, без знаний которой не обходятся люди многих профессий: врачи, фармацевты, биологи, химики, физики, минерологи, геологи, агрономы, ветеринары, инженеры, повара, автомеханики и список этот можно продолжать до бесконечности.
Вы догадались, о чем пойдет речь? (предполагаемый ответ – о металлах).
Задумывались ли вы когда – нибудь о том, какими материалами человек пользуется чаще всего? Давайте оглянемся вокруг. Наш техникум возведен из кирпичей. В окна вставлены стекла. Мебель в классе деревянная. С потолка свисают светильники. Все это состоит из камня, дерева, стекла…
Но здание держится на каркасе из сваренных между собой стальных балок, мебель держится на металлических шурупах. Из металла сделаны цоколь люминесцентной лампы и провода, по которым течет электрический ток.
Послушайте одно незатейливое стихотворение Е. Ефимовского с тем, чтобы попытаться определить, какие свойства проявляют металлы.
“Металл – это точность”.
Металл – прочность,
Скорость, высота,
Блеск и красота.
Не сразу в дом пришел металл,
Не сразу ложкой, вилкой стал.
Не сразу стал он кружкой
И заводской игрушкой.
И каждый вложит труд в металл,
Чтобы металл трудиться стал.
Он в проводах несет нам свет,
Металл – коньки, велосипед,
Метро, трамвай, будильник,
Утюг и холодильник.
О каких свойствах металлов идет речь в стихотворении? (О физических свойствах: прочность, блеск, электропроводность).
Все ли свойства, которыми обладают металлы, были перечислены? (нет
Вопрос к группе: какую тему нам надо рассмотреть на уроке? Что для этого нужно сделать, какие задачи решить?
Давайте поставим перед собой цель: что нам нужно сделать на уроке. (выявить все физические свойства металлов, определить, от чего они зависят, отличаются ли разные металлы друг от друга или они все однотипные и какое применение металлы находят в жизни и производстве).
Актуализация знаний универсальных учебных действий (УУД).
Беседа по вопросам.
Что означает слово металл? (химический элемент и простое вещество).
Чего известно больше – металлов или неметаллов? (85 из 109 химических элементов являются металлами).
Где металлы содержатся в ПСХЭ Д.И. Менделеева? (в левом нижнем углу).
В чем особенность строения атомов металлов? (малое количество электронов на внешнем энергетическом уровне, большой атомный радиус).
Как изменяются металлические свойства в периоде, в группе (в периоде ослабевают, в группе – возрастают).
Почему так происходит? (атомы металлов содержат малое количество электронов на внешнем уровне, стремясь завершить его, они легко отдают их).
Так чем можно объяснить свойства металлов? (Выдвигается гипотеза – свойства металлов можно объяснить особенностью строения их атомов, определенным видом химической связи в металлах).
Первичное восприятие и усвоение нового теоретического учебного материала
Вопрос группе: Какой вид связи в металлах? Какой тип кристаллической решетки в них?
Просмотр видеоролика «Металлическая связь»
Вставьте пропущенные слова в текст:
Атомы большинства металлов содержат на внешнем энергетическом уровне ___________ электронов. Эти электроны легко ____________, и атомы при этом превращаются в ____________. Оторвавшиеся электроны _______________ от одного ___________ к другому. При присоединении электронов к иону временно образуются __________ , а затем электроны снова отрываются от атома, и он снова превращается в __________ . В куске металла существуют все время то _________ , то _______ . Их так и называют «атом-ионы». Связь в металлах между ___________ посредством ______________________ называется _________________
По окончании работы обучающиеся осуществляют взаимопроверку в парах.
Применение теоретических положений в условиях выполнения заданий
Вопрос группе: Что же определяет физические свойства металлов? (металлическая связь и кристаллическая металлическая решётка).
Групповая исследовательская работа.
Группа разбивается на 2 подгруппы, каждая получает свое задание, работает с инструктивными картами, учебниками, таблицами, графиками и образцами металлов и выполняет задание.
По окончании работы преподаватель в ходе беседы привлекает внимание обучающихся к принципиально новым сведениям.
Зачитывается выражение М.В. Ломоносова «Металлом называется твердое непрозрачное и светлое тело, которое на огне плавить и холодное ковать можно». О каких свойствах металлов там говорится?
Почему металлы непрозрачные?
Почему для металлов характерен светлый цвет и блеск? (Металлический блеск).
Какие металлы, в отличие от остальных, имеют цвет? В чем причина красноватого цвета меди и желтого цвета золота и светло – желтого у стронция?
Все ли металлы твердые? Что вы можете сказать о температуре плавления разных металлов?
Почему одинаковые по размеру металлы имеют различную массу?
Назовите самые тяжелые металлы и самые легкие.
Почему металлы можно ковать, штамповать, вытягивать в проволоку?
Почему металлы подвержены пластической деформации?
Вы проделали опыт с двумя стеклянными пластинами. Как можете его прокомментировать?
Для чего металлы куют? (просмотр видеоролика ковкость).
Что вы можете сказать после опыта с ложками, изготовленными из разных металлов, и горячей водой? Одинакова ли теплопроводность различных металлов? Чем она объясняется?
Какое ещё свойство металлов объясняется подвижностью электронов? (электропроводность). Что появится в куске металла, если электронам придать направленное движение?
Какие металлы лучше остальных проводят ток?
Почему магнит притягивает гвоздь? (обладает магнитными свойствами). Как классифицируют металлы в зависимости от магнитных свойств? (ферромагнетики, парамагнетики и диамагнетики)
Привести пример. Ветеран Вов, артиллерист, вспоминал: «На курской дуге были и такие случаи, когда направление стрельбы определяли по звездам, по луне, по направлению ЖД, но только не по компасу. Почему?
Самостоятельное творческое использование сформированных умений и навыков.
Фронтальная работа со слайдом «Применение металлов».
Динамическая пауза.
Прослушивание колокольного звона
Обобщение усвоенного и включение его в систему ранее усвоенных ЗУНов и УУД.
Заполнить пропуски в таблице «Применение металлов на основе их физических свойств»
Физическое свойство
Применение
Входят в основу сплавов, использующихся в технике и машиностроении
Сверло для дрели, стальное лезвие
Электропроводность
Ковка, прокатка, штамповка
Радиаторы отопления, металлическая посуда
Металлический блеск
«Ни едино художество, ни едино ремесло простое употребления металлов миновать не может». М.В. Ломоносов.
9. Рефлексия деятельности.
Продолжить предложения:
Сегодня на уроке я:
-научился……
-было интересно……
-было трудно……
-мои ощущения……
10. Домашнее задание.
Подготовить сообщения на тему «Сверхпроводимость»,
infourok.ru
Источник
Физические свойства металлов отличают их от неметаллов. Все металлы, кроме ртути, – твёрдые кристаллические вещества, являющиеся восстановителями в окислительно-восстановительных реакциях.

Положение в таблице Менделеева
Металлы занимают I-II группы и побочные подгруппы III-VIII групп. Металлические свойства, т.е. способность отдавать валентные электроны или окисляться, увеличиваются сверху вниз по мере увеличения количества энергетических уровней. Слева направо металлические свойства ослабевают, поэтому наиболее активные металлы находятся в I-II группах, главных подгруппах. Это щелочные и щелочноземельные металлы.
Определить степень активности металлов можно по электрохимическому ряду напряжений. Металлы, стоящие до водорода, наиболее активны. После водорода стоят слабоактивные металлы, не вступающие в реакцию с большинством веществ.

Рис. 1. Электрохимический ряд напряжений металлов.
Строение
Вне зависимости от активности все металлы имеют общее строение. Атомы в простом металле расположены не хаотично, как в аморфных веществах, а упорядоченно – в виде кристаллической решётки. Удерживает атомы в одном положении металлическая связь.
Такой вид связи осуществляется за счёт положительно заряженных ионов, находящихся в узлах кристаллической ячейки (единицы решётки), и отрицательно заряженных свободных электронов, которые образуют так называемый электронный газ. Электроны отделились от атомов, превратив их в ионы, и стали перемещаться в решётке хаотично, скрепляя ионы вместе. Без электронов решётка бы распалась за счёт отторжения одинаково заряженных ионов.
Различают три типа кристаллической решётки. Кубическая объемно-центрированная состоит из 9 ионов и характерна хрому, железу, вольфраму. Кубическая гранецентрированная включает 14 ионов и свойственная свинцу, алюминию, серебру. Из 17 ионов состоит гексагональная плотноупакованная решётка цинка, титана, магния.

Рис. 2. Виды кристаллических решёток.
Свойства
Строение кристаллической решётки определяет основные физические и химические свойства металлов. Металлы блестят, плавятся, проводят тепло и электричество. Промышленность и металлургия нашли применение физическим свойствам металлов в изготовлении деталей, фольги, корпусов машин, зеркал, бытовой и промышленной химии. Особенности металлов и их использование представлены в таблице физических свойств металлов.
Свойства | Особенности | Примеры | Применение |
Металлический блеск | Способность отражать солнечный свет | Наиболее блестящими металлами являются Hg, Ag, Pd | Изготовление зеркал |
Плотность | Лёгкие – имеют плотность меньше 5 г/см3 | Na, K, Ba, Mg, Al. Самый лёгкий металл – литий с плотностью 0,533 г/см3 | Изготовление облицовки, деталей самолётов |
Тяжёлые – имеют плотность больше 5 г/см3 | Sn, Fe, Zn, Au, Pb, Hg. Самый тяжёлый – осмий с плотностью 22,5 г/см3 | Использование в сплавах | |
Пластичность | Способность изменять форму без разрушений (можно раскатать в тонкую фольгу) | Наиболее пластичные – Au, Cu, Ag. Хрупкие – Zn, Sn, Bi, Mn | Формовка, сгибание труб, изготовление проволоки |
Твёрдость | Мягкие – режутся ножом | Na, K, In | Изготовление мыла, стекла, удобрений |
Твёрдые – сравнимы по твёрдости с алмазом | Самый твёрдый – хром, режет стекло | Изготовление несущих конструкций | |
Температура плавления | Легкоплавкие – температура плавления ниже 1000°С | Hg (38,9°С), Ga (29,78°С), Cs (28,5°С), Zn (419,5°C) | Производство радиотехники, жести |
Тугоплавкие – температура плавления выше 1000°С | Cr (1890°С), Mo (2620°С), V (1900°С). Наиболее тугоплавкий – вольфрам (3420°С) | Изготовление ламп накаливания | |
Теплопроводность | Способность передавать тепло другим телам | Лучше всего проводят ток и тепло Ag, Cu, Au, Al | Приготовление пищи в металлической посуде |
Электропроводность | Способность проводить электрический ток за счёт свободных электронов | Передача электричества по проводам |
Рис. 3. Примеры применения металлов.
Что мы узнали?
Из урока 9 класса узнали о физических свойствах металлов. Кратко рассмотрели положение металлов в периодической таблице и особенности строения кристаллической решётки. Благодаря строению металлы обладают пластичностью, твёрдостью, способностью плавиться, проводить электрический ток и тепло. Свойства металлов неоднородны. Различают лёгкие и тяжёлые металлы, лёгкоплавкие и тугоплавкие, мягкие и твёрдые. Физические свойства используются для изготовления сплавов, электрических проводов, посуды, мыла, стекла, конструкций различной формы.
Тест по теме
Оценка доклада
Средняя оценка: 4.2. Всего получено оценок: 134.
Источник
