Какие именно электроны отвечают за свойства атомов

Атомно-молекулярное учение
Мы приступаем к изучению химии – мира молекул и атомов. В этой статье мы рассмотрим базисные понятия и разберемся с электронными
формулами элементов.
Атом (греч. а – отриц. частица + tomos – отдел, греч. atomos – неделимый) – электронейтральная частица вещества микроскопических
размеров и массы, состоящая из положительно заряженного ядра (протонов) и отрицательно заряженных электронов (электронные орбитали).
Описываемая модель атома называется “планетарной” и была предложена в 1913 году великими физиками: Нильсом Бором и Эрнестом Резерфордом

Протон (греч. protos – первый) – положительно заряженная (+1) элементарная частица, вместе с нейтронами образует ядра атомов
элементов. Нейтрон (лат. neuter – ни тот, ни другой) – нейтральная (0) элементарная частица, присутствующая в ядрах всех
химических элементов, кроме водорода.
Электрон (греч. elektron – янтарь) – стабильная элементарная частица с отрицательным электрическим зарядом (-1), заряд атома –
порядковый номер в таблице Менделеева – равен числу электронов (и, соответственно, протонов).
Запомните, что в невозбужденном состоянии атом содержит одинаковое число электронов и протонов. Так у кальция (порядковый номер 20)
в ядре находится 20 протонов, а вокруг ядра на электронных орбиталях 20 электронов.

Я еще раз подчеркну эту важную деталь. На данном этапе будет отлично, если вы запомните простое правило:
порядковый номер элемента = числу электронов. Это наиболее важно для практического применения и изучения следующей темы.
Электронная конфигурация атома
Электроны атома находятся в непрерывном движении вокруг ядра. Энергия электронов отличается друг от друга, в соответствии с этим
электроны занимают различные энергетические уровни.
Энергетические уровни подразделяются на несколько подуровней:
- Первый уровень
- Второй уровень
- Третий уровень
- Четвертый уровень
Состоит из s-подуровня: одной “1s” ячейки, в которой помещаются 2 электрона (заполненный электронами – 1s2)
Состоит из s-подуровня: одной “s” ячейки (2s2) и p-подуровня: трех “p” ячеек (2p6), на которых
помещается 6 электронов
Состоит из s-подуровня: одной “s” ячейки (3s2), p-подуровня: трех “p” ячеек (3p6) и d-подуровня:
пяти “d” ячеек (3d10), в которых помещается 10 электронов
Состоит из s-подуровня: одной “s” ячейки (4s2), p-подуровня: трех “p” ячеек (4p6), d-подуровня:
пяти “d” ячеек (4d10) и f-подуровня: семи “f” ячеек (4f14), на которых помещается 14
электронов

Зная теорию об энергетических уровнях и порядковый номер элемента из таблицы Менделеева, вы должны расположить определенное число
электронов, начиная от уровня с наименьшей энергией и заканчивая к уровнем с наибольшей. Чуть ниже вы увидите несколько примеров, а
также узнаете об исключении, которое только подтверждает данные правила.
Подуровни: “s”, “p” и “d”, которые мы только что обсудили, имеют в определенную конфигурацию в пространстве. По этим подуровням, или
атомным орбиталям, движутся электроны, создавая определенный “рисунок”.
S-орбиталь похожа на сферу, p-орбиталь напоминает песочные часы, d-орбиталь – клеверный лист.

Правила заполнения электронных орбиталей и примеры
Существует ряд правил, которые применяют при составлении электронных конфигураций атомов:
- Сперва следует заполнить орбитали с наименьшей энергией, и только после переходить к энергетически более высоким
- На орбитали (в одной “ячейке”) не может располагаться более двух электронов
- Орбитали заполняются электронами так: сначала в каждую ячейку помещают по одному электрону, после чего орбитали дополняются
еще одним электроном с противоположным направлением - Порядок заполнения орбиталей: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s
Должно быть, вы обратили внимание на некоторое несоответствие: после 3p подуровня следует переход к 4s, хотя логично было
бы заполнить до конца 4s подуровень. Однако природа распорядилась иначе.
Запомните, что, только заполнив 4s подуровень двумя электронами, можно переходить к 3d подуровню.
Без практики теория мертва, так что приступает к тренировке. Нам нужно составить электронную конфигурацию атомов углерода и
серы. Для начала определим их порядковый номер, который подскажет нам число их электронов. У углерода – 6, у серы – 16.
Теперь мы располагаем указанное количество электронов на энергетических уровнях, руководствуясь правилами заполнения.

Обращаю ваше особе внимание: на 2p-подуровне углерода мы расположили 2 электрона в разные ячейки, следуя одному из правил.
А на 3p-подуровне у серы электронов оказалось много, поэтому сначала мы расположили 3 электрона по отдельным ячейкам, а оставшимся
одним электроном дополнили первую ячейку.
Таким образом, электронные конфигурации наших элементов:
- Углерод – 1s22s22p2
- Серы – 1s22s22p63s23p4
Внешний уровень и валентные электроны
Количество электронов на внешнем (валентном) уровне – это число электронов на наивысшем энергетическом уровне, которого достигает элемент. Такие электроны называются валентными: они могут быть спаренными или неспаренными. Иногда
для наглядного представления конфигурацию внешнего уровня записывают отдельно:
- Углерод – 2s22p2 (4 валентных электрона)
- Сера -3s23p4 (6 валентных электронов)
Неспаренные валентные электроны способны к образованию химической связи. Их число соответствует количеству связей, которые данный атом может образовать с другими атомами. Таким образом неспаренные валентные электроны тесно связаны с валентностью – способностью атомов образовывать определенное число химических связей.

- Углерод – 2s22p2 (2 неспаренных валентных электрона)
- Сера -3s23p4 (2 неспаренных валентных электрона)
Тренировка
Потренируйтесь и сами составьте электронную конфигурацию для магния и скандия. Определите число электронов на внешнем (валентном) уровне и число неспаренных
электронов. Ниже будет дано наглядное объяснение этой задаче.

Запишем получившиеся электронные конфигурации магния и фтора:
- Магний – 1s22s22p63s2
- Скандий – 1s22s22p63s23p64s23d1
В целом несложная и интересная тема электронных конфигураций отягощена небольшим исключением – провалом электрона, которое только подтверждает общее
правило: любая система стремится занять наименее энергозатратное состояние.
Провал электрона
Провалом электрона называют переход электрона с внешнего, более высокого энергетического уровня, на предвнешний, энергетически более
низкий. Это связано с большей энергетической устойчивостью получающихся при этом электронных конфигураций.
Подобное явление характерно лишь для некоторых элементов: медь, хром, серебро, золото, молибден. Для примера выберем хром, и рассмотрим
две электронных конфигурации: первую “неправильную” (сделаем вид, будто мы не знаем про провал электрона) и вторую правильную, написанную
с учетом провала электрона.
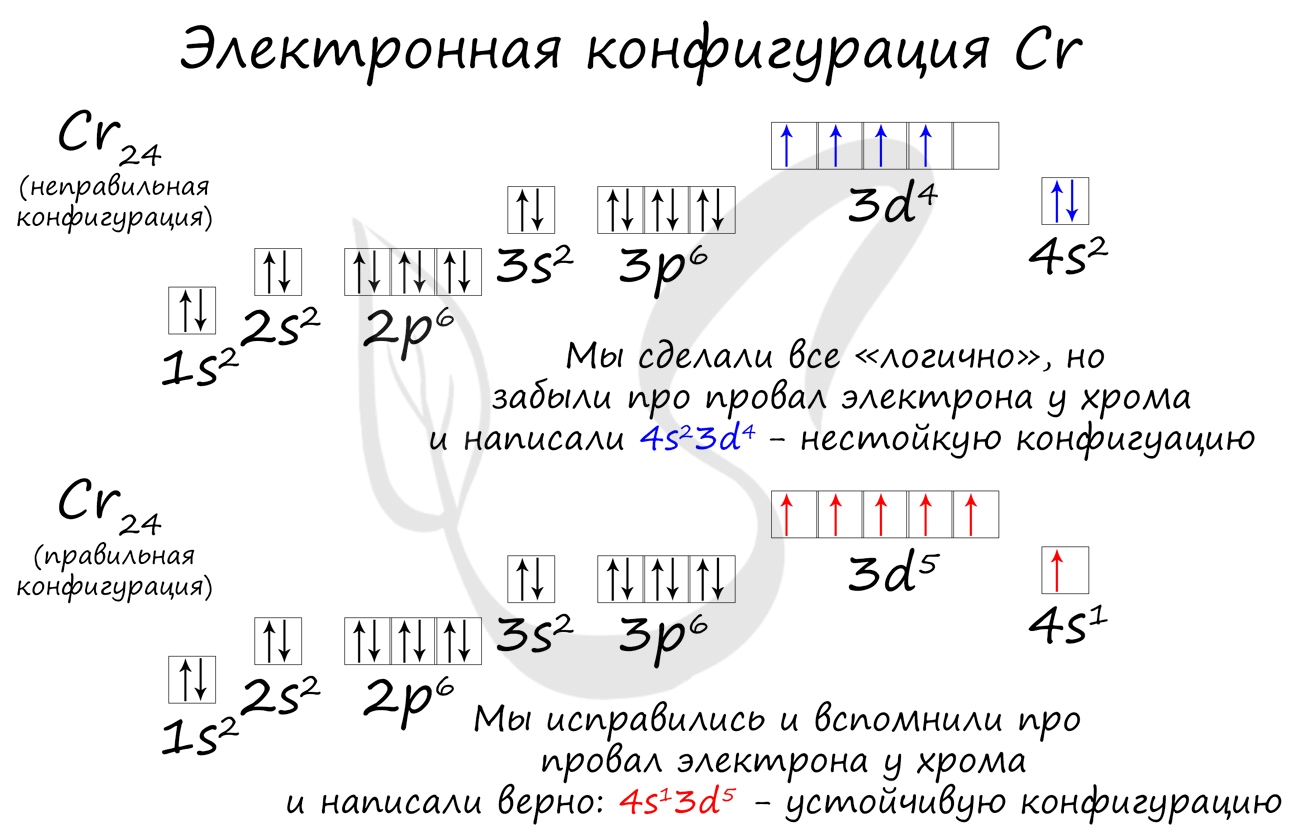
Теперь вы понимаете, что кроется под явлением провала электрона. Запишите электронные конфигурации хрома и меди самостоятельно еще раз и
сверьте с представленными ниже.

Основное и возбужденное состояние атома
Основное и возбужденное состояние атома отражаются на электронных конфигурациях. Возбужденное состояние связано с движением электронов
относительно атомных ядер. Говоря проще: при возбуждении пары электронов распариваются и занимают новые ячейки.
Возбужденное состояние является для атома нестабильным, поэтому долгое время в нем он пребывать не может. У некоторых атомов: азота,
кислорода , фтора – возбужденное состояние невозможно, так как отсутствуют свободные орбитали (“ячейки”) – электронам некуда перескакивать, к тому
же d-орбиталь у них отсутствует (они во втором периоде).
У серы возможно возбужденное состояние, так как она имеет свободную d-орбиталь, куда могут перескочить электроны. Четвертый энергетический
уровень отсутствует, поэтому, минуя 4s-подуровень, заполняем распаренными электронами 3d-подуровень.
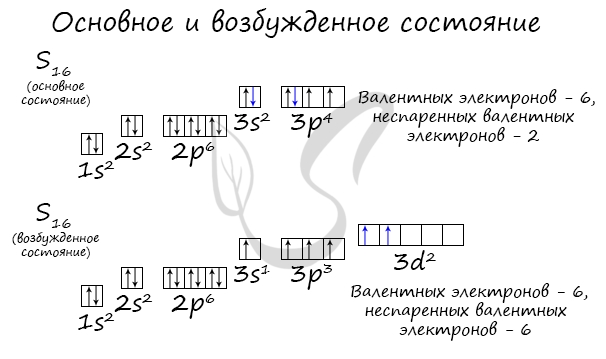
По мере изучения основ общей химии мы еще не раз вернемся к этой теме, однако хорошо, если вы уже сейчас запомните, что возбужденное состояние
связано с распаривание электронных пар.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
Атомы – мельчайшие частицы, из которых состоит все вокруг: все, что нас окружает, состоит из молекул, состоящих из атомов. Их невозможно увидеть с использованием каких бы то ни было увеличительных приборов в силу их невероятно маленьких размеров. Но ведь атомы тоже должны из чего-то состоять. Значит, должны существовать еще более маленькие частицы. Сразу говорю, это довольна непростая для понимания тема, поэтому текста много, да и читать нужно вдумчиво. Тем не менее, это крайне увлекательно – знать о настолько малых частицах, которые невозможно даже увидеть. Что ж, давайте разбираться!
Немного о самом атоме
Вообще, термин “атом” был изобретен очень давно: за 400 лет до н. э. греческий философ Демокрит выдвинул идею, что вещество можно делить до тех пор, пока не будут получены его наименьшие возможные частицы, названные атомами. Конечно, в гипотезе Демокрита атомы являются совсем не тем, чем их считают сейчас, но, тем не менее, идея атомизма очень древняя. В 1808 г. химик Джон Дальтон сформулировал атомистическую теорию: все вещества состоят из атомов, мельчайших неделимых частиц, которые нельзя ни создать, ни уничтожить. Также, Дальтон утверждал, что атомы одного и того же элемента абсолютно одинаковы. Так зародилась атомистическая теория, и было заложено начало к изучению самих атомов.
Теперь немного о характеристиках атома. Не для кого не секрет, что атом чрезвычайно мал. Но даже его можно измерить – а именно указать его массу и диаметр. Диаметры атомов в среднем – 0,2 нм (0,0000000002 м). Массы рознятся сильнее: от 10 в минус 27 степени (ноль с двадцатью шестью нолями и единицей после запятой) кг до 10 в минус 25 степени ( ноль с двадцатью четырьмя нолями и единицей после запятой) кг. Для избежания участия столь малых цифр в расчетах, массы атомов обычно выражают в атомных единицах массы (а. е. м.). 1 а. е. м. = 1,661 на 10 в минус 27 степени.
Какие частицы входят в состав атома?
Мы уже представляли себе атом таким, каким его рисуют в sci-fi фильмах: ядро, состоящее из протонов и нейтронов в центре, и электроны, вращающиеся вокруг ядра. Но что представляют из себя протоны, нейтроны и электроны?
Строение атома из фильмов, отражающее частицы, входящие в него
Нейтрон – это элементарная незаряженная частица. Электрический заряд равен 0 е, масса равна 1 а. е. м. Нейтрон был открыт в 1932 г. Чедвиком в ходе ядерной реакции между атомами бериллия и гелия. Нейтрон входит в состав атомного ядра
Протон – это элементарная положительная частица. Электрический заряд равен +1 е, масса равна 1 а. е. м. Открыт в 1919 г. Резерфордом. Входит в состав атомного ядра вместе с нейтроном, представляет собой ядро атома водорода.
Электрон – это элементарная отрицательная частица. Электрический заряд равен -1 е (равен по модулю заряду протона), масса равна 0,00054 а. е. м., поэтому для простоты расчетов считается, что электрон не имеет массы. Открыт в 1897 г. Томсоном при изучении поведения катодных лучей (электронов) в магнитном и электрическом поле. Электроны не входят в состав ядра, а находятся снаружи, двигаясь по специальным траекториям, но об этом позднее.
Как частицы располагаются в атоме?
Ученые Гейгер и Марсден в 1909 г. проводили бомбардировку золотой фольги альфа-частицами (ядрами гелия). Частицы проходили через фольгу, как и ожидалось, однако, малая их часть отражалась обратно. Примерно 1 из 8000 частиц отскакивали. Был сделан вывод, что частицы сталкиваются с положительными и тяжелыми центрами, которые должны располагаться в ничтожно малой части атома, раз так мало частиц отражается обратно. Так появилось представление об атомном ядре: отражались только те частицы, которые сталкивались с ядрами. Таким образом, атомное ядро имеет намного меньший размер, чем сам атом; остальное пространство в атоме занимают электроны. И если с ядром все понятно – лишь малая часть атома, состоящая из протонов и нейтронов, то с электронами все сложнее.
В 1925 г. Шредингер сформулировал свое уравнение, названное в его честь. Оно позволяло проследить поведение электрона в атоме. Однако, в силу принципа неопределенности Гейзенберга (электрон обладает частично-волновым дуализмом) нельзя определить точное положение электрона и его скорость. Можно лишь говорить об области пространства, где электрон находится чаще. Так появился термин атомная орбиталь – это место, где вероятность нахождения электрона составляет больше 90%. Вот и получаем первое различие с изображениями из фильмов: там электроны вращаются вокруг ядра, оставляя следы в виде полосок. На деле электроны как бы расплываются вокруг ядра. Физик Бор сформулировал постулат о том, что электроны могут обладать определенным количеством энергии, а не произвольным. Так были введены квантовые числа:
- главное квантовое число (n, положительное целое число – 1, 2, 3…) характеризует энергетический уровень электрона и указывает число подуровней на уровне;
- орбитальное квантовое число (l, неотрицательное целое число – 0, 1, 2…) характеризует форму атомной орбитали, на которой находится электрон;
- магнитное квантовое число (ml, целое число от -l до +l) характеризует количество атомных орбиталей на энергетическом подуровне;
- спиновое квантовое число (ms, значения – либо -1/2, либо +1/2) характеризует вращение электрона относительно собственной оси.
У каждого электрона в атоме свой набор квантовых чисел, на основании которых можно оценить его энергию, по которой можно судить о его местоположении в атоме. В заполнении электронами атомных орбиталей участвуют некоторые закономерности. Одна из них – это запрет Паули. Он гласит о том, что в атоме не может быть двух электронов с одинаковыми наборами всех квантовых чисел, т. е. обладающих одинаковыми энергиями.
Немного об атомных орбиталях
Другое отличие реального атома от киношного изображения – это изображение атомных орбиталей. На картинках электроны движутся по окружностям. В реальности электроны не только расплываются, но и делают это по определенной области – орбитали. На каждой атомной орбитали может находится только 2 электрона. Всего различают 5 видов орбиталей в зависимости от значения орбитального квантового числа l:
- l = 0 – s-орбиталь;
- l = 1 – p-орбиталь;
- l = 2 – d-орбиталь;
- l = 3 – f-орбиталь;
- l = 4 – g-орбиталь.
s-орбиталь представляет собой симметричную относительно ядра сферу. Вероятность нахождения электрона на каждом участке орбитали одинакова. Всего на s-орбитали может располагаться два электрона.
s-орбиталь
p-орбиталь представляет собой форму гантели. Она направлена в трех разных направлениях – по координатным осям x, y и z и в совокупности они образуют энергетический подуровень.
p-орбитали, направленные по разным осям
d-, f- и g-орбитали имеют еще намного более сложные формы, чем p-орбиталь, поэтому их описание не представляется целесообразным.
Формы d-орбиталей, по-разному расположенных в пространстве
Каждое значение орбитального числа l является энергетическим подуровнем атома. Для каждого следующего энергетического уровня количество энергетических подуровней увеличивается и содержит в себе подуровни прошлых уровней. Звучит сложновато, да. Говоря проще, чем больше значение n, тем больше ему соответствует значений l. Попробуем на примере. Значение главного числа n задает основной энергетический уровень. Например: n=1, тогда l=0. Это значит, что на первом энергетическом уровне есть только один подуровень с одной s-орбиталью. Теперь пусть n=2. Это второй энергетический уровень. Для него l=0 и l=1. Это значит, что на нем два подуровня: на одном s-орбиталь, а на другом p-орбиталь. Для n=3 уже 3 подуровня и т. д. Такое заполнение электронами орбиталей является еще одной закономерностью, называемой правилом Клечковского. Правило Клечковского гласит о том, что электроны заполняют атомные орбитали так, чтобы их суммарная энергия была минимальна, т. е. начиная с меньших энергетических уровней.
Пример сопоставления энергетическим уровням (n) энергетических подуровней (l) и орбиталей
Теперь давайте поговорим о заполнении непосредственно орбиталей. Представим себе s-орбиталь: сфера вокруг ядра, на которой есть 2 электрона: спиновое число одного – 1/2, другого – -1/2. Теперь представим себе p-орбиталь в форме гантели. Три p-орбитали (направленные по координатным осям) образуют энергетический подуровень. Поскольку на каждой орбитали может быть по 2 электрона, то на таком подуровне может быть всего 6 электронов. Но как они его заполняют? Допустим, у нас есть 4 электрона. Заполняют ли они сначала одну орбиталь, затем другую, а третью оставляют нетронутой? Здесь на помощь приходит третья закономерность – правило Гунда. Оно гласит, что электроны при заполнении подуровней занимают максимальное число свободных орбиталей. Таким образом, сначала по один займет каждую орбиталь, а затем еще один займет полузаполненную орбиталь. Таким образом, две орбитали будут заполнены наполовину, а одна полностью.
Так устроен атом. Подведем итоги. В маленькой части атома, в центре, располагается атомное ядро, состоящее из протонов и нейтронов. Вокруг располагаются энергетические уровни с подуровнями, на которых находятся орбитали разной формы – места, где скорее всего находятся электроны в данный момент времени. Электроны заполняют орбитали в соответствии запретом Паули, правилом Клечковского и правилом Гунда.
Если Вам понравилась статья, подписывайтесь на канал и ставьте лайки!
Источник
