Какие из перечисленных химических свойств характерны для метана

Самостоятельная работа
по теме: «Химические свойства и способы получения алканов»
Iвариант
1. Для предельных углеводородов характерны реакции:
а) горения, б) замещения, в) присоединения. г) нейтрализации?
Составьте соответствующие уравнения реакций.
2. Дана цепочка превращений
1 2 3
С2Н6→С2Н5Cl→С4Н10→CO2:
вторая реакция называется а) Коновалова, б) Вюрца, в) Семенова.
Составьте уравнения всех реакций.
3. Какое соединение используется для получения метана в лаборатории:
а) СНзСООН, б) СН3ОН, в) СН3С1, г) СH3СООNа
Составьте уравнение этой реакции.
4. Массовые доли углерода и водорода в углеводороде равны соответственно
82,76% и 17,24%. Плотность его паров по водороду составляет 29. Выведите формулу вещества. Число атомов водорода в молекуле равно а) 12; б) 6; в) 10 г) 14.
Приведите для данного углеводорода два гомолога и два изомера и дайте им названия.
Самостоятельная работа по теме:
«Химические свойства и способы получения алканов»
IIвариант
1. Какие из перечисленных химических свойств характерны для метана:
а) гидрирование, б) изомеризация, в) горение, г) каталитическое окисление?
Составьте соответствующие уравнения реакций.
2. В результате следующих превращений
Cl2hl Na
СН4 → Х1 → Х2
образуется конечный продукт (Х2)
а) пропан, б) хлорэтан, в) этан, г) хлорметан?
Напишите уравнения всех реакций.
3. Укажите, какое соединение используется для получения этана (по реакции
Вюрца): а) С2Н4, б) СН3I, в) СН3 – О – СН3, г) С2Н5ОН?
Составьте уравнение соответствующей реакции .
4. Массовая доля углерода в алкане составляет 81,82%.,водорода 18,18% . Относительная
плотность его паров по воздуху равна 1,518. Определите формулу алкана. Число атомов углерода в молекуле алкана равно а) 4; б) 2; в) 6; г) 3.
Приведите для данного углеводорода два гомолога и два изомера и дайте им названия.
Самостоятельная работа по теме:
«Химические свойства и способы получения алканов»
IIIвариант
1. Укажите, какие из перечисленных реакций характерны для бутана:
а) присоединения, б) крекинг, в) изомеризация, г) дегидрирования.
Составьте уравнения этих реакций.
2. По какой реакции можно получить в лаборатории метан:
а) СН3ОН + Н2→ б) СН3Вг +Nа→
в) СаС2+ Н20 → г) А14С3+ Н20 →
Составьте уравнение соответствующей реакции.
3. Укажите условия, которые необходимы для начала реакции между этаном и хлором: а) охлаждение, б) нагревание, в) повышение давления, г) освещение. Составьте уравнение соответствующей реакции
4. Массовые доли углерода и водорода в углеводороде равны соответственно 81,8% и 18,2%. Плотность его паров по водороду составляет 22.
Число атомов водорода в молекуле вещества равно а) 8; б) 6; в) 3; г)12.
Приведите для данного углеводорода два гомолога и два изомера и дайте им названия.
Самостоятельная работа по теме:
«Химические свойства и способы получения алканов»
IVвариант
1. Определите, с какими из приведенных веществ и при каких условиях
взаимодействует метан: а) гидроксид натрия, б) бром, в) азотная кислота, г) кислород.
Составьте уравнения соответствующих реакций.
2. Дана цепочка превращений
1 2 3
СН4→СН3Вг→С2Н6→С2Н5NO2
третья реакция называется реакцией:
а) Вюрца, б) Коновалова, в) Семёнова?
Составьте уравнения всех реакций.
Укажите продукт полного хлорирования метана: а) хлороформ, б) хлорметан, в) дихлорметан, г) тетрахлорметан. Составьте уравнение соответствующей реакции.
4 .Найдите молекулярную формулу углеводорода, массовая доля углерода в котором составляет 84,21 %. Относительная плотность его по гелию равна 28,5.
а) С5Н8, б) С8Н18, в) С3Н8, г) С7Н16
Составьте для этого углеводорода два гомолога и два изомера. Дайте им названия.
Источник
Анонимный вопрос
16 декабря 2018 · 2,2 K
Подготовила к ЕГЭ по химии 5000 учеников. С любого уровня до 100 в режиме онлайн 🙂 · vk.com/mendo_him
????метан????
❗️формула СН4
❗️Физические свойства:
-газ
-без цвета ,запаха
❗️химические свойства:
-хлорирование
СН4+Cl2➡️CH3Cl+HCl
-нитрование
СН4+HNO3➡️CH3NO2+H2O
-конверсия
СН4+Н2О➡️СО+3Н2
-окисление
СН4+2О2➡️СО2+2Н2О
Как получить метан из оксида углерода?
Подготовила к ЕГЭ по химии 5000 учеников. С любого уровня до 100 в режиме онлайн 🙂 · vk.com/mendo_him
????Получаем метан из CO2????
✅CO2+4H2➡️CH4+2H2O
✅Эта реакция проходит при температуре до 200° с использованием катализатора CuO
✅Это промышленный способ получения метана
Насколько достоверны утверждения о том, как пагубно влияют на организм анаболические стероиды?
Это не только известно достоверно, но куча проф. спортсменов от них умерла. Забейте в Яндексе “Андреас Мюнцер” и почитайте биографию, до конца, и увидите в каких муках он умирал. Но это профи. А любителей с загубленным здоровьем тоже немало. Вам просто никто не признается какие проблемы от стероидов он заимел. Я думаю, их стоит принимать только по назначению врача. Гормоналку они не раскачают, а атрофируют. От них увеличивается сердце, сосуды забиваются холестерином и куча других проблем. Если вы не профи, оно вам надо? Быть в форме можно в любом возрасте и без стероидов. Стероиды дают возможность лениться – не убиваться на тренировках и есть все, что хочешь. Можно быть красавцем в любом возрасте и без стероидов, но нужно много пахать в зале, бегать, читать о тренировках, продумывать их, планировать и во многом вкусном себе отказывать. Со стероидами вы получите результат “нахаляву”, тренируясь умеренно, но заплатите здоровьем. Потом, результаты на искусственных гормонах нестабильны. Вы должны “учить” организм вырабатывать свои гормоны и эффективно восстанавливаться, приспосабливаясь к нагрузкам (так и идет прогресс) – именно в этом смысл тренировок для любителя, а не в увеличении силовых и массы, как многие ошибочно считают.
Прочитать ещё 3 ответа
Как из водорода получить метан?
Водород может получаться при сильном нагревании метана.
Поэтому в промышленности большое количество водорода получают именно из метана, добавляя к нему при высокой температуре перегретый водяной пар:
1) CH4 + H2O = CO + 3 H2
2) CO + H2O = CO2 + H2
В сумме этот процесс можно записать уравнением:
CH4 + 2 H2O = 4 H2 + CO2
Горит ли кислород?
Процес горения – требует 3 составляющие.
- топливо
- достаточная температура
- окислитель
Вещества вступающие в реакцию горения выступают в роли окислителя и восстановителя.
Топливо это Восстановитель отдающий электроны.
Окислитель же принимает электроны.
Чтобы кислород выступал в качестве восстановителя и “горел” нужно нагреть его после чего добавить фтор, чтобы фтор начал окислять кислород.
Записей с горением кислорода нету по 2-м причинам:
- Крайне высокая температура для начала реакции
- Низкая интенсивность реакции
Чем выше и левее находится вещество в таблице Менделеева тем больше его Восстановительные качества.
Чем выше и правее тем больше Окислительные качества.
(Рассматривать только вещества с незавершенными внешними электронными слоями)
Горение различных вещест во вторе (при комнатной температуре))
Прочитать ещё 2 ответа
Источник
Метан, получение, свойства, химические реакции.
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Метан, CH4 – простейший по составу предельный углеводород, органическое вещество класса алканов. В природе содержится в природном газе, добываемом из газовых и газоконденсатных месторождений, в попутном нефтяном газе, в рудничном и болотном газах. Растворен в нефти, в пластовых и поверхностных водах. В твердом состоянии встречается в виде газогидратов.
Метан, формула, газ, характеристики
Физические свойства метана
Химические свойства метана
Получение метана в промышленности и лаборатории
Химические реакции – уравнения получения метана
Применение и использование метана
Метан, формула, газ, характеристики:
Метан (лат. methanum) – простейший по составу предельный углеводород, органическое вещество класса алканов, состоящий из одного атома углерода и четырех атомов водорода.
Химическая формула метана CH4, рациональная формула CH4. Изомеров не имеет.
Строение молекулы:

Метан – в обычных условиях лёгкий бесцветный газ, без вкуса и запаха. Однако в метан, используемый в качестве технического газа, могут добавляться одоранты — вещества, имеющие резкий неприятный запах для предупреждения его утечки.
Метан – это основной компонент природного газа.
Является одним из парниковых газов. Его вклад в парниковый эффект составляет 4-9 %.
В природе содержится в природном газе, добываемом из газовых и газоконденсатных месторождений, в попутном нефтяном газе. Для выделения из природного и попутного нефтяного газа производят их очистку и сепарацию газа. Также содержится в рудничном и болотном газах (отсюда произошли другие названия метана – болотный или рудничный газ), свалочном газе.
В анаэробных условиях (в болотах, переувлажнённых почвах, на дне прудов и стоячих вод, где он образуется при разложении растительных остатков без доступа воздуха, в кишечнике жвачных животных, биореакторах, биогазовых установках и пр.) образуется биогенно в результате жизнедеятельности некоторых микроорганизмов.
В растворенном виде содержится в нефти, в пластовых и поверхностных водах. При переработке нефти метан выделяют отдельно для дальнейшего использования.
Помимо газообразного состояния в природе встречается еще и в твердом состоянии на дне морей, океанов и в зоне вечной мерзлоты в виде метаногидратов (гидратов природного газа), именуемых «горючий лёд».
Также содержится в сланцевой нефти, сланцевом газе и сжиженном газе (сжиженном природном газе).
Пожаро- и взрывоопасен.
Почти не растворяется в воде и других полярных растворителях. Зато растворяется в некоторых неполярных органических веществах (метанол, ацетон, бензол, тетрахлорметан, диэтиловый эфир и другие).
Метан по токсикологической характеристике относится к веществам 4-го класса опасности (малоопасным веществам) по ГОСТ 12.1.007.
Физические свойства метана:
| Наименование параметра: | Значение: |
| Цвет | без цвета |
| Запах | без запаха |
| Вкус | без вкуса |
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | газ |
| Плотность (при 20 °C и атмосферном давлении 1 атм.), кг/м3 | 0,6682 |
| Плотность (при 0 °C и атмосферном давлении 1 атм.), кг/м3 | 0,7168 |
| Плотность (при -164,6 °C и атмосферном давлении 1 атм.), кг/м3 | 415 |
| Температура плавления, °C | -182,49 |
| Температура кипения, °C | -161,58 |
| Температура самовоспламенения, °C | 537,8 |
| Критическая температура*, °C | -82,4 |
| Критическое давление, МПа | 4,58 |
| Критический удельный объём, м3/кг | 0,0062 |
| Взрывоопасные концентрации смеси газа с воздухом, % объёмных | от 4,4 до 17,0 |
| Удельная теплота сгорания, МДж/кг | 50,1 |
| Коэффициент теплопроводности (при 0 °C и атмосферном давлении 1 атм.), Вт/(м·К) | 0,0302 |
| Коэффициент теплопроводности (при 50 °C и атмосферном давлении 1 атм.), Вт/(м·К) | 0,0361 |
| Молярная масса, г/моль | 16,04 |
| Растворимость в воде, г/кг | 0,02 |
* при температуре выше критической температуры газ невозможно сконденсировать ни при каком давлении.
Химические свойства метана:
Метан трудно вступает в химические реакции. В обычных условиях не реагирует с концентрированными кислотами, расплавленными и концентрированными щелочами, щелочными металлами, галогенами (кроме фтора), перманганатом калия и дихроматом калия в кислой среде.
Химические свойства метана аналогичны свойствам других представителей ряда алканов. Поэтому для него характерны следующие химические реакции:
- 1. конверсия метана в синтез-газ:
CH4 + H2O → CО + 3H2 (kat = Ni/Al2O3 при to = 800-900 оС или без катализатора при to = 1400-1600 оС).
Образующийся в результате реакции синтез-газ может быть использован для последующих синтезов метанола, углеводородов, уксусной кислоты, ацетальдегида и других продуктов.
- 2. галогенирование метана:
CH4 + Br2 → CH3Br + HBr (hv или повышенная to);
CH4 + I2 → CH3I + HI (hv или повышенная to).
Реакция носит цепной характер. Молекула брома или йода под действием света распадается на радикалы, затем они атакуют молекулы метана, отрывая у них атом водорода, в результате этого образуется свободный метил CH3·, который сталкиваются с молекулами брома (йода), разрушая их и образуя новые радикалы йода или брома:
Br2 → Br·+ Br· (hv); – инициирование реакции галогенирования;
CH4 + Br· → CH3· + HBr; – рост цепи реакции галогенирования;
CH3· + Br2 → CH3Br + Br·;
CH3· + Br· → CH3Br; – обрыв цепи реакции галогенирования.
Галогенирование — это одна из реакций замещения. В первую очередь галогенируется наименее гидрированый атом углерода (третичный атом, затем вторичный, первичные атомы галогенируются в последнюю очередь). Галогенирование метана проходит поэтапно – за один этап замещается не более одного атома водорода.
CH4 + Br2 → CH3Br + HBr (hv или повышенная to);
CH3Br + Br2 → CH2Br2 + HBr (hv или повышенная to);
и т.д.
Галогенирование будет происходить и далее пока, не будут замещены все атомы водорода.
CH2Br2 + Br2 → CHBr3 + HBr (hv или повышенная to);
CHBr3 + Br2 → CBr4 + HBr (hv или повышенная to).
- 3. нитрование метана:
См. нитрование этана.
- 4. окисление (горение) метана:
При избытке кислорода:
CH4 + 2O2 → CO2 + 2H2O.
Горит голубоватым пламенем.
При нехватке кислорода вместо углекислого газа (СО2) получается оксид углерода (СО), при еще меньшем количестве кислорода выделяется мелкодисперсный углерод (сажа в различном виде, в т.ч. в виде графена, фуллерена и пр.) либо их смесь.
- 5. сульфохлорирование метана:
CH4 + SO2 + Cl2 → CH3-SO2Cl + … (hv).
- 6. сульфоокисление метана:
2CH4 + 2SO2 + О2 → 2CH3-SO2ОН (повышенная to).
- 7. разложение метана:
CH4 → C + 2H2 (при to > 1000 оС).
- 8. дегидрирование метана:
2CH4 → C2H2 + 3H2 (при to > 1500 оС).
- 9. каталитическое окисление метана:
В реакциях каталитического окисления метана могут образовываться спирты, альдегиды, карбоновые кислоты.
2CH4 + O2 → 2CН3OH (при to = 200 оС, kat); – образуется метанол;
CH4 + O2 → НCНO + H2O (при to = 200 оС, kat); – образуется формальдегид;
2CH4 + 3O2 → 2НCOОН + H2O (при to = 200 оС, kat); – образуется муравьиная кислота.
Получение метана в промышленности и в лаборатории. Химические реакции – уравнения получения метана:
Так как метан в большом количестве встречается в природе. Например, содержится в природном газе, попутном нефтяном газе и выделяется при крекинге нефтепродуктов, его, как правило, не получают искусственно. Его выделяют при очистке и сепарации из природного газа, ПНГ и нефти при перегонке. Кроме того, его получают из метаногидратов (гидратов природного газа), в процессе эксплуатации биогазовых установок и пр.
Метан в промышленных и лабораторных условиях получается в результате следующих химических реакций:
- 1. газификации твердого топлива:
C + 2H2 → CH4 + H2O (повышенное давление и to, kat = Ni, Mo или без катализатора).
- 2. синтеза Фишера-Тропша:
CО + 3H2 → CH4 (kat = Ni, to = 200-300 оС);
- 3. реакции взаимодействия оксида углерода (IV) и водорода:
CО2 + 4H2 → CH4 + 2H2O (kat, to = 200-300 оС);
- 4. гидролиза карбида алюминия:
Al4C3 + 12H2O → CH4 + 4Al(OH)3.
- 5. щелочного плавления солей одноосновных органических кислот
CH3-COONa + NaOH → CH4 + Na2CO3 (повышенная to).
Применение и использование метана:
– как топливо для автомобилей, судов, газовых плит, печей, паяльных ламп, зажигалок и пр. бытовых приборов;
– как сырье в химической промышленности для проведения реакций органического синтеза.
Примечание: © Фото //www.pexels.com, //pixabay.com
карта сайта
как получить метан этилен реакция ацетилен этен 1 2 вещество хлорметан метанол кислород водород связь является углекислый газ бромная вода
уравнение реакции масса объем полное сгорание моль молекула смесь превращение горение получение метана
напишите уравнение реакций метан
Коэффициент востребованности
17 393
Источник
Химические свойства метана ничем не отличаются от свойств, присущих всем веществам класса алканов. В школьном курсе химии метан изучают одним из первых веществ органики, так как он является одним из простейших представителей алканов.
В его составе один атом углерода и четыре атома водорода.
Формула метана и способы его получения
| Молекулярная формула метана | Структурная формула метана |
СH4 | Н | Н — С — Н | Н |
Метан в больших количествах содержится в атмосфере. Мы не обращаем внимания на нахождение этого газа в воздухе, ведь на нашем организме это никак не отражается, а вот канарейки очень чувствительны к метану.
Когда-то они даже помогали шахтерам спускаться под землю. Когда процентное содержание метана изменялась, птицы переставали петь. Это служило сигналом для человека, что он спустился слишком глубоко и нужно подниматься наверх.

Образуется метан в результате распада остатков живых организмов. Не случайно с английского methane переводится, как болотный газ, ведь он может быть обнаружен в заболоченных водоемах и каменноугольных шахтах.
Основным источником газа в агропромышленном комплексе является рогатый скот. Да, метан они выводят из организма вместе с остальными продуктами жизнедеятельности. Кстати, увеличение числа рогатого скота на планете может привести к разрушению озонового слоя, ведь метан с кислородом образуют взрывоопасную смесь.
Метан в промышленности можно получить с помощью нагревания углерода и водорода или синтеза водяного газа, все реакции протекают в присутствии катализатора, чаще всего никеля.
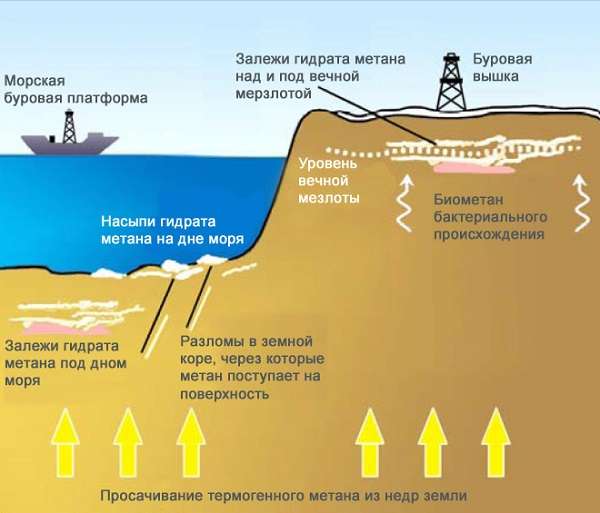
В США разработана целая система по добыче метана, она способна извлечь до 80% газа из природного угля. На сегодняшний день мировые запасы метана оцениваются экспертами в 260 триллионов метров кубических! Даже запасы природного газа значительно меньше.
В лаборатории метан получают путем взаимодействия карбида алюминия (неорганическое соединение алюминия с углеродом) и воды. Также с помощью гидроксида натрия, вступающего в реакцию с ацетатом натрия, более известного как пищевая добавка Е262.
Физические свойства метана
Характеристика:
- Бесцветный газ, без запаха.
- Взрывоопасен.
- Нерастворим в воде.
- Температура кипения: -162oC, замерзания: -183°C.
- Молярная масса: 16,044 г/моль.
- Плотность: 0,656 кг/м³.
Химические свойства метана
Говоря о химических свойствах, выделяют те реакции, в которые вступает метан. Ниже они приведены вместе с формулами.
Горение метана
Как все органические вещества, метан горит. Можно заметить, что при горении образуется голубоватое пламя.
СН4 + 2O2 → СO2↑ + 2Н2O
Называется такая реакция – реакцией горения или полного окисления.
Замещение
Метан также реагирует с галогенами. Это химические элементы 17 группы в периодической таблице Менделеева. К ним относятся: фтор, хлор, бром, йод и астат. Реакция с галогенами называется – реакцией замещения или галогенирования. Такая реакция проходит только в присутствии света.
Хлорирование и бромирование
Если в качестве галогена используется хлор, то реакция будет называться – реакцией хлорирования. Если в качестве галогена выступает бром, то – бромирование, и так далее.
CH4 + Cl2 → CH3Cl + НСl
CH4 + Br2 → CH3Br + НBr
Хлорирование. Низшие алканы могут прохлорировать полностью.
CH4 + Cl2 → CH3Cl + НСl
CH3Cl + Cl2 → CH2Сl2 + НСl
CH2Сl2+ Cl2 → CHCl3 + НСl
CHCl3 + Cl2 → CСl4 + НСl
Точно так же метан может полностью вступать в реакцию бромирования.
CH4 + Br2 → CH3Br + Н Br
CH3Br + Br2 → CH2Br2 + НBr
CH2Br2 + Br2 → CHBr3 + НBr
CHBr3 + Br2 → CBr4 + НBr
С йодом такой реакции уже нет, а с фтором наоборот сопровождается быстрым взрывом.
Разложение
Так же этому углеводороду свойственна реакция разложения. Полное разложение:
СН4 → С + 2H₂
И неполное разложение:
2СН4 → С2Н2 + 3Н2
Реакция с кислотами
Метан реагирует с концентрированной серной кислотой. Реакция носит название сульфирования и происходит при небольшом нагревании.
2СН4 + Н2SО4 → СН3SО3Н + Н2О
Окисление
Как уже было сказано, СH4 может полностью окисляться, но при недостатке кислорода возможно неполное окисление.
2СН4 + 3O2 → 2CO + 4Н2O
СН4 + О2 → С + 2Н2O
Помимо прочего для этого газа характерно каталитическое окисление. Оно происходит в присутствии катализатора. При разном соотношении моль вещества получаются разные конечные продукты реакции. В основном это:
- спирты: 2СН4 + O2 → 2СO3OН
- альдегиды: СН4 + O2 → НСОН + Н2O
- карбоновые кислоты: 2СН4 + 3O2 → 2НСОOН + 2Н2O
Реакция протекает при температуре 1500°C. Данная реакция также носит название – крекинг – термическое разложение.
Нитрование метана
Существует также реакция нитрования или реакция Коновалова, названная в честь ученого, который доказал, что с предельными углеводородами действует разбавленная азотная кислота. Продукты реакции получили название – нитросоединения.
CH4 + НNО3 → СН3NO2 + H2O
Реакция проводится при температуре 140-150°C.
Дегидрирование метана
Кроме того, для метана характерна реакция дегидрирования (разложения) – отцепление атомов водорода и получения ацетилена, в данном случае.
2CН4 → C2H2 + 3Н2
Применение метана
Метан, как и остальные предельные углеводороды, широко используется в повседневной жизни. Его применяют в производстве бензина, авиационного и дизельного топлива.
Используют в качестве базы для получения различного органического сырья на предприятиях. Также метан широко используется в медицине и косметологии.

Метан применяют для получения синтетического каучука, красок и шин.
Атлеты используют так называемый жидкий метан для быстрого набора массы за короткий промежуток времени.
А при хлорировании метана образуется вещество, которое в дальнейшем используется для обезжиривания поверхностей или как компонент в средствах для снятия лака. Некоторое время продукт взаимодействия метана и хлора использовали в качестве наркоза.
Источник
