Какие свойства характерны для соляной кислоты

Получение. Соляную кислоту получают путем растворения хлороводорода в воде.
Обратите внимание на прибор изображенный на рисунке слева. Его используют для получения соляной кислоты. Во время процесса получения соляной кислоты, следят за газоотводной трубкой, она должна находиться вблизи уровня воды, а не быть погруженной в нее. Если за этим не следить, то из-за большой растворимости хлороводорода вода попадет в пробирку с серной кислотой и 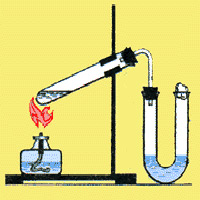 может произойти взрыв.
может произойти взрыв.
В промышленности соляную кислоту обычно получают путем сжигания водорода в хлоре и растворении продукта реакции в воде.
Физические свойства. Растворяя хлороводород в воде, можно получить даже 40% раствор соляной кислоты с плотностью 1,19 г/см3. Однако имеющаяся в продаже концентрированная соляная кислота содержит около 0,37 массовых долей, или около 37% хлороводорода. Плотность данного раствора составляет примерно 1,19 г/см3. Пр разбавлении кислоты плотность ее раствора уменьшается.
Концентрированная соляная кислота является бесценным раствором, сильно дымящая во влажном воздухе, обладающая резким запахом вследствие выделения хлороводорода.
Химические свойства. Соляная кислота обладает рядом общих свойств, которые характерны большинству кислот. Помимо этого, она обладает некоторыми специфическими свойствами.
Свойства HCL, общие с другими кислотами: 1) Изменение окраски индикаторов 2) взаимодействие с металлами 2HCL + Zn → ZnCL2 + H2↑ 3) Взаимодействие с основными и амфотерными оксидами: 2HCL + CaO → CaCl2 + H2O; 2HCL + ZnO → ZnHCL2 + H2O 4) Взаимодействие с основаниями: 2HCL + Cu (OH)2 → CuCl2 + 2H2O 5) Взаимодействие с солями: 2HCL + CaCO3 → H2O + CO2↑ + CaCL2
Специфические свойства HCL: 1) Взаимодействие с нитратом серебра (нитрат серебра является реактивом на соляную кислоту и ее соли); выпадет осадок белого цвета, который не растворяется в воде, ни в кислотах: HCL + AgNO3 → AgCL↓ + HNO3 2) Взаимодействие с окислителями (MnO2, KMnO, KCLO3 и др.): 6HCL + KCLO3 → KCL +3H2O + 3CL2↑
 Применение. Огромное количество соляной кислоты расходуется для удаления оксидов железа перед покрытием изделий из этого металла другими металлами (оловом, хромом, никелем). Для того чтобы соляная кислота реагировала только с оксидами, но не с металлом, к ней добавляют особые вещества, которые называются ингибиторами. Ингибиторы – вещества замедляющие реакции.
Применение. Огромное количество соляной кислоты расходуется для удаления оксидов железа перед покрытием изделий из этого металла другими металлами (оловом, хромом, никелем). Для того чтобы соляная кислота реагировала только с оксидами, но не с металлом, к ней добавляют особые вещества, которые называются ингибиторами. Ингибиторы – вещества замедляющие реакции.
Соляная кислота применяется для получения различных хлоридов. Ее используют для получения хлора. Очень часто, раствор соляной кислоты прописывают больным с пониженной кислотностью желудочного сока. Соляная кислота находится у каждого в организме, она входит в состав желудочного сока, который необходим для пищеварения.
В пищевой промышленности соляная кислота применяется только в виде раствора. Она используется для регулирования кислотности при производстве лимонной кислоты, желатина или фруктозы (Е 507).
Не стоит забывать, что соляная кислота опасна для кожи. Еще большую опасность она представляет для глаз. Воздействуя на человека, она может вызвать разрушение зубов, раздражение слизистых оболочек, удушье.
Помимо этого, соляная кислота активно применяется в гальванопластике и гидрометаллургии (удаление накипи, ржавчины, обработка кожи, химреактивы, в качестве растворителя породы при добыче нефти, при производстве каучуков, глутамината натрия, соды, Сl2). Соляная кислота используется для регенерации Сl2, в органическом синтезе (для получения винилхлорида, алкилхлоридов и т.д.) Она может использоваться в качестве катализатора при получении дифенилолпропана, алкилирование бензола.
© blog.tutoronline.ru,
при полном или частичном копировании материала ссылка на первоисточник обязательна.
Остались вопросы?
Задайте свой вопрос и получите ответ от профессионального преподавателя.
Источник
Характеристики и физические свойства соляной кислоты
Сильная кислота: pKa = -7,1. Концентрированная соляная кислота содержит около 37% HCl.
Основные физические свойства соляной кислоты приведены в таблице:
Температура плавления, oС | -30 |
Температура кипения, oС | 48 |
Энтальпия образования, кДж/моль | -605,22 |
Плотность, г/см3 | 1,19 |
Удельная теплоемкость, кДж/(кг×К) | 2,46 |
Вязкость, МПа×с | 1,99 |
Получение соляной кислоты
Соляная кислота получается растворением в воде хлороводорода. В настоящее время основным способом промышленного получения хлороводорода является синтез его из водорода и хлора:
H2 + Cl2 = 2HCl + 183 кДж.
Этот процесс осуществляют в специальных установках, в которых смесь водорода и хлора непрерывно образуется и тут же сгорает ровным пламенем. Тем самым достигается спокойное (без взрыва) протекание реакции. Исходным сырьем для получения хлороводорода служат хлор и водород, образующиеся при электролизе раствора хлорида натрия.
Большие количества соляной кислоты получают также в качестве побочного продукта хлорирования органических соединений согласно уравнению реакции, представленному ниже:
R-H + Cl2 = R-Cl + HCl,
где R – углеводородный радикал.
Химические свойства соляной кислоты
Соляная кислота – сильный электролит. Для нее характерны следующие химические свойства, общие для всех кислот:
— способность взаимодействовать с основаниями с образованием солей:
HCldilute + NaOHdilute = NaCl + H2O;
HCldilute + NH3×H2O = NH4Cl + H2O;
— способность взаимодействовать с некоторыми металлами с выделением водорода (разбавленный раствор):
2HCldilute + Fe = FeCl2 + H2↑;
2HCldilute + Zn = ZnCl2 + H2↑;
— способность вступать в реакции взаимодействия с основными и амфотерными оксидами с образованием солей и воды:
4HClconc + MnO2 = MnCl2 + 2H2O + Cl2↑;
4HClconc + PbO2 = PbCl2↓ + Cl2↑ + 2H2O;
— способность взаимодействовать с солями более слабых кислот:
2HCldilute + CaCO3 = CaCl2 + CO2↑ + H2O;
— способность изменять цвета индикаторов, в частности, вызывать красную окраску лакмуса;
— кислый вкус.
При диссоциации соляной кислоты образуются ионы водорода:
HCl↔H+ + Cl—.
Нагревание смеси растворов соляной и азотной кислот до температуры 100-150oС приводит к образованию очень сильного окислителя — соединения, которое называют «царская водка»:
6HClconc + 2HNO3 conc = 2NO↑ + 3Cl2↑ + 4H2O.
Соляная кислота в окислительно-восстановительных реакциях может выступать и как восстановитель (за счет хлорид-аниона Cl—) и как окислитель (за счет катиона водорода H+). Уравнения ОВР с участием соляной кислоты приведены ниже:
16HClconc + 2KMnO4 = 2MnCl2 + 5Cl2↑ + 8H2O + 2KCl;
14 HClconc + K2Cr2O7 = 2CrCl3 + 3Cl2↑ + 7H2O + 2KCl (t = 60 – 80oC);
4 HClconc + Ca(ClO)2 = 2Cl2↑ + CaCl2 + 2H2O;
6 HClconc + KClO3 = 3Cl2↑ + KCl + 3H2O.
Применение соляной кислоты
Соляная кислота – одна из важнейших кислот в химической практике. Ежегодное мировое производство соляной кислоты исчисляется миллионами тонн. Широкое применение находят также многие её соли.
Соляная кислота применяется в таких областях народного хозяйства как гидрометаллургия и гальванопластика, для травления, декапирования и лужения поверхности металлов; пищевом производстве, как регулятор кислотности (добавка Е507); в медицине, в качестве лекарства (смесь с ферментом пепсином) при недостаточной кислотности желудка.
Примеры решения задач
Источник
- Описание вещества
- Свойства
- Как получают
- Хранение и транспортировка
- Применение
Описание вещества
 Соляная кислота представляет из себя водный раствор хлористого водорода. Химическая формула данного вещества – HCl. В воде масса хлороводорода при наибольшей концентрации не может превышать 38%. При комнатной температуре хлороводород находится в газообразном состоянии. Для перехода его в жидкое состояние, он должен быть охлажден до минус 84 градуса по шкале Цельсия, в твердое – до минус 112 градусов. Плотность концентрированной кислоты при комнатной температуре составляет 1,19 г/см3. Данная жидкость входит в состав желудочного сока, который обеспечивает переваривание пищи. В этом состоянии ее концентрация не превышает 0,3%.
Соляная кислота представляет из себя водный раствор хлористого водорода. Химическая формула данного вещества – HCl. В воде масса хлороводорода при наибольшей концентрации не может превышать 38%. При комнатной температуре хлороводород находится в газообразном состоянии. Для перехода его в жидкое состояние, он должен быть охлажден до минус 84 градуса по шкале Цельсия, в твердое – до минус 112 градусов. Плотность концентрированной кислоты при комнатной температуре составляет 1,19 г/см3. Данная жидкость входит в состав желудочного сока, который обеспечивает переваривание пищи. В этом состоянии ее концентрация не превышает 0,3%.
Свойства соляной кислоты
Раствор хлористого водорода химически вреден, класс его опасности – второй.
Соляная жидкость – это сильная одноосновная кислота, которая может вступать в реакцию с множеством металлов, их солями, оксидами и гидрооксидами, она может взаимодействовать с нитратом серебра, аммиаком, гипохлоритом кальция и сильными окислителями:
Физические свойства и влияние на организм
При высоких концентрациях это едкое вещество, которое может вызвать ожоги не только слизистых оболочек, но и кожных покровов. Нейтрализовать его можно раствором пищевой соды. При открытии емкостей с концентрированным соляным раствором, его пары, соприкасаясь с находящейся в воздухе влагой, образовывают конденсат ядовитых паров в виде мельчайших капелек (аэрозоля), который раздражает дыхательные пути и глаза.
Концентрированное вещество имеет характерный резкий запах. Технические сорта раствора хлористого водорода делят на:
рыжий неочищенный, его цвет в основном обуславливается примесями хлорного железа;
очищенный, бесцветная жидкость, в которой концентрация HCl составляет порядка 25%;
дымящий, концентрированный, жидкость с концентрацией HCl в 35-38%.
Химические свойства

Как получают
Процесс производства соляной жидкости состоит из этапов получение хлорводорода и абсорбация (поглощение) его водой.
Существует три промышленных способа получения хлористого водорода:
синтетический
сульфатный
из побочных газов (абгазов) ряда технологических процессов. Последний способ является самым распространенным. Побочный HCl обычно образуется при дегихлорировании и хлорировании органических соединений, изготовлении калийных удобрений, пиролизе хлоридов металлов или органических отходов, содержащих хлор.
Хранение и транспортировка

Хранят и транспортируют соляную техническую кислоту в специализированных покрытых полимерами цистернах и контейнерах, бочках из полиэтилена, стеклянных бутылях, упаковываемых в ящики. Люки контейнеров и цистерн, пробки бочек и бутылей должны обеспечивать герметичность емкости. Кислотный раствор не должен контактировать с металлами, находящимися в линейке напряжения левее водорода, так как это может стать причиной возникновения взрывоопасных смесей.
Применение
в металлургии для извлечения руд, удаления ржавчины, окалин, грязи и окислов, паянии и лужении;
при изготовлении синтетических каучуков и смол;
в гальванопластике;
в качестве регулятора кислотности в пищевой промышленности;
для получения хлоридов металлов;
для получения хлора;
в медицине для лечения недостаточной кислотности желудочного сока;
в качестве чистящего и дезинфицирующего средства.
В нашей следующей статье мы подробно поговорить о классификации, свойствах и предназначении всасывающих рукавов.
← Назад к списку новостей
Источник
442761, Пензенская обл., Бессоновский р-н, с. Чемодановка, ул. Комсомольская дом 11 А
Режим работы:
ПН-ПТ: с 8-00 до 17-00
Соляная кислота, хлористо-водородная кислота, HCl, сильная одноосновная кислота, раствор хлористого водорода в воде. Соляная кислота — бесцветная жидкость с острым запахом хлористого водорода. Техническая кислота имеет желтовато-зелёный цвет из-за примесей хлора и солей железа. Максимальная концентрация соляной кислоты. около 36%; такой раствор имеет плотность 1,18 г/см3, на воздухе он “дымит”, т.к. выделяющийся HCl образует с водяным паром мельчайшие капельки.
Соляная кислота была известна алхимикам в конце 16 в., которые получали её нагреванием поваренной соли с глиной или с железным купоросом. Под названием “соляный спирт” её в середине 17 в. описал И. Р. Глаубер, приготовивший соляную кислоту взаимодействием NaCI с H2SO4. Метод Глаубера применяют и в настоящее время.
Соляная кислота — одна из самых сильных кислот. Она растворяет (с выделением Н2 и образованием солей — хлоридов) все металлы, стоящие в ряду напряжений до водорода. Хлориды образуются и при взаимодействии соляной кислоты с окислами и гидроокисями металлов. С сильными окислителями кислота соляная ведёт себя как восстановитель, например: MnO2 + 4HCl = MnCl2 + Cl2 + 2H2O.
Производство соляной кислоты в промышленности включает две стадии: получение HCl и его абсорбцию водой. Основной способ получения HCl — синтез из Cl2 и H2. Большие количества HCl образуются в качестве побочного продукта при хлорировании органических соединений: RH + Cl2= RCI + HCl, где R — органический радикал.
Выпускаемая техническая соляная кислота имеет крепость не менее 31% HCl (синтетическая) и 27,5% HCl (из NaCI). Торговую кислоту называют разбавленной, если она содержит, например, 12,2% HCl; при содержании 24% и больше HCl её называют концентрированной. В лабораторной практике 2н. HCl (7%-ную, плотность 1,035) обычно называют разбавленной соляной кислотой.Кислота соляная
Соляная кислота — важнейший продукт химической промышленности. Она идёт на получение хлоридов различных металлов и синтез хлор-содержащих органических продуктов. Соляная кислота применяют для травления металлов, для очистки различных сосудов, обсадных труб буровых скважин от карбонатов, окислов и др. осадков и загрязнений. В металлургии ею обрабатывают руды, в кожевенной промышленности — кожу перед дублением. Соляная кислота — важный реактив в лабораторной практике. Транспортируют соляную кислоту в стеклянных бутылях или гуммированных (покрытых слоем резины) металлических сосудах.
Газообразный HCl токсичен. Длительная работа в атмосфере HCl вызывает катары дыхательных путей, разрушение зубов, изъязвление слизистой оболочки носа, желудочно-кишечные расстройства. Допустимое содержание HCl в воздухе рабочих помещений не более 0,005 мг/л. Защита: противогаз, очки, резиновые перчатки, обувь, фартук.
Соляная кислота содержится в желудочном соке (около 0,3%); способствует пищеварению и убивает болезнетворные бактерии.
В медицинской практике разведённую соляную кислоту применяют в каплях и микстурах в комбинации с пепсином при заболеваниях, сопровождающихся недостаточной кислотностью желудочного сока (например, гастрите), а также гипохромной анемии (совместно с препаратами железа для улучшения их всасывания).
Товар в наличии на складе

Наша компания обеспечит вас продукцией наилучшего качества. У нас вы сможете купить в Пензе химические реактивы и промышленную химию, а также другие химические материалы и химическую продукцию. Мы организуем оперативную доставку и ритмичные поставки по удобному для вас графику. Для постоянных клиентов у нас действует система скидок.
Физические свойства соляной кислоты
Физические свойства растворов соляной кислоты разных концентраций приведены в таблице:
| Конц. (вес) c : кг HCl/кг | Конц. (г/л) c : кг HCl/м³ | Плотность ρ : кг/л | Молярность M | pH | Вязкость η : мПа·с | Удельная теплоемкость s : кДж/(кг·К) | Давление пара P HCl : Па | Т кипения т.кип. | Т плавления т.пл. |
| 10 % | 104,80 | 1,048 | 2,87 M | −0,5 | 1,16 | 3,47 | 0,527 | 103 °C | −18 °C |
| 20 % | 219,60 | 1,098 | 6,02 M | −0,8 | 1,37 | 2,99 | 27,3 | 108 °C | −59 °C |
| 30 % | 344,70 | 1,149 | 9,45 M | −1,0 | 1,70 | 2,60 | 1,410 | 90 °C | −52 °C |
| 32 % | 370,88 | 1,159 | 10,17 M | −1,0 | 1,80 | 2,55 | 3,130 | 84 °C | −43 °C |
| 34 % | 397,46 | 1,169 | 10,90 M | −1,0 | 1,90 | 2,50 | 6,733 | 71 °C | −36 °C |
| 36 % | 424,44 | 1,179 | 11,64 M | −1,1 | 1,99 | 2,46 | 14,100 | 61 °C | −30 °C |
| 38 % | 451,82 | 1,189 | 12,39 M | −1,1 | 2,10 | 2,43 | 28,000 | 48 °C | −26 °C |
Высокое качество
Основной ассортимент химического сырья и химреактивов получается нами напрямую с заводов-изготовителей а также европейских фирм-производителей химических реактивов и химической продукции. Наш девиз – УДОБНО, КАЧЕСТВЕННО, БЫСТРО!
Выгодные цены
Для постоянных партнеров фирмы действует гибкая система ценообразования и предоставляется товарный кредит.
Доставка по России
Ускоренная доставка продукции автотранспортом, ж/д вагонами, транспортными компаниями. Благодаря слаженной работе со службами доставки, в любой момент мы предоставим Вам информацию о местонахождении груза.
Быстрая отгрузка
Всю продукцию Вы можете получить на условиях самовывоза со склада в городе Пенза. Четкая работа нашего склада позволяет осуществить отгрузку всего за 30 минут.
442761, Пензенская обл., Бессоновский р-н, с. Чемодановка, ул. Комсомольская дом 11 А
Информация, опубликованная на Сайте, носит общий характер и служит для ознакомительных целей, не является публичной офертой.
©2007-2020 ХПК-ГРУПП. All Rights Reserved
Режим работы:
ПН-ПТ: с 8-00 до 17-00
Источник
Химическое название
Хлороводородная кислота
Химические свойства
Хлороводородная кислота, хлористый водород или хлористоводородная кислота – раствор НСl в воде. Согласно Википедии, вещество относят у группе неорганических сильных одноосновных к-т. Полное название соединения на латинском: Hydrochloricum acid.
Формула Соляной Кислоты в химии: HCl. В молекуле атомы водорода соединяются с атомами галогена – Cl. Если рассмотреть электронную конфигурацию этих молекул, то можно отметить, что в образовании молекулярных орбиталей соединения принимают участие 1s-орбитали водорода и обе 3s и 3p-орбитали атома Cl. В химической формуле Соляной Кислоты 1s-, 3s- и 3р-атомные орбитали перекрываются и образуют 1 , 2 , 3 -орбитали. При этом 3s-орбиталь не носит связывающий характер. Наблюдается смещение электронной плотности к атому Cl и снижается полярность молекулы, но увеличивается энергия связи молекулярных орбиталей (если рассматривать ее в ряду с другими галогеноводородами).
Физические свойства хлористого водорода. Это прозрачная бесцветная жидкость, обладающая способностью дымиться при соприкосновении с воздухом. Молярная масса химического соединения = 36,6 грамма на моль. При стандартных условиях, при температуре воздуха 20 градусов Цельсия, максимальная концентрация вещества составляет 38% по массе. Плотность концентрированной хлороводородной к-ты в такого рода растворе составляет 1,19 г/см³. В целом же, физические свойства и такие характеристики, как плотность, молярность, вязкость, теплоемкость, температура кипения и pН , сильно зависят от концентрации раствора. Эти величины подробнее рассматриваются в таблице плотностей. Например, плотность Соляной Кислоты 10% = 1,048 кг на литр. При затвердевании вещество образует кристаллогидраты разных составов.
Химические свойства Соляной Кислоты. С чем реагирует Соляная Кислота? Вещество вступает во взаимодействие с металлами, которые стоят в ряду электрохимических потенциалов перед водородом (железо, магний, цинк и другие). При этом образуются соли и выделяется газообразный H. С Соляной Кислотой не реагирует свинец, медь, золото, серебро и другие металлы правее водорода. Вещество вступает в реакцию с оксидами металлов, при этом образуя воду и растворимую соль. Гидроксид натрия под действием к-ты образует хлорид натрия и воду. Реакция нейтрализации характерна для данного соединения.
Разбавленная Соляная Кислота реагирует с солями металлов, которые образованы более слабыми к-ами. Например, пропионовая кислота слабее, чем соляная. Вещество не взаимодействует с более сильными кислотами. Карбонат кальция и карбонат натрия будут образовывать после реакции с HCl хлорид, угарный газ и воду.
Для химического соединения характерны реакции с сильными окислителями, с диоксидом марганца, перманганатом калия: 2KMnO4 + 16HCl = 5Cl2 + 2MnCl2 + 2KCl + 8H2O. Вещество реагирует с аммиаком, при этом образуется густой белый дым, который состоит из очень мелких кристаллов хлорида аммония. Минерал пиролюзит с Соляной Кислотой также вступает в реакцию, так как содержит диоксид марганца: MnO2+4HCl=Cl2+MnO2+2H2O (реакция окисления).
Существует качественная реакция на хлороводородную кислоту и ее соли. При взаимодействии вещества с нитратом серебра выпадает белый осадок хлорида серебра и образуется азотная к-та. Уравнение реакции взаимодействия метиламина с хлористым водородом выглядит следующим образом: HCl + CH3NH2 = (CH3NH3)Cl.
Вещество реагирует со слабым основанием анилином. После растворения анилина в воде к смеси прибавляют Соляную Кислоту. В результате основание растворяется и образует солянокислый анилин (хлорид фениламмония): (С6Н5NH3)Cl. Реакция взаимодействия карбида алюминия с хлористоводородной к-ой: Al4C3+12HCL=3CH4+4AlCl3. Уравнение реакции карбоната калия с к-той выглядит следующим образом: K2CO3 + 2HCl = 2KCl + H2O + CO2.
Получение соляной кислоты
Чтобы получить синтетическую Соляную Кислоту сжигают водород в хлоре, а затем полученный газообразный хлороводород растворяется в воде. Также распространено производство реактива из абгазов, которые образуются в виде побочных продуктов при хлорировании углеводородов (абгазная Соляная Кислота). При производстве данного химического соединения применяют ГОСТ 3118 77 – на реактивы и ГОСТ 857 95 – для технической синтетической хлористоводородной кислоты.
В лабораторных условиях можно применять давний способ, при котором поваренная соль подвергается действию концентрированной серной к-ты. Также средство можно получить с помощью реакции гидролиза хлорида алюминия или магния. Во время реакции могут образоваться оксихлориды переменного состава. Для определения концентрации вещества применяют стандарт титры, которые выпускаются в запаянных ампулах, чтобы в последствии можно было получить стандартный раствор известной концентрации и использовать его для определения качества другого титранта.
У вещества имеется достаточно широкая область применения:
- его используют в гидрометаллургии, при декапировании и травлении;
- при очистке металлов при лужении и пайке;
- в качестве реактива для получения хлорида марганца, цинка, железа и других металлов;
- при изготовлении смесей с ПАВ-ами для очистки металлических и керамических изделий от инфекции и грязи (применяется Кислота Соляная ингибированная);
- в качестве регулятора кислотности E507 в пищевой промышленности, в составе содовой воды;
- в медицине при недостаточной кислотности желудочного сока.
Данное химическое соединение имеет высокий класс опасности – 2 (по ГОСТу 12Л.005). При работе с кислотой требуется спец. защита кожи и глаз. Достаточно едкое вещество при попадании на кожу или в дыхательные пути вызывает химические ожоги. Для ее нейтрализации применяют растворы щелочи, чаще всего – питьевую соду. Пары хлороводорода образуют с молекулами воды в воздухе едкий туман, который раздражает дыхательные пути и глаза. Если вещество вступает в реакцию с хлорной известью, перманганатом калия и прочими окислителями, то образуется токсичный газ — хлор. На территории РФ ограничен оборот Соляной Кислоты с концентрацией более 15%.
Фармакологическое действие
Повышает кислотность желудочного сока.
Фармакодинамика и фармакокинетика
Что такое кислотность желудочного сока? Это характеристика концентрации Соляной Кислоты в желудке. Кислотность выражается в рН. В норме в составе желудочного сока должна вырабатываться кислота и принимать активное участие в процессах пищеварения. Формула хлороводородной кислоты: HCl. Ее продуцируют париетальные клетки, расположенные в фундальных железах, с участием Н+/К+-АТФазы. Эти клетки выстилают дно и тело желудка. Кислотность желудочного сока сама по себе изменчива и зависит от числа париетальых клеток и интенсивности процессов нейтрализации вещества щелочными компонентами желудочного сока. Концентрация продуцируемой к-ты стабильна и равняется 160 ммоль/л. У здорового человека в норме должно вырабатываться не более 7 и не менее 5 ммоль вещества в час.
При недостаточной или избыточной выработке Соляной Кислоты возникают заболевания пищеварительного тракта, ухудшается способность усваивать некоторые витамины и микроэлементы, например, железо. Средство стимулирует выделение желудочного сока, снижает рН. Активирует пепсиноген, переводит его в активный фермент пепсин. Вещество благоприятно воздействует на кислотный рефлекс желудка, замедляет переход не до конца переваренной пищи в кишечник. Замедляются процессы брожения содержимого пищеварительного тракта, исчезает боль, изжога и отрыжка, лучше усваивается железо.
После приема внутрь средство частично метаболизируется слюной и желудочной слизью, содержимым 12-перстной кишки. Несвязанное вещество проникает в 12-перстную кишку, где полностью нейтрализуется ее щелочным содержимым.
Показания к применению
Вещество входит в состав синтетических моющих средств, концентрата для полоскания ротовой полости ухода за контактными линзами. Разбавленная Соляная Кислота назначается при заболеваниях желудка, сопровождающихся пониженной кислотностью, при гипохромной анемии в сочетании с препаратами железа.
Противопоказания
Лекарство нельзя применять при аллергии на синтетическое вещество, при болезнях пищеварительного тракта, ассоциированных с повышенной кислотностью, при остром гастрите.
Побочные действия
Концентрированная Соляная Кислота при попадании на кожу, в глаза и дыхательные пути может вызывать сильные ожоги. В составе различных лек. препаратов используют разбавленное вещество, при длительном применении больших дозировок может возникнуть ацидоз, ухудшение состояния эмали зубов.
Инструкция по применению (Способ и дозировка)
Хлороводородную кислоту применяют в соответствии с инструкцией.
Внутрь лекарство назначают, предварительно растворив в воде. Обычно используют 10-15 капель препарата на пол стакана жидкости. Лекарство принимают во время еды, 2-4 раза в день. Максимальная разовая дозировка составляет 2 мл (около 40 капель). Суточная доза – 6 мл (120 капель).
Передозировка
Случаи передозировки не описаны. При бесконтрольном приеме вещества внутрь в больших количествах возникают язвы и эрозии в пищеварительном тракте. Следует обратиться за помощью к врачу.
Взаимодействие
Вещество часто используют в комбинации с пепсином и прочими лек. препаратами. Химическое соединение в пищеварительном тракте вступает во взаимодействие с основаниями и некоторыми веществами (см. химические свойства).
Особые указания
При лечении препаратами Соляной Кислоты необходимо четко придерживаться рекомендаций в инструкции.
Препараты, в которых содержится (Аналоги)
Совпадения по коду АТХ 4-го уровня:
Для промышленных целей используют Кислоту Соляную ингибированную (22-25%). В медицинских целях применяют раствор: Хлористоводородная кислота разведенная. Также вещество содержится в концентрате для полоскания ротовой полости Паронтал, в растворе для ухода за мягкими контактными линзами Биотру.
Отзывы
В Интернете часто можно встретить вопросы, как сделать Соляную Кислоту в домашних условиях и где взять Соляную Кислоту? Вещество часто приобретают для хим. лабораторий и промышленных целей. Отзывов о применении средства внутрь мало.
- “… С возрастом стала беспокоить проблема с желудком и проблемы с пищеварением. Поставили диагноз – гастрит и атрофия слизистой желудка. Врачи назначили пить ферментные лекарства с Соляной Кислотой. Сейчас я прохожу курс лечения, есть первые улучшения в состоянии”;
- “… Мне назначали это лекарство при пониженной кислотности. Но я решила, что буду лечиться более щадящими методами. Пью настой из перечной мяты, мед, растворенный в воде”.
Цена Соляной кислоты, где купить
Где купить Соляную Кислоту ингибированную? Где можно купить Соляную Кислоту в Москве? Купить в розницу данное вещество для технических целей может быть достаточно сложно. На рынке предлагают приобрести средство по приблизительной цене за литр – 20 рублей, но в больших объемах. Указать стоимость препарата для приема внутрь на данный момент невозможно.
Источник
