Какие свойства имеет оксид кремния

| Диоксид кремния | |
|---|---|
 | |
| | |
| Систематическое наименование | оксид кремния (IV) |
| Традиционные названия | кремнезём |
| Хим. формула | SiO2 |
| Рац. формула | SiO2 |
| Температура | |
| • плавления | 1600 °C |
| • кипения | 2950 °C |
| Давление пара | 0 ± 1 мм рт.ст. |
| ГОСТ | ГОСТ 9428-73 |
| Рег. номер CAS | 7631-86-9 |
| PubChem | 24261 |
| Рег. номер EINECS | 231-545-4 |
| SMILES | O=[Si]=O |
| InChI | 1S/O2Si/c1-3-2 VYPSYNLAJGMNEJ-UHFFFAOYSA-N |
| Кодекс Алиментариус | E551 |
| RTECS | VV7565000 |
| ChEBI | 30563 |
| ChemSpider | 22683 |
| Токсичность | Пыль SiO2 чрезвычайно токсична и канцерогенна при вдыхании, поражает лёгкие, приводит к силикозу |
| Пиктограммы ECB |   |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Диоксид кремния (кремнезём, SiO2; лат. silica) — оксид кремния (IV). Бесцветные кристаллы с температурой плавления +1713…+1728 °C, обладающие высокой твёрдостью и прочностью.
Диоксид кремния — главный компонент почти всех земных горных пород, в частности, кизельгура. Из кремнезёма и силикатов состоит 87 % массы литосферы. В крови и плазме человека концентрация кремнезёма составляет 0,001 % по массе.

Свойства
- Относится к группе кислотных оксидов.
- При нагревании взаимодействует с основными оксидами и щелочами.
- Молярная масса: 60,084 г/моль
- Реагирует с плавиковой кислотой.
- SiO2 относится к группе стеклообразующих оксидов, то есть склонен к образованию переохлаждённого расплава — стекла.
- Диэлектрик (электрический ток не проводит, если не имеет примесей и не нагревается).
Полиморфизм
Диоксид кремния имеет несколько полиморфных модификаций.
Самая распространённая из них на поверхности земли — α-кварц — кристаллизуется в тригональной сингонии. При нормальных условиях диоксид кремния чаще всего находится в полиморфной модификации α-кварца, которая при температуре выше +573 °C обратимо переходит в β-кварц. При дальнейшем повышении температуры кварц переходит в тридимит и кристобалит. Эти полиморфные модификации устойчивы при высоких температурах и низких давлениях.
В природе также встречаются формы — опал, халцедон, кварцин, лютецит, аутигенный кварц, которые относятся к группе кремнезёма. Опал (SiO2·nH2O) в шлифе бесцветен, изотропен, имеет отрицательный рельеф, отлагается в морских водоёмах, входит в состав многих кремнистых пород. Халцедон, кварцин, лютецит — SiO2 — представляют собой скрытокристаллические разновидности кварца. Образуют волокнистые агрегаты, розетки, сферолиты, бесцветные, голубоватые, желтоватые. Отличаются между собой некоторыми свойствами — у халцедона и кварцина — прямое погасание, у лютецита — косое, у халцедона — отрицательное удлинение.
При высоких температуре и давлении диоксид кремния сначала превращается в коэсит (который в 1953 году был синтезирован американским химиком Лорингом Коэсом), а затем — в стишовит (который в 1961 году был синтезирован С. М. Стишовым, а в 1962 году был обнаружен в кратере Бэрринджера (кратере Аризонского метеорита). Согласно некоторым исследованиям, стишовит слагает значительную часть мантии, так что вопрос о том, какая разновидность SiO2 наиболее распространена на Земле, пока не имеет однозначного ответа.
Также имеет аморфную модификацию — кварцевое стекло.
Химические свойства
Диоксид кремния SiO2 — кислотный оксид, не реагирующий с водой.
Химически стоек к действию кислот, но реагирует с газообразным фтороводородом:
SiO2 + 4HF → SiF4 + 2H2O
и плавиковой кислотой:
SiO2 + 6HF → H2[SiF6] + 2H2O
Эти две реакции широко используют для плавления стекла.
При сплавлении SiO2 с щелочами и основными оксидами, а также с карбонатами активных металлов образуются силикаты — соли не имеющих постоянного состава очень слабых, нерастворимых в воде кремниевых кислот общей формулы xH2O·ySiO2 (довольно часто в литературе упоминаются не кремниевые кислоты, а кремниевая кислота, хотя фактически речь при этом идёт об одном и том же веществе).
Например, может быть получен ортосиликат натрия:
SiO2 + 4NaOH → Na4SiO4 + 2H2O
метасиликат кальция:
SiO2 + CaO → CaSiO3
или смешанный силикат кальция и натрия:
Na2CO3 + CaCO3 + 6SiO2 → Na2CaSi6O14 + 2CO2
Из силиката Na2CaSi6O14 (Na2O·CaO·6SiO2) изготовляют оконное стекло.
Большинство силикатов не имеет постоянного состава. Из всех силикатов растворимы в воде только силикаты натрия и калия. Растворы этих силикатов в воде называют жидким стеклом. Из-за гидролиза эти растворы характеризуются сильно щелочной средой. Для гидролизованных силикатов характерно образование не истинных, а коллоидных растворов. При подкислении растворов силикатов натрия или калия выпадает студенистый белый осадок гидратированных кремниевых кислот.
Главным структурным элементом как твёрдого диоксида кремния, так и всех силикатов, выступает группа [SiO4/2], в которой атом кремния Si окружен тетраэдром из четырёх атомов кислорода О. При этом каждый атом кислорода соединён с двумя атомами кремния. Фрагменты [SiO4/2] могут быть связаны между собой по-разному. Среди силикатов по характеру связи в них фрагментов [SiO4/2] выделяют островные, цепочечные, ленточные, слоистые, каркасные и другие.
Получение
Синтетический диоксид кремния получают нагреванием кремния до температуры +400…+500 °C в атмосфере кислорода, при этом кремний окисляется до диоксида SiO2. А также термическим оксидированием при больших температурах.
В лабораторных условиях синтетический диоксид кремния может быть получен действием кислот, даже слабой уксусной, на растворимые силикаты. Например:
Na2SiO3 + 2CH3COOH → 2CH3COONa + H2SiO3↓
кремниевая кислота сразу распадается на воду и SiO2, выпадающий в осадок.
Натуральный диоксид кремния в виде песка используется там, где не требуется высокая чистота материала.
Применение
Аморфный непористый диоксид кремния применяется в пищевой промышленности в качестве вспомогательного вещества E551, препятствующего слёживанию и комкованию, в парафармацевтике (зубные пасты), в фармацевтической промышленности в качестве вспомогательного вещества (внесён в большинство фармакопей), для стабилизации суспензий и линиментов, в качестве загустителя мазевых основ, наполнителя таблеток и суппозиториев. Он входит в состав композиции пломбировочных материалов, снижает гигроскопичность сухих экстрактов, замедляет выход БАВ из различных лекарственных форм; в качестве пищевых добавок и сорбента, а также матриц для создания лекарственных форм с заданными свойствами – так как нет кристаллической структуры (аморфен) – безопасен, а также в качестве пищевой добавки или лекарственного препарата в качестве энтеросорбента Полисорб МП с широким спектром применения с учётом высокой удельной поверхности сорбции (в интервале 300-400 м² ) на 1 г основного вещества.
Диоксид кремния применяют в производстве стекла, керамики, абразивов, бетонных изделий, для получения кремния, как наполнитель в производстве резин, при производстве кремнезёмистых огнеупоров, в хроматографии и другом.
Кристаллы кварца обладают пьезоэлектрическими свойствами и поэтому используются в радиотехнике, ультразвуковых установках, в зажигалках.
Искусственно полученные плёнки диоксида кремния используются в качестве изолятора при производстве микросхем и других электронных компонентов.
Также используется для производства волоконно-оптических кабелей. Используется чистый плавленый диоксид кремния с добавкой в него некоторых специальных ингредиентов.
Кремнезёмная нить также используется в нагревательных элементах электронных сигарет, так как хорошо впитывает жидкость и не разрушается под нагревом спирали.
Также диоксид кремния нашёл наиболее широкое применение в шинной промышленности, производстве РТИ и пластмасс, химической промышленности, машиностроении, а в ряде конкретных операций:
- как носитель катализаторов и химических средств защиты растений;
- в качестве сорбентов и фильтровальных порошков для регенерации нефтепродуктов;
- как высококачественный флюс в процессах цветной металлургии;
- как сырьё для производства экологически чистого стекла, стеклотары и хрусталя;
- как наполнитель в бумагу и картон для получения гигиенически чистых упаковочных материалов для пищевой промышленности;
- фильтрующие порошки для пива, масел, соков, матирующие добавки в лаки и краски;
- для получения карбида кремния в машиностроении – керамические двигатели, детали для авиастроительного комплекса;
- для получения кристаллического кремния в электронной и электротехнической промышленностях, керамические электроизоляторы, стекловолокна, волоконная оптика, супертонкое волокно;
- для синтеза искусственных цеолитов в нефтехимии — крекинг нефти и прочее.
Крупные прозрачные кристаллы кварца используются в качестве полудрагоценных камней; бесцветные кристаллы называют горным хрусталём, фиолетовые — аметистами, жёлтые — цитрином.
В микроэлектронике диоксид кремния является одним из основных материалов. Его применяют в качестве изолирующего слоя, а также в качестве защитного покрытия. Получают в виде тонких плёнок термическим окислением кремния, химическим осаждением из газовой фазы, магнетронным распылением.
Пористые кремнезёмы
Пористые кремнезёмы получают различными методами.
Силохром получают путём агрегирования аэросила, который, в свою очередь, получают сжиганием силана (SiH4). Силохром характеризуется высокой чистотой, низкой механической прочностью. Характерный размер удельной поверхности 60—120 м²/г. Применяется в качестве сорбента в хроматографии, наполнителя резин, катализе.
Силикагель получают путём высушивания геля кремниевой кислоты. В сравнении с силохромом обладает меньшей чистотой, однако может обладать чрезвычайно развитой поверхностью: обычно от 300 м²/г до 700 м²/г .
Кремниевый аэрогель приблизительно на 99,8 % состоит из воздуха и может иметь плотность до 1,9 кг/м³ (всего в 1,5 раза больше плотности воздуха).
Токсичность
Хотя и сам диоксид кремния считается нетоксичным, однако его пыль является токсичной и канцерогенной при вдыхании (как и пыль асбеста) . Вдыхание пыли приводит к бронхиту, воспалению лёгких (силикоз) и онкологическим заболеваниям.
Источник
Кремний – неметаллический элемент IVa группы периодической таблицы Д.И. Менделеева. Второй после кислород элемент по распространенности
в земной коре.
В чистом виде в природе практически отсутствует. Чаще всего встречается в виде кремнезема – SiO2 – песок, песчаник, кварц, глина.

Кремниевая (силиконовая) долина
Регион в штате Калифорния (США), отличающийся большой плотностью высоко технологичных компаний, связанных с производством
компьютеров и микропроцессоров.
Кремний является природным полупроводником, используется как основной материал для производства микросхем. Кремний ближе, чем
вы думаете: внутри гаджета, которым вы пользуетесь 😉

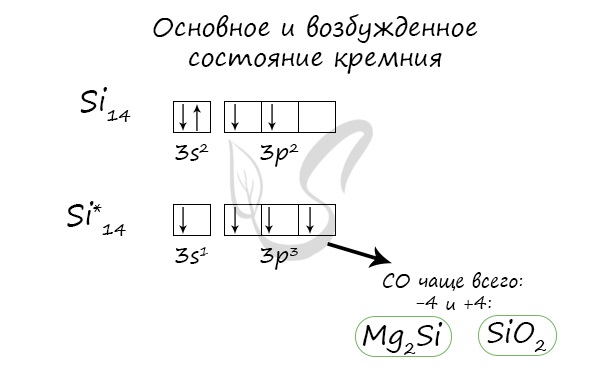
Основное и возбужденное состояние кремния
При возбуждении атома кремния электроны на s-подуровне распариваются и один из них переходит на p-подуровень.
Природные соединения
В природе кремний встречается в виде следующих соединений:
- SiO2 – кварц, кремнезем, гранит, песчаник, песок, глина
- SiO2 с примесью Fe3+ – цитрин
- SiO2 с примесью Fe2+ и Fe3+ – аметист

Получение
В промышленности кремний получают путем восстановления кремнезема в электрических печах, алюминотермией.
SiO2 + C → (t) Si + CO2↑
SiO2 + Al → (t) Si+ Al2O3
В лабораторных условиях мелкий белый песок прокаливают с магнием:
SiO2 + Mg → (t) MgO + Si
Химические свойства
- Реакции с неметаллами
- Реакции с металлами
- Реакция с щелочами
При обычных условиях без нагревания кремний реагирует только со фтором.
Si + F2 → SiF4
При нагревании кремний вступает в реакции с остальными галогенами (Cl, Br, I), углеродом, кислородом. При очень высоких температурах (1200 °C) кремний
с кислородом образует оксид кремния II – несолеобразующий оксид.
Si + Cl2 → (t) SiCl4
Si + C → (t) SiC
Si + O2 → (t) SiO2
Si + O2 → (t = 1200 °C) SiO

В подобных реакциях кремния проявляет свои окислительные способности.
Ca + Si → Ca2Si (силицид кальция)
С целью травления (удаления поверхностного слоя материала) кремниевые изделия можно погружать в раствор щелочи.
KOH + Si → K2SiO3 + H2↑
Оксид кремния IV – SiO2
Оксид кремния IV имеет атомное строение, обладает высокой прочностью и твердостью. Плавится при температуре
+1730 °C градусов.
Получение
В промышленности оксид кремния IV получают нагреванием кремния в атмосфере кислорода.
Si + O2 → SiO2
В лабораторных условиях проводят реакция силиката натрия с уксусной кислотой. Кремниевая кислота сразу же распадается на SiO2,
который выпадает в осадок, и воду.
Na2SiO3 + CH3COOH → CH3COONa + H2SiO3↓
H2SiO3 → SiO2 + H2O

Химические свойства
- Реакции с кислотами
- Реакции с основными оксидами и щелочами
- С карбонатами
Химически SiO2 устойчив к действию кислот, однако вступает в реакцию с газообразным фтороводородом (газом) и плавиковой кислотой (жидкостью).
SiO2 + HF → SiF4 + H2O
SiO2 является кислотным оксидом, соответствует кремниевой кислоте. Вступая в реакции с основными оксидами и щелочами, образует соли
данной кислоты – силикаты.
MgO + SiO2 → MgSiO3
NaOH + SiO2 → Na2SiO3 + H2O

Так как чаще всего кислотные оксиды с солями не реагируют, тем более необычной кажется реакция оксида кремния IV с карбонатами.
K2CO3 + SiO2 → K2SiO3 + CO2↑
Кремниевая кислота
Слабая, малорастворимая в воде кислота. Ее соли носят название – силикаты.
Получение
Поскольку кремниевая кислота малорастворима, то банальной реакцией SiO2 с водой ее не получить. Эту задачу решают в две стадии
через ее соли – силикаты.
LiOH + SiO2 → Li2SiO3 + H2O
Li2SiO3 + HCl → LiCl + H2SiO3↓
Химические свойства
Кремниевая кислота слабая, нестойкая, легко распадается на воду и оксид кремния IV.
H2SiO3 → H2O + SiO2

© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
Силан $SiH_4$
По аналогии с углеводородами известны силаны состава $Si_nH_{2n+2}$. Все они очень ядовитые вещества с неприятным запахом. Первые два – $SiH_4$ и $Si_2H_6$ – газы, $Si_3H_8$ и $Si_4H_{10}$ – жидкости, остальные – твердые вещества.

Наиболее хорошо изучено простейшее соединение – $SiH_4$ силан, который представляет из себя бесцветный ядовитый газ.
Строение силана схоже со строением метана: это тетраэдрическая молекула. Все связи – ковалентные, образованы по обменному механизму за счет обобществления неспаренных электронов атома кремния и атомов водорода.
Образуются силан при действии кислот на силициды металлов IA и IIA групп, например, соляной кислоты на силицид магния:
$Mg_2Si + 4HCl xrightarrow[]{t, ^circ C}2MgCl_2 + SiH4uparrow$
Химические свойства силана
Силаны химически менее устойчивы, чем углеводороды.
Силан горит с образованием высшего оксида:
$ SiH_4 + 2O_2 xrightarrow[]{t, ^circ C} SiO_2 + 2H_2O$
Под действием высоких температур силан разлагается на простые вещества:
$SiH4 xrightarrow[]{t, ^circ C}Si + 2H_2$
Силаны проявляют кислотные свойства и взаимодействуют со щелочами:
$SiH_4 + 2NaOH + H_2O = Na_2SiO_3 + 4H_2 uparrow$
В нейтральной и кислой среде силаны устойчивы.
Кроме того, силан является сильным восстановителем:
$SiH_4 + 2AgCl = SiH_3Cl + HCl + 2Ag$
Оксид кремния (II) $SiO$
или монооксид кремния. Пары монооксида SiO образуются при нагревании кремнезема с кремнием при 1300$^oC$ и конденсируются в черно-коричневый порошок, на воздухе медленно окисляющийся до $SiO_2$:
$2SiO + O_2 = 2SiO_2$
Это тугоплавкий темно-коричневый порошок. Типичный несолеобразующий оксид: не растворяется в кислотах, кроме плавиковой.
Легко растворяется в щелочах с выделением водорода:
$SiO + 4NaOH _{textrm{(конц.)}} = H_2 uparrow + Na_4SiO_4 + H_2O$
ОКСИД КРЕМНИЯ(IV) $SIO_2$
или диоксид кремния, кремнезем. Твердое, очень тугоплавкое, кристаллическое вещество, нерастворимое в воде и не вступающее с ней во взаимодействие.
Оксид кремния(IV) – высший оксид кремния, проявляет окислительные свойства. При температуре выше 1000 °С реагирует с активными металлами, при этом образуется кремний:
$SiO_2 + 2Mg = Si + 2MgO$
$3SiO_2+4Al=3Si+2Al_2O_3$
или при избытке восстановителя – силициды:
$SiO_2 + 4Mg = Mg_2Si + 2MgO$
Реагирует с водородом:
$SiO_2 + 2H_ 2= Si + 2H_2O$
Взаимодействует с углеродом с образованием карборунда (карбида кремния):
$SiO_2 + 3C = SiС + 2CO$
По химическим свойствам оксид кремния (IV) относится к кислотным оксидам.
С оксидом кремния (IV) непосредственно реагирует только плавиковая кислота:
$SiO_2 + 4HF = SiF_4 + 2H_2O$.
При сплавлении оксида кремния (IV) со щелочами, основными оксидами и карбонатами щелочных металлов образуются соли кремниевой кислоты — силикаты:
$SiO_2 + 2NaOH = Na_2SiOO_3 + H_20$
$SiO_2 + CaO = CaSiO_3$
$SiO_2 + K_2CO_3 = K_2SiO_3 + CO_2$
$SiO_2 +H_2O ne$
Эти реакции лежат в основе производства стекла. Диоксид кремния широко распространен в природе. Кристаллический оксид кремния – это кварц, горный хрусталь, халцедон, яшма, основа кварцевого песка. Очень твердое, прочное, тугоплавкое вещество. При обычном давлении и температуре существуют три кристаллические модификации $SiO_2$: кварц, тридимит и кристобалит. Для каждой модификации известны низкотемпературные $alpha$- и высокотемпературные $beta$-формы. Все они построены из тетраэдров $SiO_4$, соединенных с другими тетраэдрами всеми четырьмя атомами кислорода в трехмерные решетки.
Взаимное расположение тетраэдров в различных модификациях совершенно различно, но между собой $alpha$- и $beta$- формы отличаются незначительно, поэтому между ними превращения протекают при низких температурах, а взаимные переходы между различными модификациями требуют разрыва связей Si – O – Si, поэтому они протекают при высоких температурах и довольно медленно.
КРЕМНИЕВАЯ КИСЛОТА $H_2SIO_3$

твердое аморфное вещество, представляющее собой полимерную структуру, практически нерастворимо в воде, поэтому катионы водорода в воде практически не отщепляются.

В связи с этим такое общее свойство кислот, как действие на индикаторы, $H_2SiO_3$ не обнаруживает, она еще слабее угольной кислоты.
$H_2SiO_3$ — непрочная кислота и при нагревании постепенно разлагается:
$H_2SiO_3 xrightarrow[]{t ^circ C} SiO_2 + H_2O$
.
Силикаты – соли кремниевой кислоты $MSiO_3$
Соли кремниевой кислоты – силикаты $SiO_3^{2-}$. Обычно они нерастворимы в воде, исключения составляют силикаты натрия и калия, их называют «жидким стеклом».
Силикаты проявляют типичные свойства средних солей.
Взаимодействуют с кислотами с образованием нерастворимой кремниевой кислоты:
$Na2SiO_3+2HCl=2NaCl+H_2SiO_3$
Взаиодействуют с угольной кислотой (единственная кислота, которая слабее кремниевой):
$Na_2SiO_3+C0_2+H_20=Na2CO_3 + H_2SiO_3 downarrow$
Силикаты широко распространены в природе. Свойства силикатов различны в зависимости от их состава и строения, очень часто они имеют красивую окраску, некоторые из них используются в ювелирном деле (гранат, топаз, изумруд).
Стекло – тоже силикат. Состав обычного оконного стекла: $Na_2O cdot CaO cdot 6SiO_2$ Стекло получают при сплавлении в специальных печах смеси соды $Na_2CO_3$, известняка $CaCO_3$ и белого песка $SiO_2$:
$6SiO_2 + Na_2CO_3 + CaCO_3 = Na_2O cdot CaO cdot 6SiO_2 + 2CO_2$
Для получения специального стекла вводят различные добавки, так стекло содержащее ионы:
$Pb^{2+}$ – хрусталь;
$Cr^{3+}$ – имеет зеленую окраску,
$Fe^{3+}$ – коричневое бутылочное стекло,
$Co^{2+ }$– дает синий цвет,
$Mn^{2+}$ – красновато–лиловый.
Источник
