Какие свойства металлов отличают их от свойств неметаллов

В повседневной жизни человек взаимодействует с множеством веществ. Все элементы можно классифицировать по физическим и химическим качествам. В статье рассмотрим, чем отличаются металлы от неметаллов, их свойства и понятие.
Определение металла и его свойства
Каждый день мы имеем дело с металлами и это неспроста. Большинство элементов таблицы Менделеева являются ими. Все они имеют свои характеристики и свойства.
Как правило, металлы — это такие элементы, которые хорошо проводят тепло и электричество. Также металлы очень пластичны, что позволяет изменять их форму путем ковки, еще они имеют высокий коэффициент твердости. Отличительной особенностью этого элемента является блеск, который называется металлическим. Свойства металла делятся на две основные фракции, такие как:
- Физические свойства.
- Химические свойства.
Чем металлы отличаются от металлов по физическим характеристикам? К физическим свойствам относится:
- Цвет. Металлы, как правило, имеют плотную структуру, которая не пропускает сквозь себя свет. А их цвет определяется отражением света от его поверхности. Так, металлы в большинстве случаев имеют расцветку от серого до серебристого. Но есть и исключения, как, например, медь, которая имеет красный цвет, и золото, имеющее желтый окрас.
- Состояние формы, твердость и плотность. Сами по себе металлы имеют твердое агрегатное состояние, но способны переходить в жидкое при высоких температурах. Так, металлы плавятся при температуре от 40 до 3400 градусов по Цельсию. Но встречаются металлы, чье основное агрегатное состояние – жидкое. К таким элементам относят ртуть.
- Электропроводимость. Особенностью является ее снижение при повышении температуры вещества.
- Теплопроводность и температура кипения/плавления.
Чем металлы отличаются от металлов по химическим свойствам? В этой группе выделяют:
- Окисляемость. Также металлы окисляются, и оксидная пленка на поверхности может придать им другой оттенок.
- Вступление в реакцию с неметаллами, кислотами, водой, солями.

Чем металлы отличаются друг от друга
Многие не знают, чем металлы отличаются от металлов. Их различия можно классифицировать:
- Металлы между собой отличаются по цвету, как, например, золото и медь.
- Также металлы плавятся при разных температурах. Некоторые металлы, например, олово и свинец, можно расплавить в домашних условиях, а вот для остальных нужна более высокая температура.
- Между собой металлы делятся на две группы: тяжелые и легкие. К тяжелым металлам относятся те, чья плотность составляет от 5 г/см3, легкие металлы имеют плотность меньше 5 г/см3. К легким металлам относится литий, который имеет плотность 0.2 г/см3, место самого тяжелого металла делят между собой осмий и иридий. Их плотность составляет 22.6 г/см3.
- Металлы отличаются друг от друга пластичностью и электропроводность. Некоторые из них очень пластичны. К примеру, из всего лишь 1 грамма золота можно сделать тонкую проволоку в 3.5 километра. Она будет гибкой и не сломается. Повторить такое с менее пластичным металлом не получится.
- Также часть металлов проводит ток лучше, чем другие. Самыми электропроводными металлами признаны медь, серебро и алюминий. Их наиболее часто применяют в качестве проводящих элементов.
Чем неметаллы отличаются от металлов
Неметаллами принято называть элементы, которые имеют неметаллические свойства. Чем отличаются металлы от неметаллов? Рассмотрим подробнее:
- Форма. Так неметаллы имеют три агрегатных состояния: жидкое, твердое и газообразное.
- Электропроводимость. Неметаллы не проводят ток как металлы, имеют более низкую теплопроводность.
- Зрительные отличия. Металл легко отличить визуально от неметалла, так как первый имеет металлический блеск. К неметаллам относятся такие элементы как бром, сера и водород.
- Химическое строение. Также легко отличить их и по строению. Металлы имеют четкую кристаллическую решетку. У неметаллов строение ионное.
- Вступление в реакции. Неметаллы имеют большее число незанятых электронов, находящихся на внешних уровнях. Именно это позволяет им иметь высокую окислительную способность по сравнению с металлами.

Чем дерево похоже на металл и в чем их отличия
Дерево — это растительное сырье. Металл же это результат природного химического соединения. Чем отличается дерево от металла:
- Древесина не проводит электричество и возгорается при довольно низкой температуре по сравнению с металлами.
- Древесина не плавится при воздействии высоких температур.
- Также дерево плохо проводит тепло, в отличие от металлов.
- Древесина упругая, но не гибкая. Металлы же имеют более низкий коэффициент упругости, но они более пластичны. Так сложить пополам проволоку и не сломать ее можно легко, древесина при таком воздействии сломается пополам.
- Также отличительной чертой древесины от металла является то, что она не покрывается коррозией. Есть породы дерева, которые могут долгое время находиться в воде и не гнить. Металлы же при таких условиях покрываются ржавчиной.
- Плотность древесины достаточно низкая по сравнению с металлами. Хотя некоторые металлы имеют плотность ниже дерева, они относятся к легким металлам.

Чем отличаются полупроводники от металлов
Полупроводниками называются неметаллы, которые имеют некоторые металлические свойства. Металлы и полупроводники имеют схожесть в том, что и те, и другие способны проводить ток.
Но полупроводники имеют отличительную особенность, которая заключается в том, что их электропроводность может возрастать в несколько раз в зависимости от внешних факторов. Таким образом, полупроводник проводит ток лучше при повышении температуры. У металлов электропроводность с повышением температуры уменьшается. Также на электропроводность может повлиять наличие посторонних примесей. Так, в металлах примеси понижают электропроводность, а в полупроводниках повышают.
Полупроводники в отличие от металлов могут обладать позитивной и негативной электропроводимостью. Сами по себе полупроводники по способности пропускать сквозь себя ток стоят между металлом и элементами, которые не проводят ток совсем.

Отличие металла от стали
Ошибочно считать, что металл и сталь — это совершенно разные элементы. На самом деле сталь — это тоже металл. Чем отличается металл от стали?
Дело в том, что металлами называют целую группу элементов, которые имеют металлические свойства. В эту группу входит и железо. Сталь не что иное, как сплав железа с элементами, входящими в группу металлов.
Чаще всего в состав стали помимо железа входят такие элементы таблицы Менделеева как молибден, хром и ванадий. Также в состав стали входит и углерод. С помощью него повышают прочность железа.
Таким образом, варьируя количеством углерода в сплаве можно получить очень прочный материал. Но чем прочнее сталь, тем больше она становится хрупкой. Так, при длительной динамической нагрузке сталь легко ломается. Добавление других примесей к ней помогает добиться устойчивости к каким-либо воздействиям.

Итак, в статье было рассмотрено, чем металлы отличаются от металлов и неметаллов. Характеристики всех элементов можно сравнивать по химическим и физическим свойствам. Ежедневно человек пользуется такими элементами и создает новые вещества для улучшения качества жизни.
Источник
Напомню, что в одной из предыдущих частей мы ввели такие понятия как металлические и неметаллические свойства, теперь же пришло время научится отличать металлы от неметаллов по таблице Менделеева.
Многие из Вас, столкнувшись с данным вопросом, могут справедливо заметить, дескать: “Ха, вот глупости. Автор не от мира сего, ведь металлы и неметаллы в таблице Менделеева отмечены разным цветом! Как сейчас помню таблицу Менделеева в учебнике, где неметаллы отмечены красным цветом, а металлы – чёрным и зелёным. Шах и мат.”
Не спешите с критикой
Это всё замечательно, отвечу я, да только учащиеся, что приходят на экзамен по химии, получают чёрно-белый вариант таблицы Менделеева и Ваше возможное замечание окажется неуместно.
Тот самый черно-белый вариант
И прежде чем мы всё-таки ответим на поставленный вопрос, нам необходимо освоить несколько базовых химических понятий, касающихся работы с таблицей Менделеева. Дело в том, что помимо довольно однозначно определяемых периодов и групп, в таблице Менделеева есть место так же и для, так называемым, подгрупп.
С сегодняшнего дня мы начнём различать главную подгруппу (или подгруппу А) и побочную подгруппу (или подгруппу В).
Как же определить к какой подгруппе относится тот или иной химический элемент?
На отношение к той или иной подгруппе химического элемента нам могут указать следующие знаки:
Во-первых, нередко в шапочке, где указан номер группы, к которому относится столбец, есть указание и на подгруппы:
Главная подгруппа – А, побочная – В
Во-вторых, само положение химического символа химического элемента в ячейке указывает на отношение к подгруппе. Так, если химический символ химического элемента смещён относительно центра ячейки влево, то мы имеем дело с элементом главной подгруппы (подгруппы А), если же вправо – то побочной подгруппы (подгруппы В)
Например, в совершенно случайной чёрно-белой таблице Менделеева мы видим, что фосфор относительно центра ячейки смещён влево, это значит, что фосфор – элемент главной подгруппы (подгруппы А) пятой группы.
“адрес” фосфора: P – II (период), VА (группа – подгруппа), 15 (порядковый номер).
Как понятие о подгруппах поможет нам отличать металлы от неметаллов?
А вот как: дело в том, что все элементы побочных подгрупп – это металлы!
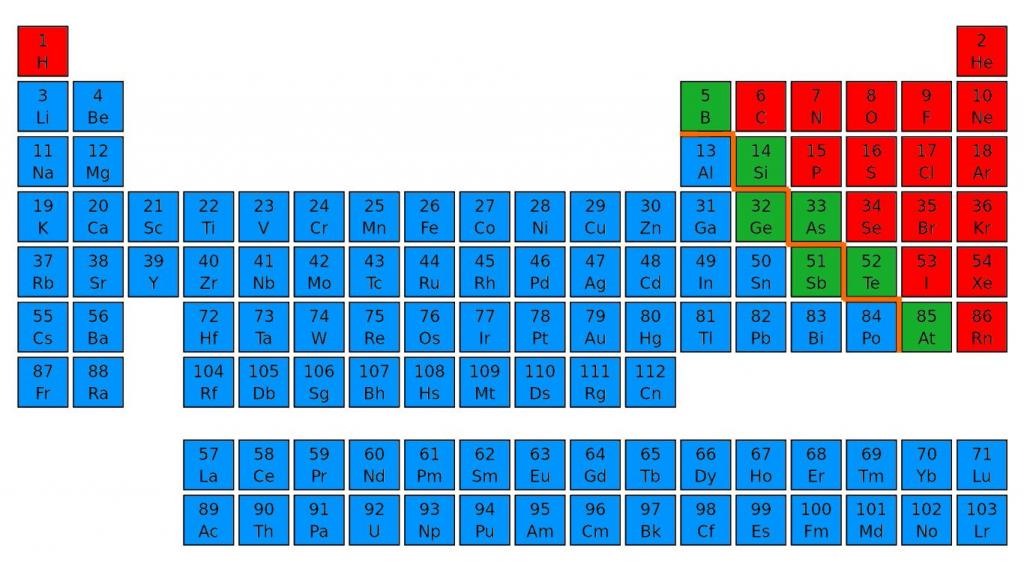
Красным выделены все элементы побочных подгрупп первых шести периодов. Все они – металлы.
А через элементы главных подгрупп мы можем провести одну особенную диагональ, которая “отсечёт” металлы от неметаллов.
Данная диагональ проходит через такие неметаллы, как бор (B) – кремний (Si) – мышьяк (As) – теллур (Te) – астат (As).
Зелёным цветом выделены все неметаллы в таблице Менделеева
Таким образом все элементы главных подгрупп, что лежат ниже и левее данной диагонали являются металлами, а все, что лежат выше и правее – неметаллами.
Однако нельзя не заметить, что деление на металлы (Ме) и неметаллы (неМе) всё же несколько условно, а некоторые таблицы, Менделеева, которые Вы можете найти в сети, игнорируют указанные мной правила работы с подгруппами.
В следующей части мы выделим закономерности, согласно которым металлические и неметаллические свойства изменяются в пределах рассматриваемой Периодической системы Менделеева и разберёмся, какое отношение к этому имеет атомный радиус. А на этом у меня всё. Спасибо. Пока.
Источник
Одни отдают электроны, другие принимают.
65
Автор: Алексей Морозов
Дата: 23.12.2020
Металлы – это такие элементы, которые стараются отдавать свои электроны. Неметаллы – наоборот, стараются их принимать. Вам надо понять, почему это происходит, и что значат фразы типа «металлические свойства усиливаются, а неметаллические ослабевают». Сейчас я вам это объясню.
Почему металлические свойства слабеют «слева направо»
Итак. В атоме есть три частицы: протоны, нейтроны и электроны. У протонов заряд +1, у электронов -1. У нейтронов заряда нет.
Протоны и нейтроны находятся в ядре. Поэтому заряд ядра всегда плюсовой. А электроны крутятся вокруг ядра и притягиваются к нему, потому что у них заряд минусовой.
Электроны крутятся по электронным уровням – как планеты по орбитам вокруг Солнца.
Атомный номер показывает, сколько в атоме протонов. Как видите, это количество постоянно увеличивается.
Чем больше протонов, тем сильнее они «тянут» к себе электроны. Сравните:
Вывод – чем больше становится протонов, тем сильнее они удерживают электроны. Тем сложнее становится эти электроны отдавать. Поэтому слева направо, с увеличением порядкового номера (и, соответственно, числа протонов) металлические свойства слабеют, а неметаллические усиливаются.
На заметку – про радиус атома
Чем сильнее протоны притягивают электроны, тем ближе эти электроны становятся к протонам. Поэтому радиус атома уменьшается, атом как бы сжимается из-за увеличения заряда.
Почему неметаллические свойства слабеют «сверху вниз»
Идем дальше. Период в таблице показывает количество уровней (тех самых орбит), по которым летают электроны.
Чем больше период, тем больше этих орбит и тем дальше оказываются электроны от ядра. Сравните:
Кому сложнее удерживать электроны на последнем уровне? Меди, конечно, потому что эти электроны в два раза дальше от ядра, чем, например, у лития. Их проще становится отдать, чем пытаться удерживать.
Следовательно, «сверху вниз» количество уровней, по которым движутся электроны, растет, удерживать их становится сложнее, поэтому металлические свойства усиливаются, а неметаллические – слабеют.
Еще про радиус
Если смотреть на таблицу «сверху вниз» радиус ядра растет, потому что уровней становится больше.
Да, заряд атома тоже растет, но все-таки расстояние перевешивает. Чем больше уровней, тем труднее становится держать электроны, даже несмотря на то, что заряд увеличивается.
Обобщаю:
- Слева направо в таблице металлические свойства слабеют, неметаллические усиливаются из-за того, что ядро сильнее тянет к себе электроны.
- Сверху вниз металлические свойства усиливаются, неметаллические слабеют, потому что уровней становится больше, и удерживать электроны на последних уровнях становится труднее.
Из этих двух положений следует, что в правом углу таблицы Менделеева будут сосредоточены неметаллы, а в левом – металлы.
Я нашел вам вот такую картинку, на ней показаны все неметаллы. То, что выделено курсивом – это так называемые металлоиды – вроде и не совсем металлы, и в то же время не неметаллы. Нечто среднее.
Это основа основ. Надеюсь, я объяснил понятно и вы разобрались. Если нет – перечитайте еще раз, задайте вопросы мне в комментариях. Только когда разберетесь – читайте дальше.
Свойства металлов
Эти свойства проявляются в разной мере, но все-таки присущи всем металлам:
- Плавятся.
- Их можно ковать.
- Обладают металлическим блеском.
- Проводят электрический ток. Это происходит благодаря металлической связи, которая соединяет их атомы.
- Проводят тепло.
- Твердые – это касается всех, кроме ртути.
На сегодняшний день металлов известно 87.
Свойства неметаллов
У них почти все наоборот:
- Ковать нельзя, потому что они хрупкие.
- Не обладают металлическим блеском.
- Не проводят электрический ток (за редким исключением – кремний и графит могут быть проводниками).
- Очень плохо проводят тепло.
- Есть твердые, газообразные, жидкие.
Неметаллов на данный момент 22.
Это первая статья по химии на нашем сайте. Напишите, что не так, что нравится и не нравится. Я буду думать, как сделать материал лучше.
И еще – есть идея записывать видеоролики с объяснениями. Лично вам удобнее разбираться в чем-то, читая текст, или просматривая видео?
Буду рад каждому вашему отзыву и комментарию.
ЕЖЕНЕДЕЛЬНАЯ РАССЫЛКА
Получайте самые интересные статьи по почте и подписывайтесь на наши социальные сети
ПОДПИСАТЬСЯ
Источник
Все химические элементы условно можно разделить на неметаллы и металлы. Знаете ли вы, по каким признакам они отличаются? Как определить их положение в таблице химических элементов? На эти и другие вопросы вы найдете ответы в нашей статье.
Положение неметаллов и металлов: таблица Менделеева
По внешним признакам и физическим свойствам не всегда можно выяснить, к какой группе относится химический элемент. Свойства металлов и неметаллов можно определить по расположению в периодической таблице.
Для этого нужно зрительно провести диагональ от бора до астата, от 5 до 85 номера. В правом верхнем углу будут преимущественно находиться неметаллы. Их в таблице меньшинство, всего 22 элемента. Металлы находятся в правой части периодической таблицы наверху – в основном в I, II и III группах.
Энергетический уровень
Отличия неметаллов и металлов первоначально обусловлены строением их атомов. Начнем с количества электронов на внешнем энергетическом уровне. У атомов металлов оно варьирует от одного до трех. Как правило, они обладают большим радиусом, поэтому атомы металлов достаточно легко отдают наружные электроны, так как имеют сильные восстановительные свойства.
У неметаллов число электронов на внешнем уровне больше. Это объясняет их окислительную активность. Неметаллы присоединяют недостающие электроны, полностью заполняя энергетический уровень. Самые сильные окислительные свойства проявляют неметаллы второго и третьего периода VI-VII групп.
Заполненный энергетический уровень содержит 8 электронов. Самой большой окислительной способностью обладают галогены с валентностью I. Среди них лидирует фтор, так как у этого элемента нет свободных орбиталей.

Строение металлов и неметаллов: кристаллические решетки
Физические свойства веществ определяются порядком расположения элементарных частиц. Если условно соединить их воображаемыми линиями, то получится структура, которая называется кристаллической решеткой. В ее узлах могут находиться разные структуры: атомы, молекулы или заряженные частицы – ионы.
У некоторых неметаллов формируется атомная кристаллическая решетка, частицы которой соединены ковалентными связями. Вещества с таким строением твердые и нелетучие. К примеру, фосфор, кремний и графит.
В молекулярной кристаллической решетке связь между элементарными частицами слабее. Обычно подобные неметаллы находятся в жидком или газообразном агрегатном состоянии, но в некоторых случаях – это твердые легкоплавкие неметаллы.
В любом образце металла часть атомов теряет наружные электроны. При этом они превращаются в положительно заряженные частицы – катионы. Последние снова соединяются с электронами, образуя нейтрально заряженные частицы – в металлической решетке одновременно находятся катионы, электроны и атомы.

Физические свойства
Начнем с агрегатного состояния. Традиционно принято считать, что все металлы – твердые вещества. Исключением является только ртуть, тягучая жидкость серебристого цвета. Ее пары являются контаминантом – токсичным веществом, вызывающим отравление организма.
Еще одна характерная черта – металлический блеск, который объясняется тем, что поверхность металла отражает световые лучи. Еще одна важная особенность – электро- и теплопроводность. Это свойство обусловлено наличием в металлических решетках свободных электронов, которые в электрическом поле начинают двигаться направленно. Лучше всех проводит тепло и ток ртуть, наименьшими показателями обладает серебро.
Металлическая связь обусловливает ковкость и пластичность. По этим показателям лидирует золото, из которого можно раскатать лист толщиной в человеческий волос.
Чаще всего физические свойства металлов и неметаллов противоположны. Так, последние характеризуются невысокими показателями электро- и теплопроводности, отсутствием металлического блеска. При обычных условиях неметаллы находятся в газообразном или жидком состоянии, а твердые всегда хрупкие и легкоплавкие, что объясняется молекулярным строением неметаллов. Алмаз, красный фосфор и кремний – тугоплавкие и нелетучие, это вещества с немолекулярным строением.

Что такое полуметаллы
В периодической таблице между металлами и неметаллами находится ряд химических элементов, которые занимают промежуточное положение. Их называют полуметаллами. Атомы полуметаллов связаны ковалентной химической связью.
Эти вещества совмещают признаки металлов и неметаллов. К примеру, сурьма является кристаллическим веществом серебристо-белого цвета и вступает в реакцию с кислотами, образуя соли – типичные металлические свойства. С другой стороны, сурьма – очень хрупкое вещество, которое не поддается ковке, а измельчить его можно даже вручную.
Итак, типичные неметаллы и металлы обладают противоположными свойствами, но деление это достаточно условно, поскольку ряд веществ сочетает в себе и те и другие признаки.
Источник
