Какие свойства нафталина лежат в основе его применения
| Нафталин | |
|---|---|
| Систематическое наименование | Нафталин |
| Традиционные названия | Нафталин, антимит, гексален |
| Хим. формула | С10Н8 |
| Рац. формула | С10Н8 |
| Молярная масса | 128,17052 г/моль |
| Плотность | 1,14 г/см3 (15,5 °C); 1,0253 г/см3 (20 °C); 0,9625 г/см3 (100 °C)[1] |
| Энергия ионизации | 8,12 ± 0,01 эВ[2] |
| Температура | |
| • плавления | 80,26 °C |
| • кипения | 217,97[1] °C |
| • вспышки | 79—87 °C |
| Пределы взрываемости | 0,9 ± 0,1 об.%[2] |
| Мол. теплоёмк. | 165,72[1] Дж/(моль·К) |
| Энтальпия | |
| • образования | 78,53[1] кДж/моль |
| Давление пара | 0,08 ± 0,01 мм рт.ст.[2] |
| Показатель преломления | 1,5898[1] |
| Рег. номер CAS | 91-20-3 |
| PubChem | 931 |
| Рег. номер EINECS | 202-049-5 |
| SMILES | c1cccc2c1cccc2 |
| InChI | InChI=1S/C10H8/c1-2-6-10-8-4-3-7-9(10)5-1/h1-8H UFWIBTONFRDIAS-UHFFFAOYSA-N |
| RTECS | QJ0525000 |
| ChEBI | 16482 |
| ChemSpider | 906 |
| Предельная концентрация | 20 мг/дм³ |
| ЛД50 | 5000-12376 мг/кг |
| Токсичность | Класс опасности 4 |
| NFPA 704 | 2 2 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
| Медиафайлы на Викискладе | |
Нафтали́н (бицикло-[4.4.0]-дека-1,3,5,7,9-пентаен) — твердое кристаллическое вещество с характерным запахом. В воде не растворяется, но хорошо растворим в бензоле, эфире, спирте, хлороформе.
Химические свойства[править | править код]
Нафталин по химическим свойствам сходен с бензолом: легко нитруется, сульфируется, взаимодействует с галогенами. Отличается от бензола тем, что ещё легче вступает в реакции[3].
Физические свойства[править | править код]
Плотность 1,14 г/см³, температура плавления 80,26 °C, температура кипения 217,7 °C, растворимость в воде примерно 30 мг/л, температура вспышки 79—87 °C, температура самовоспламенения 525 °C, молярная масса 128,17052 г/моль.
Электропроводность[править | править код]
Кристаллический нафталин имеет заметную электропроводность при комнатной температуре с удельным сопротивлением около 1012 Ом·м. При плавлении удельное сопротивление уменьшается более чем в тысячу раз, примерно до 4·108 Ом·м.
Как в жидком, так и в твердом виде сопротивление зависит от температуры приблизительно как
, где (Ом·м) и (эВ) — некоторые постоянные параметры, — постоянная Ботльцмана (8,617·10−5 эВ/K), а — абсолютная температура (K). Параметр равен 0,73 эВ в твёрдом нафталине. В твёрдом виде имеет полупроводниковый тип проводимости при температуре даже ниже 100 К[4][5].
Получение[править | править код]
Нафталин получают из каменноугольной смолы.
Также нафталин можно выделять из тяжёлой смолы пиролиза (закалочное масло), которая применяется в процессе пиролиза на этиленовых установках. Ещё одним способом промышленного получения нафталина является деалкилирование его алкилпроизводных.
В природе нафталин выделяют термиты вида Coptotermes formosanus, чтобы защитить свои гнёзда от муравьёв, грибков и нематод[6].
Применение[править | править код]
Важное сырьё химической промышленности: применяется для синтеза фталевого ангидрида, тетралина, декалина, разнообразных производных нафталина.
Производные нафталина применяют для получения красителей и взрывчатых веществ, в медицине, как инсектицид моли в быту.
Крупные монокристаллы применяются в качестве сцинтилляторов для регистрации ионизирующих излучений.
Может использоваться для создания синтетических аналогов каннабиноидов.
Влияние на здоровье[править | править код]
При остром отравлении нафталин вызывает головные боли, тошноту, рвоту, раздражение слизистых оболочек. Длительное воздействие нафталина может вызвать повреждение или разрушение красных кровяных телец (эритроцитов). Хроническое воздействие нафталина также приводит к нарушению работы печени и поджелудочной железы, вызывает развитие атрофического ринита и фарингита.
International Agency for Research on Cancer (IARC) классифицировала нафталин как возможный канцероген, вызывающий рак у людей и животных [Group 2B].
В человеческом организме чаще всего концентрируется в жировой ткани, где может накапливаться до тех пор, пока жировая ткань не начнёт сжигаться, и данное вещество (нафталин) не попадёт в кровь, после чего наступает отравление организма (кровотечения, возникновение опухолей и т. д.).
См. также[править | править код]
- Малоопасные вещества
- Органические вещества
Примечания[править | править код]
Литература[править | править код]
- Новый справочник химика и технолога. Радиоактивные вещества. Вредные вещества. Гигиенические нормативы / Редкол.: Москвин А. В. и др.. — СПб.: АНО НПО «Профессионал», 2004. — 1142 с.
Источник
Что такое нафталин? Вещество представляет собой химический состав, который выступает продуктом переработки кокса и нефти. Внешне имеет вид твердых кристаллов. Обладает углеводородной структурой. Представленная субстанция не растворяется в воде, однако разрушается под воздействием бензолов.
Сферы применения
Что такое нафталин? Это субстанция, известная своей высокой химической активностью. Вещество находит широкое применение в металлургической и текстильной промышленности. Известны также полезные качества нафталина, которые используются в народной медицине. Применяют вещество и в быту. В частности, таблетки нафталина выступают эффективным инсектицидом.
Народная медицина
Что такое нафталин и какими целебными свойствами обладает вещество? Положительный терапевтический эффект на организм средство оказывает при различного рода инфекциях, заболеваниях дыхательных органов. В данных целях кристаллы нафталина помещают в кипяченую воду и прибегают к ингаляциям. Подобные методы лечения нередко практикуются в санаториях. Ингаляции с использованием нафталина оказывают антибактериальное воздействие на слизистые оболочки легких, ротовой полости, носоглотки. Главной целью подобных мероприятий выступает активизация отделения слизи из бронхов.

Нафталин используют для устранения инфекционных поражений органов желудочно-кишечного тракта. Антисептические свойства вещества способствуют восстановлению нормальной работы пищеварительной системы. Облегчение применение нафталина приносит также при развитии энтероколитов и диареи.
Что такое нафталин, было хорошо известно нашим предкам. В древности вещество применяли в целях противоглистной терапии. Считалось, что нафталин позволяет изгнать из организма ленточных паразитов. Для борьбы с гельминтами несколько грамм субстанции принимают внутрь 3-4 раза в день. Если паразиты не исчезают, терапия повторяется через неделю.
Издавна народным средством на основе нафталина лечили подагру. Для его приготовления порядка 25 граммов растертых в порошок кристаллов смешивали с молоком. Состав подвергали кипячению, а затем на 10-15 минут оставляли на водяной бане, периодически помешивая. Полученное лекарство помещали в холодное место. Средство применяли для смазывания участков тела, в которых наблюдались воспалительные процессы.
В народной медицине вещество используют для устранения патологических проявлений на коже. Нафталин оказывает положительный эффект при лечении псориаза и экземы. Измельченные кристаллы обладают обеззараживающим действием на незаживающие раны.

Использоваться химическая субстанция может при ухудшении зрения. В прошлом офтальмологи и гомеопаты рекомендовали применять нафталин в случае развития катаракты, а также отслоениях тканей сетчатки.
Применение нафталина в онкологии
Вещество известно своими чудодейственными свойствами в борьбе со злокачественными опухолями. Химическая субстанция оказывает деструктивное воздействие на новообразования ракового характера. Для приготовления лекарства чайная ложка нафталина соединяется со 100 граммами кипяченой воды. На протяжении дня средство принимают внутрь по одному глотку через каждый час. Продолжительность терапии зависит от индивидуальных особенностей организма и характера заболевания.
Нафталин от моли
Само по себе химическое вещество не приводит к уничтожению насекомых, не вредит кладкам их яиц и личинкам. Зато запах нафталина прекрасно отпугивает моль. Интенсивный аромат не позволяет бабочкам таких насекомых размножаться в одежде, всевозможных тканях.

Как правильно пользоваться средством? Таблетки препарата раскладываются по холщевым мешочкам. Средство помещается в шкафы, укладывается в карманы одежды. Постепенно образуются пары нафталина. Частицы вещества создают в воздушном пространстве своеобразную пелену, которая не позволяет моли паразитировать на тканях.
Предостережения
Нафталин выступает токсичным веществом. При его употреблении в количестве более 10 граммов возникает сильное отравление организма, что ведет к летальному исходу. Навредить человеку могут также пары химической субстанции. Продолжительное вдыхание аромата вещества способно повлечь за собой нарушение координации движений, обморочные состояния, проблемы с функционированием почек. Поэтому применять нафталин в терапевтических целях рекомендуется исключительно под контролем врача.
Источник
Нафталин является производным продуктом нефти и кокса. Это ароматический углеводород, который представляет собой белые твердые кристаллы с характерным запахом. Вещество не растворяется в воде, но поддается воздействию бензола и бензина.

Нафталин используют в химической, текстильной, металлургической промышленностях. Известны полезные свойства этого углеводорода, которые позволяют применять его в быту. Например, благодаря специфическому запаху, он отпугивает моль, и поэтому, вполне заслуженно считается хорошим инсектицидом.
Как лечиться нафталином
Это едкое вещество и его производные нашли широкое применение в альтернативной (гомеопатия) и народной медицине. Рассмотрим подробнее целебные свойства нафталина.
1. Хороший лечебный эффект, при заболевании дыхательных путей и различных инфекционных заболеваниях, дают ингаляции паров воды с кристаллами нафталина. Такое лечение практикуют в некоторых санаторно-курортных учреждениях. Подобные ингаляции действуют антибактериально на слизистую оболочку: носа, ротовой полости, горла и легких. Процедура облегчает отделение слизи из бронхов.
2. Еще в 19 веке были замечены целебные свойства нафталина в лечении кишечных инфекций. Антисептическое действие этого углеводорода помогает восстановить пищеварительную функцию и работу кишечника при поносах и энтероколитах.
3. В старых книгах народных рецептов встречаются записи по изгнанию ленточных глистов с помощью нафталина. В течение дня нужно принять 1,2 грамма этого вещества, разбив его на четыре приема. В случае необходимости такое лечение следует повторить через семь дней.
4. В старину подагру лечили рецептом, в состав которого входил нафталин. Готовили смесь: в стакан домашнего молока добавляли 25 г растертого в порошок вышеупомянутого углеводорода, размешивали, доводили до кипения и ставили на 10 минут на водяную баню. (Все время помешивая). Когда снадобье остынет, его нужно перелить в бутылку, плотно закупорить и поместить для хранения в холодильник. Этой «мазью» дважды в день смазывают все воспаленные и больные места.
5. Как противомикробное и противовоспалительное средство нафталин используют в борьбе с кожными болезнями: экземой, псориазом, рожистыми поражениями. Слабым раствором также обрабатывают незаживающие раны.
6. Согласно опытным данным известного врача-гомеопата Л. Хартмана, прием этого производного из дегтя продукта при туберкулезе устраняет такие симптомы как чрезмерное ночное потоотделение и изнуряющий кашель.
7. Врачи – гомеопаты используют такой продукт нефтехимического производства для лечения различных недугов: глазных болезней (катаракта, отслоение сетчатки), аллергии, мастопатии, пиелонефрита, цистита и гонореи.
От онкологии
Среди множества народных рецептов можно обнаружить описание по применению нафталина в лечении злокачественных опухолей и полипов в желудочно-кишечном тракте. Он оказывает разрушающее действие на раковые новообразования. В большинстве источников для лечения рекомендуют брать щепотку этого вещества и, растворять его в 100 миллилитрах кипятка. В течение дня раствор пьют по чайной ложке через каждый час. Длительность лечения назначаются индивидуально.
Против гноя
Способность нафталина «выедать» гной и, тем самым, способствовать очищению ран, использовали давно и в военной медицине. Однако после такой терапии целесообразно назначать кровоостанавливающие, противовоспалительные и ранозаживляющие средства.
Осторожность превыше всего
 Нафталин в разумных количествах может оказывать целительное действие. Но следует также помнить, что этот углеводород является токсическим веществом и может вызвать сильное отравление. Например, доза более 10 грамм в сутки для взрослого человека – является смертельной. Для маленького ребенка даже 0,4 грамма нафталина в организме могут вызвать летальный исход.
Нафталин в разумных количествах может оказывать целительное действие. Но следует также помнить, что этот углеводород является токсическим веществом и может вызвать сильное отравление. Например, доза более 10 грамм в сутки для взрослого человека – является смертельной. Для маленького ребенка даже 0,4 грамма нафталина в организме могут вызвать летальный исход.
Отравиться нафталином можно не только, принимая его внутрь. Вдыхание и непосредственный контакт токсичного вещества с кожей также приводят к серьезным последствиям со здоровьем. При отравлении могут возникнуть: состояние оцепенения, нарушение координации, полная потеря сознания, сильная диспепсия, проблемы с почками.
Поэтому использование нафталина в лечебных целях должно проводиться только под контролем профессионального и опытного специалиста.
Загрузка…
Источник
Легкокристаллизирующийся нафталин (т.пл. 80оС) был выделен из каменноугольной смолы раньше бензола, еще в 1819 г. Гарденом.Содержание нафталина в этом источнике достигает 6% и он не потерял своего значения до наших дней. Состав нафталина был определен в 1838 г. Воскресенским, а строение установлено в 1866 г. Эрленмейером и Гребе.Приписываемое нафталину строение – два конденсированных бензольных кольца – подтверждено многочисленными синтезами и результатами физико-химических методов исследований. Однако метод доказательства, использованный Эрленмейером и Гребе, имеет познавательное значение. Поэтому он вполне заслуживает упоминания.
Эрленмейеру и Гребе было известно, что нафталин и α-нафтиламин при окислении образуют о-фталевый ангидрид, а α-нитронафталин – о-нитрофталевый ангидрид
Этих данных оказалось вполне достаточно, чтобы убедиться, что оба кольца в нафталине бензольные, равноценные и связаны они в двух точках.
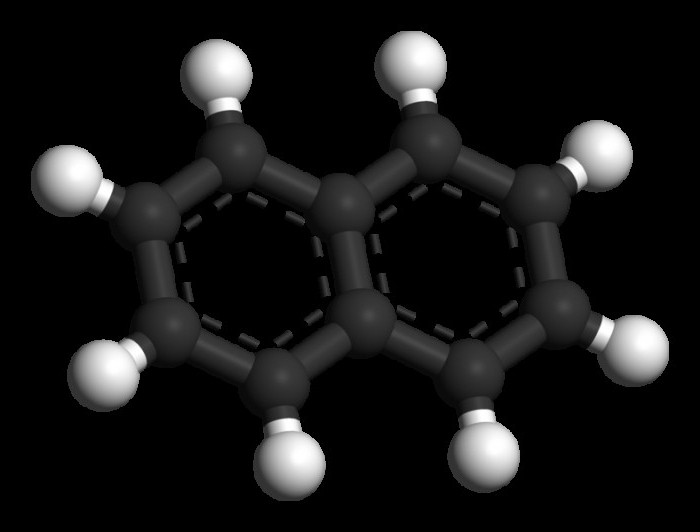
Строение нафталина.По современным представлениям нафталин представляет собой систему из двух бензольных колец, в которой все углероды sp2-гибридизованы и лежат в одной плоскости. В отличие от бензола, у которого все связи между углеродами имеют одинаковую длину, в нафталине он отличаются друг от друга
То, что в нафталине связи имеют различную длину и кольца не симметричны, свидетельствует о неравномерном характере распределения электронной плотности в молекуле.
Нафталин подчиняется правилу Хюккеля для ароматических систем – 4n + 2 при n=2 и содержит 10π-электронов.
Хотя нафталин и проявляет ароматический характер, однако он выражен в меньшей степени, чем у бензола. Как известно, бензол термодинамически более выгоден, чем гипотетический циклогексатриен на величину 150,73 кДж/моль. Можно было бы ожидать, что для нафталина, состоящего из двух бензольных колец, энергия резонанса составит величину 150,73 х2=301,46 кДж/моль. Однако резонансная энергия нафталина всего лишь 255,41 кДж/моль.
Таким образом, нафталин – ароматическая система, которая, однако, менее ароматична, чем бензол.
Не все свойства нафталина могут быть объяснены исходя из формул
Для объяснения некоторых реакций нафталина, в которые он вступает вопреки вышеприведенным формулам, изобразим его в виде резонансных структур
Из рассмотрения этих канонических формул видно, что в двух случаях из трех – II и III – на одно из колец приходится лишь две π-связи. Отсюда следует, что нафталин, с учетом вклада этих структур в резонансный гибрид, может рассматриваться как сочетание бензольного кольца с 1,3-диеновой системой. С учетом этого обстоятельства предлагалось молекулу нафталина изображать как систему, состоящую из бензола и диена
При таком подходе к строению нафталина становятся объяснимыми такие его свойства как склонность к вступлению в реакции 1,4-присоединения
Удалось осуществить с нафталином за счет его 1,3-диеновой составляющей и такую классическую реакцию как реакция Дильса-Альдера. Правда, для этого пришлось использовать сильные диенофилы в жестких условиях (более 150оС)
Способы получения. Нафталин образуется при пропускании ацетилена или же ацетилена и бензола над древесным углем при 400оС
Также как и в случае бензола, нафталиновые углеводороды могут быть получены реакцией дегидроциклизации исходя из подходящих алкилбензолов (Pt, 300оС)
Для получения нафталина можно использовать и реакцию диенового синтеза с участием диенов и бензохинона в качестве диенофила
Наиболее универсальным синтезом нафталиновых соединений является, пожалуй, метод Хеуорса,представляющийсобой сочетание реакций ацилирования, восстановления оксо-групп по Клеменсену и ароматизацию тетралина дегидрированием
Синтез Хеуорса предоставляет широкие возможности для его модификации:
– при использовании замещенных бензолов заместитель в нафталине оказывается в β-положении;
– при помощи магнийорганического синтеза с участием оксо-групп β-бензоилпропионовой кислоты и тетралона в нафталиновое кольцо можно ввести одинаковые или различные заместители;
– при использовании замещенных янтарных ангидридов появляется возможность получения 2,3-дизамещенных нафталинов.
Химические свойства. Как уже отмечалось, нафталин – ароматическое соединение. Он вступает в реакции замещения, присоединения и восстановления – окисления.
В реакциях электрофильного замещения нафталин активнее бензола. Следует только отметить, что речь идет об одном из бензольных колец – первом. Для нарушения его ароматичности требуется лишь 104,68 кДж/моль, а оставшееся кольцо реагирует уже как обычное соединение моноароматического ряда. В этом случае для нарушения ароматичности требуется уже 150,73 кДж/моль.
В отличие от бензола, у нафталина два неравноценных положения α– и β. Поэтому электрофил в общем случае мог бы занять любое из них
Однако оказалось, что в реакциях электрофильного замещения с участием нафталина более привлекательным является α-положение. Происходит это потому, что σ-комплекс с α-положением заместителя I оказывается более стабильным, чем другой возможный σ-комплекс II. Это хорошо видно, если эти комплексы изобразить, воспользовавшись теорией резонанса
При α-замещении σ-комплекс, представляющий собой резонансный гибрид структур III, IV и V, включает в себя две неустойчивые канонические структуры с сохранением одного бензольного кольца – III и IV. В то же время σ-комплекс, образовавшийся при β-замещении включает лишь одну стабильную предельную структуру с сохранением бензольного кольца – VI. Это обстоятельство и обуславливает большую устойчивость I по сравнению с II. Считают, что I энергетически на 41,87 кДж/моль более выгодна, чем II.
Рассмотрим теперь конкретные реакции электрофильного замещения в нафталиновом ряду.
Нитрование и галогенирование. Нафталин нитруется и галогенируется в α-положение. Реакции идут настолько легко, что, например, галогенирование протекает даже без участия катализатора
Через галоген- и нитро-производные открываются возможности для синтеза многих производных нафталина через амины и диазосоединения, а также через магнийорганические соединения.
Ацилирование. Нафталин под действием ацилирующих агентов в присутствии хлорида алюминия ацилируется. При этом место вступления остатка кислоты зависит от растворителя: в сероуглероде, тетрахлорэтане имеет место α-замещение, а в нитробензоле – в β-положение нафталиновой системы
Предполагается, что нитробензол образует как с хлористым ацетилом, так и хлоридом алюминия, комплексы, для которых α-положение нафталина менее доступно по пространственным соображениям.
Сульфирование. Результаты сульфирования нафталина зависят от температуры, при которой проводится реакция. При повышенной температуре (160оС) основным продуктом реакции является β-нафталинсульфокислота, а при более низкой температуре – α-изомер
Интересно при этом, что при нагревании до 1600С α-изомер превращается в β-изомер.
Эти факты можно объяснить тем, что при более низких температурах сульфирования накопление продуктов реакции происходит в соответствии с относительными скоростями образования изомерных кислот. Уже отмечалось, что α-положение нафталина более подвержено электрофильной атаке, т.к. в этом случае реакция идет через более стабильный σ-комплекс (кинетический контроль). При повышенных температурах накопление продуктов идет в соответствии с термодинамическими устойчивостями изомеров – здесь преимущество за β-изомером нафталинсульфокислоты (термодинамический контроль).
В случае участия в реакциях электрофильного замещения производных нафталина, место вступления нового заместителя диктуется имеющимся заместителем.
При этом электронодонорные заместители способствуют реакции и новый заместитель направляют в α-положение того же кольца
В то же кольцо вступает новый заместитель и в том случае, если в замещенном нафталине электронодонорный заместитель находится в β-положении
Электроноакцепторный заместитель в нафталине новый заместитель направляет в незамещенное кольцо в положения 5 и 8
Электроноакцепторный заместитель в нафталине в β-положении затрудняет реакцию и новый заместитель направляет в незамещенное кольцо в положения 5 и 8
Кроме рассмотренных реакций, нафталин способен к окислению и восстановлению.
Восстанавливается нафталин легче, чем бензол, даже атомарным водородом. При этом в зависимости от температуры реакции, восстановление идет в положения 1 и 4 или 1, 2, 3 и 4
При каталитическом гидрировании нафталин вначале образует тетралин, который далее может, при более жестких условиях, превратиться в декалин
Интересно отметить, что декалин существует в виде цис– и транс-изомеров. В цис-изомере водороды у общих для двух циклогексановых колец углеродов расположены в цис-положении, а у транс-изомера – в транс-положении
В зависимости от условий проведения реакции, окисление нафталина приводит к различным кислоросодержащим продуктам. При окислении оксидом хрома в среде уксусной кислоты при комнатной температуре продуктом реакции оказывается нафтахинон, а окисление бихроматом калия направляется на боковую алкильную цепь
Нафталин окисляется легче, чем бензол. Это позволяет окислить одно бензольное кольцо нафталина, сохранив другое
На этом основано получение о-фталевого ангидрида в промышленных масштабах.
Источник
