Какие свойства воды описаны вода химическое соединение которое в природе
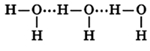
Оксид водорода (H2O), гораздо более известный всем нам под названием “вода”, без преувеличения, является главной жидкостью в жизнедеятельности организмов на Земле, ибо все химико-билогические реакции проходят, либо с участием воды, либо в растворах.
Вода является вторым, после воздуха, самым важным веществом для организма человека. Прожить без воды человек может не более 7-8 суток.
Чистая вода в природе может существовать в трех агрегатных состояниях: в твердом – в виде льда, в жикдом, собственно вода, в газообразном – в виде пара. Таким разнообразием агрегатных состояний в природе больше не может похвастаться ни одно вещество.
Физические свойства воды
- при н.у. – это жидкость без цвета, запаха и вкуса;
- вода обладает высокой теплоёмкостью и низкой электропроводностью;
- температура плавления 0°C;
- температура кипения 100°C;
- максимальная плотность воды при 4°C равна 1 г/см3;
- вода – хороший растворитель.
Строение молекулы воды
Молекула воды состоит из одного атома кислорода, который соединен с двумя атомами водорода, при этом связи O-H образуют угол в 104,5°, при при этом общие электронные пары смещены к атому кислорода, который более электроотрицателен по сравнению с атомами водорода, поэтому, на атоме кислорода формируется частичный отрицательный заряд, соответственно, на атомах водорода – положительный. Таким образом, молекулу воды можно рассматривать, как диполь.
Молекулы воды могут между собой образовывать водородные связи, притягиваясь противоположно заряженными частями (на рисунке водородные связи показаны пунктиром):
Формирование водородных связей объясняет высокую плотность воды, температуру ее кипения и плавления.
Количество водородных связей зависит от температуры – чем выше температура, тем меньшее кол-во связей образуется: в парах воды присутствуют только отдельные ее молекулы; в жидком состоянии – образуются ассоциаты (H2O)n, в кристаллическом состоянии каждая молекула воды связана с соседними молекулами четырьмя водородными связями.
Химические свойства воды
Вода “охотно” вступает в реакции с другими веществами:
- с щелочными и щелочноземельными металлами вода реагирует при н.у.:
2Na+2H2O = 2NaOH+H2↑
- с менее активными металлами и неметаллами вода реагирует только при высокой температуре:
3Fe+4H2O=FeO → Fe2O3+4H2↑
C+2H2O → CO2+2H2↑ - с основными оксидами при н.у. вода реагирует с образованием оснований:
CaO+H2O = Ca(OH)2
- с кислотными оксидами при н.у. вода реагирует с образованием кислот:
CO2+H2O = H2CO3
- вода является главным участником реакций гидролиза (подробнее см. Гидролиз солей);
- вода участвует в реакциях гидратации, присоединяясь к органическим веществам с двойными и тройными связями.
Растворимость веществ в воде
- хорошо растворимые вещества – в 100 г воды растворяется более 1 г вещества при н.у.;
- малорастворимые вещества – в 100 г воды растворяется 0,01-1 г вещества;
- практически нерастворимые вещества – в 100 г водры растворяется менее 0,01 г вещества.
Совершенно нерастворимых веществ в природе не существует.
При растворении многих веществ в воде вокруг их молекул образуется оболочка из молекул воды – такой “слоеный пирог” называется гидратом. После кристаллизации в составе таких комплексов сохраняются некоторая часть молекул воды, образуя кристаллогидрат:
CuSO4+5H2O = CuSO4·5H2O
См. далее:
- Жесткость воды
- Пероксид водорода (H2O2)
Источник
Вода — это необыкновенная субстанция, которая не перестает
нас удивлять. Она основной компонент планеты, вода необходима для жизни всего
живого. Люди могут выдержать без воды только несколько дней. Если не
восстановить вовремя ее потери в организме, это верная смерть. Поэтому важно
научиться разумно, тратить ее и знать, что же такое вода.
Химические названия
Почему же воду назвали водой? Слово «вода» происходит от
древнегерманского «мокрый, текучий». В химии могут встречаться разные названия
этого соединения. Самые распространенные – гидроксид водорода и окись водорода.
Также в химической литературе ее называют:
- монооксид дигидрофосфата;
- гидроксильная кислота;
- дигидромонооксид
- оксидан

Образование воды
Многих интересует, какая вода находится в реках, морях, под
землей. Образовавшаяся миллиарды лет назад вода сконцентрировалась в океанах.
Из океанов она испаряется и поднимается, где образуются облака. После долгого
путешествия она возвращается на землю в виде осадков. Вода собирается и
возвращается через реки обратно в море. Часть просачивается в почву и попадает
в грунтовые воды. Там формируются новые источники, которые текут в море.
В более холодном климате вода остается на ледниках, которые
очень медленно, стекают к более низким высотам, где и тают. В полярных регионах
этот механизм скольжения настолько медленный, что в ледниках можно найти воду,
попавшую на поверхность Земли десятки тысяч лет назад. Вот откуда берется в
природе вода.
Свойства
Влияние воды на жизнь на земле огромное. Это среда обитания
для многих организмов. Она является хорошим растворителем не только для солей,
но и для многих других веществ. Например, питательные соли присутствуют в почве
в виде ионов, то есть в растворенном виде. Только в таком виде растения могут
поглощать их через корни. Поэтому не случайно вода— это источник жизни на
земле.
Вода является важным источником химических и биохимических
реакций, например, для фотосинтеза. Это заметно, когда растение увядает из-за
потери воды, а листья и цветы опадают. Не зря говорят, что вода—это главный
источник жизни.

Физические свойства
Что мы все знаем о воде? То, что она состоит из одного атома
кислорода и двух атомов водорода, знают все, а вот о том что они притягиваются,
друг к другу водородной мостиковой связью знают не все. Эта связь объясняет ее
основные свойства.
- Н2О имеет высокое поверхностное натяжение, то есть
тенденцию принимать сферический объем. - Другим свойством является капиллярность. Молекула H2O
способна перемещаться в очень узких пространствах. - Удельная теплоемкость у нее примерно в 4 раза больше,
чем у воздуха. Это определяет устойчивость к изменениям температуры. - Плотность воды увеличивается с понижением температуры,
примерно до 4 С. Ниже этого порога плотность уменьшается. - Она обладает минимальной вязкостью при высоких
давлениях. Поэтому, чем больше давление, тем легче ей проникать.
Агрегатные состояния
В нормальных условиях вода, является жидкостью. Это
единственное известное вещество, которое существует в природе во всех трех
классических состояниях материи: жидком, твердом, газообразном.
Кстати, термин вода используется для жидкого агрегатного
состояния. В твердом, то есть в замороженном состоянии, она называется льдом, в
газообразном состоянии— водяным паром или просто паром. Существует порог, где
при определенных температурах и равновесного давления три состояния могут
сосуществовать одновременно.

Оптические свойства
Когда свет пересекает границу раздела вода-воздух, полное
отражение происходит под углом 49 град. Это означает, что световые лучи,
попадающие на граничную поверхность, не излучаются из воды, а отражаются.
Преломление света приводит к оптическим иллюзиям. Поэтому
под водой объекты видятся не в том месте, где они находятся на самом деле. То
же самое происходит если смотреть через воду на воздух. Светопропускная
ценность воды обеспечивает присутствие в ней водорослей и растений, которым
необходим свет для жизни. Длинноволновый (красный) свет поглощается сильнее,
чем коротковолновый (синий) свет.
Изотопные модификации
Молекулы воды состоят из разных изотопов кислорода и
водорода, каждый из которых встречается в разных концентрациях. В определенных
процессах, таких как образование осадков и фазовые переходы, происходит
фракционирование изотопов, то есть Н2О меняет свой изотопный состав. В
зависимости от условий окружающей среды и исходного состава это приводит к
определенным изотопным сигналам, которые могут выступать в качестве своего рода
отпечатка пальца для различных процессов и областей происхождения. Эта
методология используется в гидрогеологии и палеоклиматологии.
Химические свойства
Вода амфотерна, в зависимости от окружающей среды, может
действовать как кислота и основание. В водных растворах сильные кислоты и
сильные основания полностью диссоциируют на ионы H 3 O + и O H. Это называется
выравнивающим эффектом воды. Чтобы иметь возможность различать очень сильные
кислоты по кислотности, константы равновесия определяют в неводных растворах, и
переносят в растворитель воду.

Многих интересует, вода является органическим веществом или
неорганическим. С точки зрения химии, она относится к неорганическим веществам.
Поскольку, в органики должен присутствовать углерод, а в воде его нет.
Волновая функция основного состояния воды
Под водой скорость звука в 4,4 раза выше, чем у поверхности,
и составляет 1483 м /с при температуре 20 С. Поэтому пространственное
восприятие звука под водой сильно затруднено, мозг просто не успевает
обработать информацию. Важно знать, что звук под водой не только проходит
быстрее, но также в большей степени чем в воздухе зависит от частоты. Поэтому
глубокие частоты, такие как звуки больших морских двигателей, часто могут быть
услышаны драйверами на расстоянии нескольких километров.
В природе
Вода в природе везде. Реки и океаны, облака на небе, к этому
добавляются грунтовые воды и те, которые постоянно хранятся в почве и
обеспечивает основу для ее плодородия. Вода в природе — это жизнь, без воды все
ничто. Она— основа плодородия, без нее не было бы ни растений, ни пищи.
Атмосферные осадки
Вода в природе находится в круговороте. Испаряясь, она
поднимается как водяной пар в атмосферу. За тем крошечные капельки собираются и
образуют облака. Когда облака попадают в холодный воздух, маленькие капли воды
конденсируются и образуют дождь, снег или град.

Вода за пределами земли
Вода за пределами Земли на одних небесных телах находится в
твердом состоянии (лед), а на других как водяной пар. В виде льда, она была
обнаружена в кометах («грязные снежки»), на Марсе и на некоторых других внешних
планетах. Только кольца Сатурна содержат примерно в 20-30 раз больше воды, чем
Земля. Доказательства присутствия льда в метеоритных кратерах вблизи полюсов
можно найти даже на Меркурии, планете, ближайшей к Солнцу.
Биологическая роль
Вода является источником здоровой жизни и очень важна для
организма. Как часть крови, она снабжает нас кислородом и питательными
веществами. В то же время токсины транспортируются через кровоток в почки,
удаляются из организма. Вода регулирует температуру тела. Если температура
воздуха высокая, человек потеет, и тело охлаждается. Однако, если пот не
выделяется, то поднимается температура и самочувствие ухудшается.
Многие витамины, молекулы сахара могут использоваться
организмом только через воду. Органические вещества расщепляются в воде и
транспортируются к нужным органам. Кроме того, она является важным компонентом
клеток и тканей. Например, мозг на 90 % состоит из жидкости.
Применение
Вода используется во всех сферах жизни. Люди пьют ее,
готовят пищу, поливают растения. На гидроэлектростанциях вода используется, как
источник энергии. Она также необходима на фабриках, например, для производства
и переработки бумаги. Кстати, для производства одного листа бумаги требуется 10
литров воды! При тушении пожаров без нее не обойтись. Сельское хозяйство было
бы невозможно без Н2О.

Многие используют ее в качестве лекарства от разных
болезней. Особенно много целебных свойств, приписывают органической воде.
Исследования
Вода существует миллиарды лет, и, казалось бы, что о ней
знают все, но она все равно остается тайной. Создаются целые институты, которые
пытаются узнать, как сделать аналог воды, откуда она появилась на Земле и в
космосе. Они изучают ее влияние на жизнь, ландшафт, природу.
Происхождение воды на планете
Многих интересует, откуда все-таки взялась вода. Она
родилась четыре с половиной миллиарда лет назад в глубинах вселенной. Земля,
еще не полностью сформированная, состояла в основном из вулканов. Газы, богатые
водяным паром, выделялись в атмосферу, там образовывались облака. За
тысячелетия земля остыла, и пары, сгущаясь, падали обратно на земную кору в
виде дождя. Также формированию этого очень важного источника жизни,
способствовали падающие кометы, состоящие в основном изо льда и фрагментов
породы. Это явление способствовало образованию рек, озер и океанов, где
миллионы лет спустя появились бы первые формы жизни.
Гидрология
Понять, как вода взаимодействует с атмосферой, как влияет на
жизнедеятельность, помогает наука гидрология. Она изучает, какая вода находится
в водной оболочке Земли. Гидрология помогает понять, как рационально управлять
водными объектами. Она составляет прогнозы состояния водных ресурсов, и дает им
оценку.
Гидрогеология
Наука, которая изучает подземные воды, гидрогеохимию
называется гидрогеология. Гидрогеологи занимаются поиском новых подземных
водных источников, изучают, как сделать воду из подземных источников полезной
для мелиорации, водоснабжения, природного ландшафта. Данные полученные учеными
помогают снизить негативные влияния деятельности людей, на подземные водные
источники.
Теперь вы знаете всю правду о воде, и понимаете, насколько
важно бережно к ней относится. Ведь если пропадет вода, то не станет и нас.
Источник
СОДЕРЖАНИЕ:
- Строение молекулы воды
- Какие связи имеет H2O?
- Физические свойства H2O
- Химические свойства H2O
- Круговорот воды в природе
- Почему не кончается вода на Земле?
- Виды воды
СТРОЕНИЕ МОЛЕКУЛЫ ВОДЫ
Молекула представляет собой совокупность атомных ядер и электронов , что является достаточно устойчивым , чтобы обладать наблюдаемыми свойствами — и есть несколько молекул , которые являются более стабильными и трудно разлагаются , чем H 2 O.
В воде, каждое ядро водорода связаны с центральным атомом кислорода парой электронов, которые делятся между ними. Химики называют эту общую электронную пару ковалентной химической связью. В H 2О, только два из шести электронов кислорода внешней оболочки используются для этой цели, оставляя четыре электрона, которые организованы в две несвязывающие пары.
Четыре электронные пары, окружающие кислород, имеют тенденцию располагаться как можно дальше друг от друга, чтобы минимизировать отталкивания между этими облаками отрицательного заряда. Это обычно приводит к тетраэдрической геометрии, в которой угол между электронными парами (и, следовательно, угол связи HOH ) составляет 109,5 °.
Однако, поскольку две несвязывающие пары остаются ближе к атому кислорода, они оказывают более сильное отталкивание на две пары ковалентных связей, эффективно сближая два атома водорода. Результатом является искаженное тетраэдрическое расположение, в котором угол Н-О-Н составляет 104,5 °.
Хотя молекула воды не несет чистого электрического заряда, ее восемь электронов распределены неравномерно. Немного более отрицательный заряд (фиолетовый) на кислородном конце молекулы и компенсирующий положительный заряд (зеленый) на водородном конце. Получающаяся полярность в значительной степени ответственна за уникальные свойства воды.
Поскольку молекулы меньше световых волн, их нельзя наблюдать непосредственно, и их необходимо «визуализировать» альтернативными способами. Внешняя оболочка показывает эффективную «поверхность» молекулы, определяемую протяженностью облака отрицательного электрического заряда, созданного восемью электронами.
КАКИЕ СВЯЗИ ИМЕЕТ H2O2
Молекула H 2 O электрически нейтральна, но положительные и отрицательные заряды распределены неравномерно. Это иллюстрируется градацией цвета на схематической диаграмме здесь. Электронный (отрицательный) заряд концентрируется на кислородном конце молекулы, отчасти благодаря несвязывающимся электронам (сплошные синие кружки) и высокому заряду ядра кислорода, который оказывает сильное притяжение на электроны.
Это смещение заряда представляет собой электрический диполь , представленный стрелкой внизу; Вы можете думать об этом диполе как о электрическом «образе» молекулы воды.
Как все мы узнали в школе, противоположные заряды притягиваются, поэтому частично положительный атом водорода на одной молекуле воды электростатически притягивается к частично отрицательному кислороду на соседней молекуле. Этот процесс называется (несколько обманчиво) водородной связью.
Обратите внимание, что водородная связь длиннее, чем ковалентная связь О-Н. Это означает, что он значительно слабее. На самом деле он настолько слаб, что данная водородная связь не может существовать дольше, чем крошечная доля секунды.
ФИЗИЧЕСКИЕ СВОЙСТВА H2O2
Давно известно, что вода обладает многими физическими свойствами, которые отличают ее от других небольших молекул сопоставимой массы. Химики называют их «аномальными» свойствами воды, но они ни в коем случае не являются загадочными. Все они являются полностью предсказуемыми последствиями того, как размер и заряд ядра атома кислорода способствуют искажению облаков электронного заряда атомов других элементов, когда они химически связаны с кислородом. Вода является одним из немногих известных веществ, чья твердая форма менее плотная, чем жидкость.
Расширение между –4 ° и 0 ° обусловлено образованием более крупных агрегатов с водородными связями. Выше 4 ° начинается тепловое расширение, поскольку колебания связей О — Н становятся более энергичными, что приводит к выталкиванию молекул дальше друг от друга.
Другое широко цитируемое аномальное свойство воды — ее высокая температура кипения. Как показывает этот график, молекула, столь же легкая, как H 2 O, «должна» кипеть при температуре около –90 ° C. То есть, он существовал бы в мире в виде газа, а не жидкости, если бы не было водородных связей. Обратите внимание, что Н-связь также наблюдается с фтором и азотом.
ХИМИЧЕСКИЕ СВОЙСТВА H2O2
Соленость воды может быть определена как концентрация всех катионов, в значительной степени Na + , K + , Mg ++ и Ca ++, а также анионов CO 3 = и SO 4 = и галогенидов, причем все HCO 3 — превращаются в CO = 3. Приведенный выше средний состав пресной воды соответствует среднему речному водоснабжению. В мягких водах Ca ++ и CO = 3 могут быть значительно снижены. В кислых водах сульфат может быть доминирующим.
КРУГОВОРОТ ВОДЫ В ПРИРОДЕ
Что происходит в естественном круговороте воды?
В естественном круговороте воды используются физические процессы для перемещения воды с поверхности земли в атмосферу и обратно.
Испарение — это когда солнце светит на воду и нагревает ее, превращая в газ, называемый водяным паром, который поднимается в воздух.
Транспирация — это когда солнце согревает людей, растения и животных, и они выпускают водяной пар в воздух.
Конденсация — это когда водяной пар в воздухе охлаждается и превращается в жидкость, образуя крошечные капельки воды в небе.
Осадки — это когда капли воды падают с неба в виде дождя, снега или града.
Сток — это когда вода течет по земле и впадает в ручьи, реки и океаны.
Инфильтрация — это когда вода падает на землю и впитывается в почву.
Перколяция — это когда вода все глубже проникает в крошечные места в почве и камне.
ПОЧЕМУ НЕ КОНЧАЕТСЯ ВОДА НА ЗЕМЛЕ
Земля содержит огромное количество воды:
- в океанах;
- озерах;
- реках;
- атмосфере;
- в скалах внутренней Земли.
В течение миллионов лет большая часть этой воды рециркулируется между внутренней Землей, океанами и реками и атмосферой. Этот циклический процесс означает, что пресная вода постоянно поступает на поверхность Земли, где мы все живем.
Вулканы выпускают огромное количество воды из внутренней Земли в атмосферу.
Наша планета также очень эффективно удерживает эту воду. Вода, будучи паром в нашей атмосфере, потенциально может сбежать в космос с Земли. Но вода не вытекает, потому что некоторые области атмосферы очень холодные. (Например, на высоте 15 километров температура атмосферы составляет всего -60 ° С!). При этой холодной температуре вода образует твердые кристаллы, которые падают обратно на поверхность Земли.
Хотя на нашей планете в целом никогда не кончится вода, важно помнить, что чистая пресная вода не всегда доступна там, где и когда она нужна людям. Фактически, половина пресной воды в мире может быть найдена только в шести странах. Более миллиарда человек живут без достаточного количества чистой воды.
Кроме того, каждая капля воды, которую мы используем, продолжается в круговороте воды. Вещи, которые мы кладем в канализацию, попадают в чью-то воду. Мы можем помочь защитить качество пресной воды на нашей планете, используя ее более разумно.
ВИДЫ ВОДЫ
«Чистая вода»
Для химика термин «чистый» имеет значение только в контексте конкретного применения или процесса. Дистиллированная или деионизированная вода, которую мы используем в лаборатории, содержит растворенные атмосферные газы и иногда немного кремнезема, но их небольшое количество и относительная инертность делают эти примеси незначительными для большинства целей.
Когда для определенных типов точных измерений требуется вода с наивысшей достижимой чистотой, ее обычно фильтруют, деионизируют и подвергают тройной вакуумной дистилляции. Но даже эта «химически чистая» вода представляет собой смесь изотопных частиц: есть два стабильных изотопа водорода (H 1 и H 2 , последний часто обозначается как D) и кислорода (O 16 и O 18 ), которые вызывают комбинации, такие как H 2O 18 , HDO 16 и т. Д. Они легко идентифицируются в инфракрасных спектрах водяного пара.
И вдобавок ко всему, два атома водорода в воде содержат протоны, магнитные моменты которых могут быть параллельными или антипараллельными, что приводит к орто- и пара- воде соответственно. Две формы обычно присутствуют в соотношении о / п 3: 1.
Количество редких изотопов кислорода и водорода в воде достаточно разнится от места к месту, поэтому теперь можно с некоторой точностью определить возраст и источник конкретного образца воды. Эти различия отражены в изотопных профилях H и O организмов. Таким образом, изотопный анализ волос человека может быть полезным инструментом для расследования преступлений и антропологических исследований.
Питьевая вода
Наша обычная питьевая вода, напротив, никогда не бывает химически чистой, особенно если она контактировала с отложениями. Подземные воды (из родников или колодцев) всегда содержат ионы кальция и магния, а также часто железо и марганец; положительные заряды этих ионов уравновешиваются отрицательными ионами карбонат / бикарбонат, а иногда и некоторым количеством хлорида и сульфата. В некоторых регионах подземные воды содержат недопустимо высокие концентрации естественных токсичных элементов, таких как селен и мышьяк.
Можно подумать, что дождь или снег будут освобождены от загрязнения, но когда водяной пар конденсируется из атмосферы, это всегда происходит на частице пыли, которая выделяет вещества в воду, и даже самый чистый воздух содержит углекислый газ, который растворяется с образованием углекислота За исключением сильно загрязненных атмосфер, примеси, улавливаемые снегом и дождем, слишком малы, чтобы вызывать беспокойство.
Различные правительства установили верхние пределы количества загрязняющих веществ, допустимых в питьевой воде; самые известные из них — Стандарты питьевой воды EPA США.
Безионная вода
Иногда можно услышать, что не содержащая минералов вода и особенно дистиллированная вода вредны для здоровья, потому что они «вымывают» необходимые минералы из организма. Дело в том, что минеральные ионы не проходят через клеточные стенки при обычной осмотической диффузии, а скорее переносятся метаболическими процессами.
Обширное исследование 2008 года не подтвердило более ранние сообщения о том, что низкий уровень кальция / магния в питьевой воде коррелирует с сердечно-сосудистыми заболеваниями. Любая сбалансированная диета должна содержать все необходимые нам минеральные вещества.
Хорошо известно, что люди, которые занимаются тяжелой физической активностью или находятся в очень жаркой среде, должны избегать употребления большого количества даже обычной воды. Чтобы предотвратить серьезные проблемы с электролитным дисбалансом, необходимо компенсировать потери солей при потливости. Это может быть достигнуто путем приема соленых продуктов или напитков (включая «спортивные напитки») или соленых таблеток.
Статью проверил и отредактировал Papa Vlada.
Первоисточник статьи опубликован на сайте про воду.
Источник
