Каким свойством обладают газы

Физические законы и параметры газов являются основополагающими для создания вакуумных систем. Даже при крайне низких значениях давлений, используемых в вакуумной технике, физические процессы, протекающие в газах, подчиняются общим газовым законам. Необходимость создания вакуума обычно связана с потребностью уменьшения концентрации молекул газа или частоты их столкновений с поверхностью сосуда. Газовые процессы в вакуумных системах можно, как правило, рассматривать с точки зрения законов идеального газа, а некоторые общие физические процессы вакуумных систем могут быть описаны с помощью статических и динамических свойств газов. Физические процессы, протекающие в газах при низком давлении, а также различные параметры и свойства газового потока рассмотрены ниже.
Параметры состояния газа
Если взять образец газа, то для описания его состояния достаточно знать три из четырех параметров. Этими параметрами являются давление, объем, температура и количество газа.
Давление – это сила, с которой газ воздействует на единицу площади поверхности сосуда. В СИ единицей измерения давления является паскаль, или ньютон на квадратный метр (Н/м2). В вакуумной технике также используется единица измерения миллиметр ртутного столба, или Торр: 1 мм рт. ст. = 133 Па (1 Па = 7,5 мм рт. ст.).
Объем – мера пространства, которое занимает газ; обычно он задается размерами сосуда. Единицей объема в СИ является кубический метр (м3), однако для обозначения быстроты откачки и потока газа, а также других величин широко используются литры.
Температура газа при давлении ниже 1 Торр главным образом определяется температурой поверхностей, с которыми он соприкасается. Как правило, газ находится при комнатной температуре. При выводе уравнений, описывающих состояние газов, для измерения температуры используют Кельвины (К).
Количество газа в данном объеме измеряется в молях.
Моль – число граммов газа (или любого вещества), равное его молекулярной массе. Моль содержит 6,02 х 1023 молекул. Один моль любого газа при 0 °С и давлении 760 Торр занимает объем, равный 22,4 л. Масса 1 моля газа равна его молекулярной массе в граммах.
Молярный объем является универсальной постоянной. Экспериментально установлено, что он составляет 22,414 л при 760 Торр и 0 °С. Поскольку 1 моль любого газа при температуре 0 °С и давлении 760 Торр занимает объем 22,4 л, из этого соотношения можно рассчитать молекулярную концентрацию любого объема газа, если известны его температура и давление. Например, 1 см3 воздуха при 760 Торр и 0 °С содержит 2,7 x 1019 молекул; в то время как при давлении 1 Торр и температуре 0 °С 1 см3 воздуха содержит 3,54 x 1016 молекул.
Газовые законы
Газовые законы устанавливают соотношения между физическими параметрами состояния газа (давление, объем, температура и количество газа) при постоянном значении одного из параметров. Эти законы справедливы для идеального газа в котором объем всех молекул является незначительным по сравнению с объемом газа, и энергия притяжения между молекулами является незначительной по сравнению с их средней тепловой энергией. Это означает, что данное вещество (в данном случае газ) находится в газообразном состоянии при температуре, которая достаточно высока для его конденсации. К газам, по своим свойствам близким к идеальным при комнатной температуре, относятся 02, Ne, Аг, СО, Н2 и NO.
Ниже приведены общие формулировки газовых законов.
Закон Бойля – произведение давления на объем рУ, где р – давление газа, V – его объем, является постоянной величиной для данной массы газа при постоянной температуре.
Закон Гей-Люссака – величина V/T, где Т- абсолютная температура газа, является постоянной для данной массы газа при постоянном давлении.
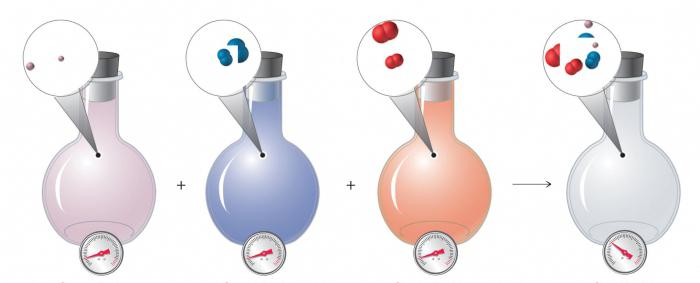
Закон Авогадро – равные объемы различных газов при одинаковых температуре и давлении содержат одно и то же количество молекул. Из этого закона можно получить важное соотношение между числом молей газа и давлением, которое создает газ.
Основное уравнение состояния идеального газа (уравнение Клапейрона) устанавливает зависимость между давлением, объемом и температурой для данной массы газа, т. е. теми параметрами, которые необходимы для описания состояния газа:
$$pV=MRT, (1.1)$$
где R – универсальная газовая постоянная данного газа, R = 8,31 ДжДмоль К) (62,4 Торр-л/(моль x К)); М – это число молей в объеме V
Данный закон будет справедлив и для большинства газов, которые при низких давлениях ведут себя как идеальные газы.
Закон парциальных давлений Дальтона – общее давление, создаваемое смесью газов, равняется сумме парциальных давлений, создаваемых отдельными компонентами смеси.
Парциальное давление, создаваемое одним компонентом смеси газов, – это давление, создаваемое этим компонентом, если бы он занимал весь объем.
Закон Авогадро – равные объемы идеального газа при постоянных температуре и давлении содержат одно и то же количество молекул.
Число Авогадро – число молекул в 1 моле газа или любого вещества, является универсальной постоянной и составляет 6,023 • 1023.
Число Лошмидта – число молекул в кубическом сантиметре газа при атмосферном давлении и температуре 0 °С. Это универсальная постоянная, равная 2,637 x 1019.
Для 1 моля газа при атмосферном давлении и температуре 0 °С (273,2 К), занимающего объем V = 22,414 л, R= 8.31 Дж/(моль x К) или в тепловых единицах R/J= 1,99 кал/К (У – механический эквивалент теплоты, J = 4,182 Дж кал). Следовательно, количество теплоты 1,99 кал будет повышать температуру 1 моля любого идеального газа на 1 К, или после повышения температуры 1 моля любого идеального газа на 1 К увеличение энергии газа составит 8,31 Дж.
Неидеальные газы
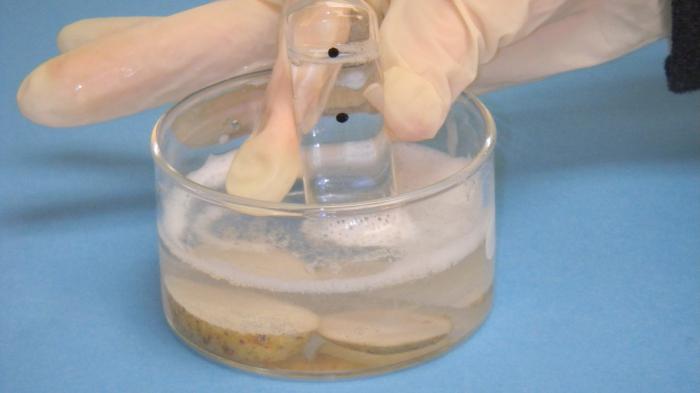
Примерами некоторых распространенных неидеальных газов являются аммиак, этан, бензол, диоксид углерода (углекислый газ), пары ртути, SO и S02. Газовые законы должны описывать физические процессы, протекающие в любом газе при температуре выше критической. При критической температуре, Тс, газ начинает конденсироваться. Ниже этой критической температуры имеет место давление паров над жидким конденсатом, которое называется давлением пара. Если газ конденсируется (его объем уменьшается), давление изменяться не будет, но большее количество газа будет переходить в жидкую фазу. По мере снижения температуры над жидкостью будет присутствовать меньшее количество молекул, при этом давление паров также будет снижаться.
Источник
Есть вопросы? Пожалуйста, задавайте их в нашей группе Вконтакте, чтобы их смогли прочитать другие покупатели. Оперативный и подробный ответ гарантируем!
| В газообразном виде все тела получают особые свойства, а именно: ближе всего они обладают в высшей степени упругостью, т.е. под сильным давлением способны сжиматься до плотности жидкого, а порой даже твёрдого тела; но, уступая давлению, газы вследствие той же упругости сохраняют в соответствующей степени способность отпора, так что, будучи сдавленными или сжатыми, они стремятся расшириться до полного равновесия с атмосферным воздухом. Это стремление, основанное на взаимном отталкивании однородных частиц, до того развито в газах, что если бы на безвоздушную луну метнуть шар, наполненный воздухом, то шар этот, конечно, лопнул бы от силы внутреннего напора, а содержащийся в нем воздух равномерно облек бы всю поверхность луны. Поэтому воздушный шар, дойдя до известной высоты, должен либо остановиться, либо выпустить часть газа, либо лопнуть. Другая особенность газов заключается в том, что они занимают значительно больше места, чем тот материал, из которого они образовались. Так, например, кубический дюйм пороха превращается в 288 кубических дюймов газа. Если газы образуются медленно и при этом могут постепенно уходить в атмосферу, то сам акт появления их не окажет никакого особого действия: они расплывутся в пространстве. Если же образование этих газов последует очень быстро, но всё-таки на свободе, то получится только вспышка, т.е. мгновенное появление огня, сопровождаемое слабым шумом. Например, если спалить клочок пироксилина на открытой ладони, горсть пороха на камне, кучку бертолетовой соли с магнием или смесь 1 части алюминиевого порошка с 2 частями марганцовокислого калия. В иных случаях даже при таких обстоятельствах получается «хлопок», т.е. порывистый звук, образовавшийся от внезапного и сильного колебания воздушных волн (например, от взрыва щепотки гремучей ртути). Но если взрывчатый состав помещается в сжатом пространстве и окружен плотной оградой или стеной, то сдавленные газы стремятся расширить свой объём и, напирая изнутри, проявляют давление, пропорциональное их количеству в сравнении с занимаемым ими местом. Подобное явление больше всего замечается у огнестрельных орудий: в момент своего образования пороховые газы имеют плотность, почти равную плотности заряда, т.е. занимают место, в 288 раз меньшее по природному объёму. Вследствие этого газы напирают на стены, на казенник (заднюю часть орудия) и на дно снаряда (ядра), но, встречая в стенах и казеннике сопротивление, достаточное, чтобы выдержать напор, газы эти со всей силой напирают на ядро или пулю, которые буквально выдуваются или выталкиваются («выбрасываются») в данном направлении.
Огнестрельное орудие времен Гражданской войны в США Следовательно, сила «взрыва», т.е. мгновенного превращения твёрдого вещества в газообразное или густого газа в менее плотный, зависит, во-первых, от количества газов в сравнении с занимаемым ими местом, а во-вторых, от одновременности их появления, т.е. в данном случае – от быстроты сгорания состава. Третье – весьма существенное – условие заключается в том, чтобы как можно больше состава сгорало, т.е. как можно меньше получалось бы остатков и дыма. Но газы обладают ещё одним свойством, играющим крайне важную роль по отношению к взрыву: сила их напора возвышается с температурой, т.е. одно и то же количество газов, находящееся при одинаковых условиях помещения, получает значительно большую силу напора при повышении коэффициента теплоты. Так, например, порох, хорошо приготовленный и сгорающий почти мгновенно, даёт по объёму всего 288 кратных газа, но вследствие высокого нагревания (Ueberheizung surchauffe) напор этих газов превышает более 2000 раз атмосферное давление. Сухой пироксилин при тех же условиях развивает втрое большую силу. Давление это можно ещё значительно усилить, ускорив горение и именно посредством примеси какого-нибудь быстро воспламеняющегося тела к составу, горящему более медленно; если, например, порох взорвать посредством небольшого количества нитроглицерина, воспламененного гремучей ртутью, то давление происходит в 4 раза более сильное (т.е. в 8000 атмосфер, вместо 2000); а если посредством гремучей ртути взорвать сухой пироксилин, то давление в сравнении с порохом будет шестикратное (т.е. 12000 атмосфер). О механической работе пороха будет упомянуто в свое время. Сила напора, как уже сказано, всецело зависит от степени сжатия газов, но действие этого напора, т.е. направление его силы, находится в связи с быстротой горения веществ: если вещество сгорает постепенно (как, например, порох), то давление больше всего сосредоточивается на том месте окружающей среды, которое представляет наименьшее сопротивление. Порох выбрасывает пулю или бомбу, но разрывает орудие только в особых случаях. Если же горение происходит сразу, безо всякой последовательности, то газы напирают во все стороны. В первом случае действие называется «метательным» (Schleuderkraft), а во втором – «дробящим» (Brisanz). Метательные вещества употребляются для стрельбы, а дробящие – для взрывов. Выше было сказано, что газы, высвободившись из тесноты, сообщают наружному воздуху толчок, производящий колебание воздушных волн. От этого колебания получается звук, называемый «ударом», или «шлагом» (детонацией – Schlag, detonation). Его сила («интенсивность») зависит не столько от количества газов, сколько от степени внутреннего напора, так что сильный удар можно произвести сравнительно малыми средствами. Вещества или тела, простые или составные, способные при известных условиях (вследствие развития тепла от зажигания или от удара) быстро разлагаться, превращаясь в то же время почти наполовину (по весу, конечно) в сильно нагретые газы, производят взрыв, а потому и называются «взрывчатыми» (Explosivstoffe); так, например, порох превращается в размере 40 % (по весу) в газы, а остальные 60 % либо образуют твёрдый остаток, либо улетучиваются в виде дыма. При неблагоприятных условиях имеется ещё и третья потеря: слишком быстрое воспламенение выбрасывает значительную часть несгоревшего заряда. В противоположность к взрывчатым веществам имеются такие смеси и составы, которые не обладают особой способностью быстро превращаться в газы, но зато горят ярким, либо белым, либо цветным пламенем. Т.к. подобные огни не обнаруживают сильного напора, а горят тихо, без детонации, то их вообще называют пассивными (faules Feuer), а Детонирующие смеси – активными (Treib-feuer); первые употребляются для световых эффектов, вторые – для силовых. Помимо этого, состав может быть пламенным, искристым или ударным. Ударный производит только шлаг; пламенный даёт лишь пламя, искристый выкидывает раскаленные частицы, не составляющие элемента горения. Такие частицы либо сгорают в воздухе, либо тухнут (охлаждаются) в нём. Из этих трёх данных образуются сложные огни, т.е. такие, которые обладают двумя или всеми тремя упомянутыми свойствами: и светят, и искрятся, и дают шлаги. Правильная комбинация этих эффектов за- висит от точного знания свойств ингредиентов и от правильного дозирования смесей. Эта-то часть, называемая «пиротехнической химией», и составляет главнейшую суть всего фейерверочного дела, и чем меньше она основана на эмпирике, т.е. на опыте, слепо идущем наобум, ощупью, без сознательного понимания действия и причин, тем работа выйдет лучше и удачнее. Но до того, чтобы перейти к «синтезу» составов, т.е. к теории образования горючих смесей, необходимо предварительно ознакомиться с материалом, входящим в состав этих смесей; иначе придётся трактовать о неизвестных величинах, а это на практике почти всегда равносильно толчению воды в ступе. |
Источник
На сегодняшний день известно о существовании более чем 3 миллионов различных веществ. И цифра эта с каждым годом растет, так как химиками-синтетиками и другими учеными постоянно производятся опыты по получению новых соединений, обладающих какими-либо полезными свойствами.
Часть веществ – это природные обитатели, формирующиеся естественным путем. Другая половина – искусственные и синтетические. Однако и в первом и во втором случае значительную часть составляют газообразные вещества, примеры и характеристики которых мы и рассмотрим в данной статье.

Агрегатные состояния веществ
С XVII века принято было считать, что все известные соединения способны существовать в трех агрегатных состояниях: твердые, жидкие, газообразные вещества. Однако тщательные исследования последних десятилетий в области астрономии, физики, химии, космической биологии и прочих наук доказали, что есть еще одна форма. Это плазма.
Что она собой представляет? Это частично или полностью ионизированные газы. И оказывается, таких веществ во Вселенной подавляющее большинство. Так, именно в состоянии плазмы находятся:
- межзвездное вещество;
- космическая материя;
- высшие слои атмосферы;
- туманности;
- состав многих планет;
- звезды.
Поэтому сегодня говорят, что существуют твердые, жидкие, газообразные вещества и плазма. Кстати, каждый газ можно искусственно перевести в такое состояние, если подвергнуть его ионизации, то есть заставить превратиться в ионы.
Газообразные вещества: примеры
Примеров рассматриваемых веществ можно привести массу. Ведь газы известны еще с XVII века, когда ван Гельмонт, естествоиспытатель, впервые получил углекислый газ и стал исследовать его свойства. Кстати, название этой группе соединений также дал он, так как, по его мнению, газы – это нечто неупорядоченное, хаотичное, связанное с духами и чем-то невидимым, но ощутимым. Такое имя прижилось и в России.
Можно классифицировать все газообразные вещества, примеры тогда привести будет легче. Ведь охватить все многообразие сложно.
По составу различают:
- простые,
- сложные молекулы.
К первой группе относятся те, что состоят из одинаковых атомов в любом их количестве. Пример: кислород – О2, озон – О3, водород – Н2, хлор – CL2, фтор – F2, азот – N2 и прочие.
Ко второй категории следует относить такие соединения, в состав которых входит несколько атомов. Это и будут газообразные сложные вещества. Примерами служат:
- сероводород – H2S;
- хлороводород – HCL;
- метан – CH4;
- сернистый газ – SO2;
- бурый газ – NO2;
- фреон – CF2CL2;
- аммиак – NH3 и прочие.
Классификация по природе веществ
Также можно классифицировать виды газообразных веществ по принадлежности к органическому и неорганическому миру. То есть по природе входящих в состав атомов. Органическими газами являются:
- первые пять представителей предельных углеводородов (метан, этан, пропан, бутан, пентан). Общая формула CnH2n+2;
- этилен – С2Н4;
- ацетилен или этин – С2Н2;
- метиламин – CH3NH2 и другие.
К категории газов неорганической природы относятся хлор, фтор, аммиак, угарный газ, силан, веселящий газ, инертные или благородные газы и прочие.
Еще одной классификацией, которой можно подвергнуть рассматриваемые соединения, является деление на основе входящих в состав частиц. Именно из атомов состоят не все газообразные вещества. Примеры структур, в которых присутствуют ионы, молекулы, фотоны, электроны, броуновские частицы, плазма, также относятся к соединениям в таком агрегатном состоянии.
Свойства газов
Характеристики веществ в рассматриваемом состоянии отличаются от таковых для твердых или жидких соединений. Все дело в том, что свойства газообразных веществ особенные. Частицы их легко и быстро подвижны, вещество в целом изотропное, то есть свойства не определяются направлением движения входящих в состав структур.
Можно обозначить самые главные физические свойства газообразных веществ, которые и будут отличать их от всех остальных форм существования материи.
- Это такие соединения, которые нельзя увидеть и проконтролировать, ощутить обычными человеческими способами. Чтобы понять свойства и идентифицировать тот или иной газ, опираются на четыре описывающих их все параметра: давление, температура, количество вещества (моль), объем.
- В отличие от жидкостей газы способны занимать все пространство без остатка, ограничиваясь лишь величиной сосуда или помещения.
- Все газы между собой легко смешиваются, при этом у этих соединений нет поверхности раздела.
- Существуют более легкие и тяжелые представители, поэтому под действием силы тяжести и времени, возможно увидеть их разделение.
- Диффузия – одно из важнейших свойств этих соединений. Способность проникать в другие вещества и насыщать их изнутри, совершая при этом совершенно неупорядоченные движения внутри своей структуры.
- Реальные газы электрический ток проводить не могут, однако если говорить о разреженных и ионизированный субстанциях, то проводимость резко возрастает.
- Теплоемкость и теплопроводность газов невысока и колеблется у разных видов.
- Вязкость возрастает с увеличением давления и температуры.
- Существует два варианта межфазового перехода: испарение – жидкость превращается в пар, сублимация – твердое вещество, минуя жидкое, становится газообразным.
Отличительная особенность паров от истинных газов в том, что первые при определенных условиях способны перейти в жидкость или твердую фазу, а вторые нет. Также следует заметить способность рассматриваемых соединений сопротивляться деформациям и быть текучими.

Подобные свойства газообразных веществ позволяют широко применять их в самых различных областях науки и техники, промышленности и народном хозяйстве. К тому же конкретные характеристики являются для каждого представителя строго индивидуальными. Мы же рассмотрели лишь общие для всех реальных структур особенности.
Сжимаемость
При разных температурах, а также под влиянием давления газы способны сжиматься, увеличивая свою концентрацию и снижая занимаемый объем. При повышенных температурах они расширяются, при низких – сжимаются.
Под действием давления также происходят изменения. Плотность газообразных веществ увеличивается и, при достижении критической точки, которая для каждого представителя своя, может наступить переход в другое агрегатное состояние.
Основные ученые, внесшие вклад в развитие учения о газах
Таких людей можно назвать множество, ведь изучение газов – процесс трудоемкий и исторически долгий. Остановимся на самых известных личностях, сумевших сделать наиболее значимые открытия.
- Амедео Авогадро в 1811 году сделал открытие. Неважно, какие газы, главное, что при одинаковых условиях их в одном объеме их содержится равное количество по числу молекул. Существует рассчитанная величина, имеющая название по фамилии ученого. Она равна 6,03*1023 молекул для 1 моль любого газа.
- Ферми – создал учение об идеальном квантовом газе.
- Гей-Люссак, Бойль-Мариотт – фамилии ученых, создавших основные кинетические уравнения для расчетов.
- Роберт Бойль.
- Джон Дальтон.
- Жак Шарль и многие другие ученые.
Строение газообразных веществ
Самая главная особенность в построении кристаллической решетки рассматриваемых веществ, это то, что в узлах ее либо атомы, либо молекулы, которые соединяются друг с другом слабыми ковалентными связями. Также присутствуют силы ван-дер-ваальсового взаимодействия, когда речь идет о ионах, электронах и других квантовых системах.
Поэтому основные типы строения решеток для газов, это:
- атомная;
- молекулярная.
Связи внутри легко рвутся, поэтому эти соединения не имеют постоянной формы, а заполняют весь пространственный объем. Это же объясняет отсутствие электропроводности и плохую теплопроводность. А вот теплоизоляция у газов хорошая, ведь, благодаря диффузии, они способны проникать в твердые тела и занимать свободные кластерные пространства внутри них. Воздух при этом не пропускается, тепло удерживается. На этом основано применение газов и твердых тел в совокупности в строительных целях.

Простые вещества среди газов
Какие по строению и структуре газы относятся к данной категории, мы уже оговаривали выше. Это те, что состоят из одинаковых атомов. Примеров можно привести много, ведь значительная часть неметаллов из всей периодической системы при обычных условиях существует именно в таком агрегатном состоянии. Например:
- фосфор белый – одна из аллотропных модификаций данного элемента;
- азот;
- кислород;
- фтор;
- хлор;
- гелий;
- неон;
- аргон;
- криптон;
- ксенон.
Молекулы этих газов могут быть как одноатомными (благородные газы), так и многоатомными (озон – О3). Тип связи – ковалентная неполярная, в большинстве случаев достаточно слабая, но не у всех. Кристаллическая решетка молекулярного типа, что позволяет этим веществам легко переходить из одного агрегатного состояния в другое. Так, например, йод при обычных условиях – темно-фиолетовые кристаллы с металлическим блеском. Однако при нагревании сублимируются в клубы ярко-фиолетового газа – I2.

К слову сказать, любое вещество, в том числе металлы, при определенных условиях могут существовать в газообразном состоянии.
Сложные соединения газообразной природы
Таких газов, конечно, большинство. Различные сочетания атомов в молекулах, объединенные ковалентными связями и ван-дер-ваальсовыми взаимодействиями, позволяют сформироваться сотням различных представителей рассматриваемого агрегатного состояния.
Примерами именно сложных веществ среди газов могут быть все соединения, состоящие из двух и более разных элементов. Сюда можно отнести:
- пропан;
- бутан;
- ацетилен;
- аммиак;
- силан;
- фосфин;
- метан;
- сероуглерод;
- сернистый газ;
- бурый газ;
- фреон;
- этилен и прочие.
Кристаллическая решетка молекулярного типа. Многие из представителей легко растворяются в воде, образуя соответствующие кислоты. Большая часть подобных соединений – важная часть химических синтезов, осуществляемых в промышленности.
Метан и его гомологи
Иногда общим понятием “газ” обозначают природное полезное ископаемое, которое представляет собой целую смесь газообразных продуктов преимущественно органической природы. Именно он содержит такие вещества, как:
- метан;
- этан;
- пропан;
- бутан;
- этилен;
- ацетилен;
- пентан и некоторые другие.
В промышленности они являются очень важными, ведь именно пропан-бутановая смесь – это бытовой газ, на котором люди готовят пищу, который используется в качестве источника энергии и тепла.

Многие из них используются для синтеза спиртов, альдегидов, кислот и прочих органических веществ. Ежегодное потребление природного газа исчисляется триллионами кубометров, и это вполне оправданно.
Кислород и углекислый газ
Какие вещества газообразные можно назвать самыми широко распространенными и известными даже первоклассникам? Ответ очевиден – кислород и углекислый газ. Ведь это они являются непосредственными участниками газообмена, происходящего у всех живых существ на планете.
Известно, что именно благодаря кислороду возможна жизнь, так как без него способны существовать только некоторые виды анаэробных бактерий. А углекислый газ – необходимый продукт “питания” для всех растений, которые поглощают его с целью осуществления процесса фотосинтеза.
С химической точки зрения и кислород, и углекислый газ – важные вещества для проведения синтезов соединений. Первый является сильным окислителем, второй чаще восстановитель.
Галогены
Это такая группа соединений, в которых атомы – это частицы газообразного вещества, соединенные попарно между собой за счет ковалентной неполярной связи. Однако не все галогены – газы. Бром – это жидкость при обычных условиях, а йод – легко возгоняющееся твердое вещество. Фтор и хлор – ядовитые опасные для здоровья живых существ вещества, которые являются сильнейшими окислителями и используются в синтезах очень широко.
Источник

