Какими химическими свойствами обладает se

Сера,
её физические и химические свойства. Биологическое значение серы, её применение
(демеркуризация).СЕРА S
Cера в природе
Самородная сера
Сульфиды
PbS – свинцовый блеск
Cu2S – медный блеск
ZnS – цинковая обманка
FeS2 – пирит, серный колчедан, кошачье золото
H2S – сероводород (в минеральных источниках и природном газе)
Белки
Сульфаты
CaSO4 * 2H2O – гипс
MgSO4 * 7H2O – горькая соль (английская)
Na2SO4 *10H2O – глауберова соль (мирабилит)
Физические свойства
Твердое кристаллическое вещество желтого цвета, нерастворима в воде, водой не смачивается (плавает на поверхности), t°кип = 445°С.
Одно из особенных физических свойств серы – флотация, способность мелкого порошка серы всплывать, тогда, как ее крупные кристаллы тонут в воде. Дело в том, что сера не смачивается водой, и ее частички держатся на поверхности воды за счет прилипших к ним мелких пузырьков воздуха. Это свойство используют при отделении самородной серы от примесей. Руду размалывают, заливают водой, а снизу продувают воздухом, сера всплывает, а примеси остаются на дне.
Аллотропия
Для серы характерны несколько аллотропных модификаций, но наиболее известные видоизменения: ромбическая (кристаллическая), моноклинная (игольчатая) и пластическая.
Ромбическая (a – сера) – S8
t°пл. = 113°C; ρ = 2,07 г/см3. Наиболее устойчивая модификация.
Моноклинная (b – сера) – S8
темно-желтые иглы, t°пл. = 119°C; ρ = 1,96 г/см3. Устойчивая при температуре более 96°С; при обычных условиях превращается в ромбическую.
Пластическая Sn
коричневая резиноподобная (аморфная) масса. Неустойчива, при затвердевании превращается в ромбическую.
ПОЛУЧЕНИЕ ПЛАСТИЧЕСКОЙ СЕРЫ
Взаимопревращение аллотропных модификаций серы
Строение атома серы
Размещение электронов по уровням и подуровням
Основное состояние
1s22s22p63s23p4
Размещение электронов по
орбиталям (последний слой)Степень
окисленияВалентность
-2
В основном состоянии
II
+4
Первое возбуждённое состояние
IV
+6
Второе возбуждённое состояние
VI
Получение серы
1. Промышленный метод – выплавление из руды с помощью водяного пара.
2. Неполное окисление сероводорода (при недостатке кислорода).
2H2S + O2 = 2S + 2H2O
3. Реакция Вакенродера
2H2S + SO2 = 3S + 2H2O
Химические свойства серы
Сера – окислитель S0 + 2ē→ S-2 | Сера – восстановитель: S – 4ē → S+4; S – 6ē →S+6 |
1. Взаимодействие серы со всеми щелочными и щелочноземельными металлами, медью, ртутью, серебром без нагревания: 2Na + S → Na2S ОПЫТ S + Hg = HgS Ртуть обладает высокой летучестью. Её пары ядовиты. Эта реакция лежит в основе удаления и обезвреживания ртути, например из разбитого медицинского термометра. Места, из которых нельзя извлечь капельки ртути, засыпают порошком серы. Сера и ртуть вступают в реакцию при соприкосновении. В результате образуется химически инертное и безвредное вещество. Этот процесс называется демеркуризацией 2. Взаимодействие серы c остальными металлами (кроме Au,Pt) при повышенной t°: 2Al + 3S t→ Al2S3 Zn + S t°→ ZnS ОПЫТ Cu + S t→ CuS ОПЫТ 3.Взаимодействие серы с некоторыми неметаллами с образованием бинарных соединений: H2 + S → H2S 2P + 3S→ P2S3 C + 2S → CS2 | 1. Взаимодействие серы c кислородом: S + O2 t°→ S+4O2 2S + 3O2 t°;pt→ 2S+6O3 2. Взаимодействие серы c галогенами (кроме йода): S + Cl2 → S+2Cl2 **Взаимодействие серы с кислотами – окислителями: S + 2H2SO4(конц) → 3S+4O2 + 2H2O S + 6HNO3(конц) → H2S+6O4 + 6NO2 + 2H2O **Реакции диспропорционирования: 4. 3S0 + 6KOH→ K2S+4O3 + 2K2S-2 + 3H2O |
Тренажёр №1 – Характеристика серы по её положению в периодической системе Д. И. Менделеева
Тренажёр №2 – Химические свойства серы
Тренажёр №3 – Взаимодействие серы с металлами
Применение
Вулканизация каучука, получение эбонита, производство спичек, пороха, в борьбе с вредителями сельского хозяйства, для медицинских целей (серные мази для лечения кожных заболеваний), для получения серной кислоты и т.д.
Применение серы и её соединений
Домашнее задание параграф 21; упражнения 1, 3, 4 стр. 99-100.
Дополнительные зхадания
Закончите уравнения реакций, расставьте коэффициенты методом электронного баланса, укажите окислитель, восстановитель.
- S + O2
- S + Na
- S + H2
№2. Осуществите превращения по схеме:
Это интересно…
- Содержание серы в организме человека массой 70 кг – 140 г.
- В сутки человеку необходимо 1 г серы.
- Серой богаты горох, фасоль, овсяные хлопья, пшеница, мясо, рыба, плоды и сок манго.
- Сера входит в состав гормонов, витаминов, белков, она есть в хрящевой ткани, в волосах, ногтях. При недостатке серы в организме наблюдается хрупкость ногтей и костей, выпадение волос.
Следите за своим здоровьем!
Знаете ли вы..
- Соединения серы могут служить лекарственными препаратами;
- Сера – основа мази для лечения грибковых заболеваний кожи, для борьбы с чесоткой. Тиосульфат натрия Na2S2O3 используется для борьбы с нею.
- Многие соли серной кислоты содержат кристаллизационную воду: ZnSO4×7H2O и CuSO4×5H2O. Их применяют как антисептические средства для опрыскивания растений и протравливания зерна в борьбе с вредителями сельского хозяйства.
- Железный купорос FeSO4×7H2O используют при анемии.
- BaSO4 применяют при рентгенографическом исследовании желудка и кишечника.
- Алюмокалиевые квасцы KAI(SO4)2×12H2O – кровоостанавливающее средство при порезах.
- Минерал Na2SO4×10H2O носит название «глауберова соль» в честь открывшего его в VIII веке немецкого химика Глаубера И.Р.Глаубер во время своего путешествия внезапно заболел. Он ничего не мог есть, желудок отказывался принимать пищу. Один из местных жителей направил его к источнику. Как только он выпил горькую соленую воду, сразу стал есть. Глаубер исследовал эту воду, из нее выкристаллизовалась соль Na2SO4×10H2O. Сейчас ее применяют как слабительное в медицине, при окраске хлопчато- бумажных тканей. Соль также находит применение в производстве стекла.
- Тысячелистник обладает повышенной способностью извлекать из почвы серу и стимулировать поглощение этого элемента с соседними растениями.
- Чеснок выделяет вещество – альбуцид, едкое соединение серы. Это вещество предотвращает раковые заболевания, замедляет старение, предупреждает сердечные заболевания.
Источник

История элемента

Элемент был открыт Й. Я. Берцелиусом в 1817 году. Шведский химик и минералог проводил опыты с серной кислотой вместе с Я. Г. Ганом. Учёные обнаружили в веществе красновато-коричневый осадок с редечным запахом, который тогда служил определением присутствия теллура. Берцелиус решил исследовать осадок, надеясь обнаружить новый металл. После изучения этого явления он смог выявить неизвестное вещество, которое по свойствам напоминало теллур. Поскольку второй элемент был назван в честь Земли, химик назвал новый элемент Selenium (селен), что переводится с латинского «Луна».
В 1873 году Уиллоуби Смит доказал, что электрическое сопротивление элемента зависит от освещённости. Через несколько лет были разработаны первые продукты в виде ячеек на основе селена, которые использовали в фотофоне, созданном А. Г. Беллом. С помощью химического элемента можно было изменять электропроводимость световых лучей, которые отражались от зеркала под влиянием звука. Полезное свойство селена позволило использовать его в разных измерителях освещённости.
В первой половине XX века начали производить выпрямители на основе этого элемента, которые заменили медно-закисные изделия. Полупроводниковые диоды широко использовали до 1970-х годов.
Когда начали происходить массовые отравления работников на селеновых заводах и животных, поедавших траву около этих предприятий, люди поняли, что химический элемент токсичен. В середине прошлого века учёные раскрыли биологическое значение вещества для живых организмов.
Нахождение в природе и получение

Неметалл в объёме 500 мг/т содержится в земной коре. Основные черты вещества можно определить по близкому отношению ионных радиусов селена и серы. С «лунным» элементом образуются 37 минералов, включая ашавалит, гуанахуатит, клаусталит, платинит, тиманнит и хастит. Селен в виде самородков встречается довольно редко. Его минералы можно найти чаще, но добывают материал в основном из сульфидов. В этих соединениях объём неметалла варьируется в пределах чисел 7−100 г/т. В морской воде концентрация вещества составляет 0,4 мкг/л.
Основным источником неметалла выступают шламы свинцовых камер и пыль, которая образуется при обжиге сульфидов с соответствующим веществом. Сырьё обрабатывают концентрированной серной кислотой с нитратом натрия. В результате реакции образуется селенистая кислота с формулой H2SeO3 и в небольшом объёме селеновая кислота (H2SeO4). Затем селенистую кислоту обрабатывают сернистым газом и получают элементарный селен и серную кислоту.
Чтобы очистить полученный осадок, его сжигают в кислороде, который насыщают парами азотной кислоты. В результате получается чистый диоксид селена. В раствор SeO2 добавляют соляную кислоту, а затем пропускают через него сернистый газ, осаждая нужный элемент. Полученное вещество переплавляют, фильтруют через стеклоткань или активированный уголь. Последняя стадия очистки элемента подразумевает дистилляцию в вакууме.
Строение атома и структура
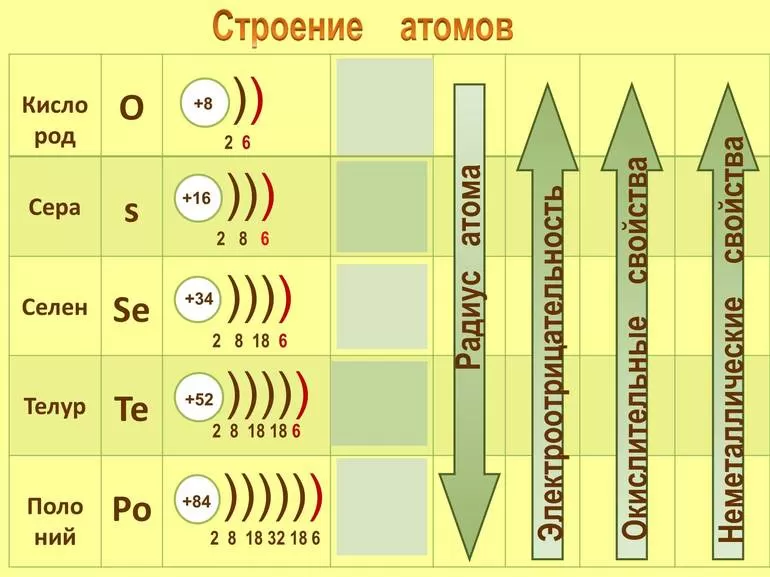
Селен состоит в 4-м периоде VI группы химических элементов. Неметалл имеет порядковый номер 34, его обозначение в таблице — Se. Атомная масса составляет 78,96 а. е. м., электронная формула селена — 1s22s22p63s23p63d104s24p4. Атом химического элемента имеет ядро с положительным зарядом +34. В него входят 34 протона, 45 нейронов и 34 электрона, которые движутся по 3-м орбитам.
Элемент отличается интересной конфигурацией. На внешнем энергетическом уровне располагаются 6 валентных отрицательно заряженных частиц. Поскольку в атоме селена есть два неспаренных электрона, это говорит о его ковалентности.
Вещество может быть представлено в двух модификациях:
- кристаллическая (моноклинный и гексагональный селен);
- аморфная.
Во втором случае неметалл имеет порошкообразную, коллоидную или стекловидную форму. Аморфная модификация неустойчива. Красный порошкообразный или коллоидный селен образуется при восстановлении из раствора селенистой кислоты. Чтобы получить стекловидную форму чёрного цвета, вещество любой модификации нагревают до температуры 220 °C, а потом сразу же охлаждают.
Гексагональный селен тёмно-серого оттенка устойчив в термодинамических условиях. Любую форму вещества нагревают до температуры плавления и затем охлаждают до 180−200°C, выдерживая этот показатель определённый период.
Физические особенности
Селен относится к группе халькогенов. Неметалл представляет собой хрупкое и непрозрачное вещество чёрного цвета. В неустойчивой форме он имеет оттенок киноварь. Обладает металлическим блеском.
Основные характеристики селена в гексагональной модификации:
- твёрдость по шкале Мооса — 2;
- плотность — 4,8 г/см3;
- температура плавления — 217 °C;
- температура кипения — 685−688°C;
- цвет черты — красный.

Гибкий материал относится к диамагнетикам. Он характеризуется высоким оптическим рельефом и анизотропией. Цвет минерала в воздухе — белый. В иммерсии (микроскопическое наблюдение) оттенок становится темнее и может быть серовато-коричневым. Только на просвет химический элемент приобретает красную окраску.
Химические свойства

Так как неметалл характеризуется двумя неспаренными электронами, степень окисления селена равна +2. Но у вещества есть вакантные орбитали на четвёртом уровне 4d-подуровня. Это говорит о том, что элемент может находиться в возбуждённом состоянии, при котором степень окисления меняется на +4.
По химическим свойствам неметалл близок к теллуру и сере, занимая промежуточное место между ними. Однако в соединениях со степенью окисления -2 он служит сильным восстановителем, а с показателем +6 — окислителем. Простое вещество селен отличается меньшей активностью, чем сера. Элемент способен гореть в воздухе самостоятельно. Окисление неметалла происходит только при нагревании. Вещество горит синим пламенем. Бурные реакции с селеном наблюдаются при взаимодействии с щелочными металлами.
Химический элемент может образовывать с кислородом несколько оксидов. SeO2 и SeO3 выступают ангидридами селеновой и селенистой кислот, с которыми получают селенат и селенит. Также неметалл может образовывать SeO и SeO5. Диоксид селена (SeO2) представляет собой кристаллическое вещество. Он хорошо растворяется в воде и считается довольно устойчивым соединением.
Меры безопасности

«Лунный» элемент относится к третьему классу опасности, поэтому с токсичным веществом и его соединениями следует работать осторожно. По характеру воздействия на человеческий организм селен напоминает мышьяк. Он может поражать печень, почки и ЦНС. В металлической форме вещество менее токсично. Наиболее опасными соединениями считаются диоксид селена, селеноводород и селениты натрия или лития.
Если вещество в форме металлического порошка попало в организм через рот, тогда у человека возникнут сильные боли в животе и диарея. Пострадавшему не потребуется помощь, если объём токсичного материала не превышал 1 г. Через какое-то время симптомы пройдут самостоятельно.
На кожном покрове могут возникнуть ожоги или аллергическая реакция в виде дерматита при контакте с солями неметалла. Диоксид селена вызывает резкую боль и онемение. Соединения химического элемента могут сильно раздражить слизистые оболочки. Также они вызывают покраснения, а при попадании в органы зрения — режущую боль, слезотечение и конъюнктивит.
Сферы применения
Селен, а также его соединения и сплавы широко используются в качестве полупроводника для выпрямителей переменного тока. В современной технологии применяют селениды висмута, олова, свинца, сурьмы.
Неметалл используется и в других областях:

- Это вещество необходимо при создании фототехники.
- В виде источника излучения для дефектоскопии применяют радиоактивный изотоп селен-75.
- Селен может использоваться как наполнитель в резиновой промышленности.
- В металлургии элемент необходим для придания полученным сплавам мелкозернистой структуры.
- В стекольной промышленности вещество используется для обесцвечивания или окрашивания прозрачного материала в красные или розовые оттенки. Обычно для этого выбирают металлическую форму элемента или селенистокислый натрий. Селеном окрашены рубиновые звёзды Московского Кремля.
- Материал применяется и в производстве керамических изделий, которым он придаёт красноватые оттенки. Также этим веществом окрашивают эмали.
Хотя селен относится к токсичным веществам, он может использоваться и в сфере медицины благодаря своим антиоксидантным свойствам. Неметалл выступает мощным противораковым средством. Препараты с селеном применяют в профилактике развития различных болезней. В малых концентрациях вещество подавляет гистамин. Селен обладает противоаллергическим и антидистрофическим эффектом. Соли неметалла избавляют от гипотонии при шоке и коллапсе.
Значение для человека

Селен — жизненно необходимый для живых организмов микроэлемент. Он содержится в активных центрах некоторых белков в виде аминокислот селеноцистеина. Объём вещества в человеческом организме составляет 10−14 мг. Основная часть находится в печени, почках, селезёнке, яичках и семенных канатиках у мужчин. В небольших количествах микроэлемент присутствует в костном мозге, сердце, лёгких, коже, волосах и ногтях.
Вещество взаимодействует с различными витаминами и ферментами. Он обнаружен в составе более 30 биологических соединений. Благодаря учёным удалось узнать о пользе и вреде селена для организма человека:

- Микроэлемент восстанавливает работу нервной и эндокринной системы.
- Препараты с этим веществом усиливают иммунитет.
- Селен улучшает функцию сосудов и препятствует развитию сердечно-сосудистых патологий.
- Сильный антиоксидант тормозит старение организма и выводит из него чужеродные вещества.
- Неметалл снижает возможность развития злокачественных опухолей.
- Он улучшает работу половых желёз и стимулирует репродуктивную функцию.
- Селен нормализует процессы обменов в человеческом организме и защищает его от возможного токсического действия кадмия, ртути, свинца, серебра и таллия.
- Вещество уменьшает боли при воспалениях.
Микроэлемент также участвует в обмене белков, жиров и углеводов. Без него не обходятся окислительно-восстановительные процессы. Из занимательных фактов о селене нужно отметить, что он контролирует весь цикл жизни клетки.
Полезные продукты
Для людей суточная норма селена составляет 70−110 мкг. Объём зависит от возраста и половой принадлежности человека. Для взрослых мужчин максимальное количество вещества в день составляет 140 мкг.
Селеном богаты продукты как животного, так и растительного происхождения:

- злаковые культуры;
- масло оливы;
- орехи;
- томаты;
- маслины;
- чеснок;
- грибы;
- рыба и другие морепродукты;
- говяжьи почки и печень;
- морская соль;
- ржаной хлеб;
- яйца курицы.

Повышенное содержание микроэлемента в человеческом организме может вызвать тошноту, рвоту или понос. В некоторых случаях развивается депрессия. На избыток вещества указывают такие симптомы, как желтушность и шелушение кожи, разрушение ногтей, выпадающие волосы, отсутствие аппетита, постоянная усталость и расстройства ЦНС. Если в организме повышается объём ртути, меди или сульфатов, тогда наблюдается недостаток селена. К дефициту элемента может привести применение медикаментозных средств от малярии.
Селен выполняет важную роль не только в различных сферах жизни человека, но и в его организме. С правильным рационом получится поддерживать объём вещества на нужном уровне.
Источник
Сера – элемент VIa группы 3 периода периодической таблицы Д.И. Менделеева. Относится к
группе халькогенов – элементов VIa группы.
Сера – S – простое вещество имеет светло-желтый цвет. Использовалась еще до нашей эры в составе священных курений при
религиозных обрядах.

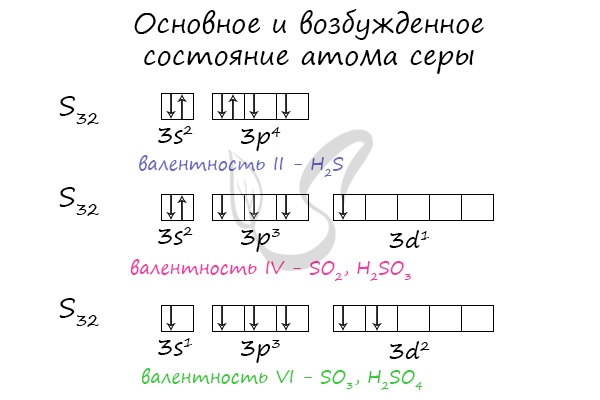
Основное и возбужденное состояние атома серы
Электроны s- и p-подуровня способны распариваться и переходить на d-подуровень. Как и всегда, количество валентных
электронов отражает количество возможных связей у атома.
В разных электронных конфигурациях сера способна принимать валентности: II, IV и VI.
Природные соединения
- FeS2 – пирит, колчедан
- ZnS – цинковая обманка
- PbS – свинцовый блеск (галенит), Sb2S3 – сурьмяный блеск, Bi2S3 – висмутовый блеск
- HgS – киноварь
- CuFeS2 – халькопирит
- Cu2S – халькозин
- CuS – ковеллин
- BaSO4 – барит, тяжелый шпат
- CaSO4 – гипс
В местах вулканической активности встречаются залежи самородной серы.

Получение
В промышленности серу получают из природного газа, который содержит газообразные соединения серы: H2S,
SO2.
H2S + O2 = S + H2O (недостаток кислорода)
SO2 + C = (t) S + CO2
Серу можно получить разложением пирита
FeS2 = (t) FeS + S
В лабораторных условиях серу можно получить слив растворы двух кислот: серной и сероводородной.
H2S + H2SO4 = S + H2O
Химические свойства
- Реакции с неметаллами
- Реакции с металлами
- Реакции с кислотами
- Реакции с щелочами
- Реакции с солями
На воздухе сера окисляется, образуя сернистый газ – SO2. Реагирует со многими неметаллами, без нагревания –
только со фтором.
S + O2 = (t) SO2
S + F2 = SF6
S + Cl2 = (t) SCl2
S + C = (t) CS2

При нагревании сера бурно взаимодействует со многими металлами с образованием сульфидов.
K + S = (t) K2S
Al + S = Al2S3
Fe + S = (t) FeS
При взаимодействии с концентрированными кислотами (при длительном нагревании) сера окисляется до сернистого газа или серной кислоты.
S + H2SO4 = (t) SO2 + H2O
S + HNO3 = (t) H2SO4 + NO2 + H2O
Сера вступает в реакции диспропорционирования с щелочами.
S + KOH = (t) K2S + K2SO3 + H2O
Сера вступает в реакции с солями. Например, в кипящем водном растворе сера может реагировать с сульфитами с образованием тиосульфатов.
Na2SO3 + S → (t) Na2S2O3
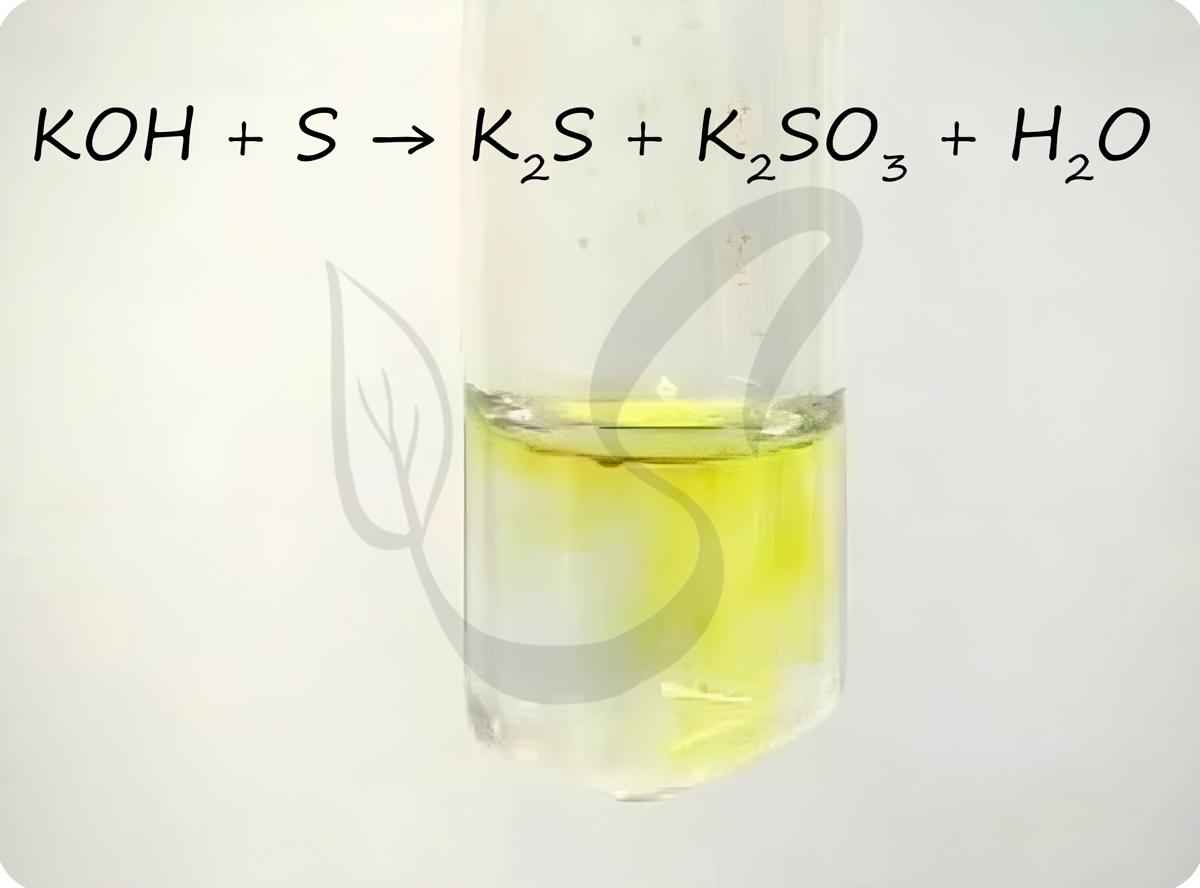
Сероводород – H2S
Бесцветный газ с характерным запахом тухлых яиц. Огнеопасен. Используется в химической промышленности и в лечебных целях (сероводородные
ванны).

Получение
Сероводород получают в результате реакции сульфида алюминия с водой, а также взаимодействия разбавленных кислот с сульфидами.
Al2S3 + H2O = (t) Al(OH)3↓ + H2S↑
FeS + HCl = FeCl2 + H2S↑

Химические свойства
- Кислотные свойства
- Восстановительные свойства
- Качественная реакция
Сероводород плохо диссоциирует в воде, является слабой кислотой. Реагирует с основными оксидами, основаниями с образованием средних и кислых солей (зависит
от соотношения основания и кислоты).
MgO + H2S = (t) MgS + H2O
KOH + H2S = KHS + H2O (гидросульфид калия, избыток кислоты)
2KOH + H2S = K2S + 2H2O
Металлы, стоящие в ряду напряжений до водорода, способны вытеснить водород из кислоты.
Ca + H2S = (t) CaS + H2
Сероводород – сильный восстановитель (сера в минимальной степени окисления S2-). Горит в кислороде синим пламенем, реагирует с кислотами.
H2S + O2 = H2O + S (недостаток кислорода)
H2S + O2 = H2O + SO2 (избыток кислорода)
H2S + HClO3 = H2SO4 + HCl

Качественной реакцией на сероводород является реакция с солями свинца, при котором образуется сульфид свинца.
H2S + Pb(NO3)2 = PbS↓ + HNO3
Оксид серы – SO2
Сернистый газ – SO2 – при нормальных условиях бесцветный газ с характерным резким запахом (запах загорающейся
спички).

Получение
В промышленных условиях сернистый газ получают обжигом пирита.
FeS2 + O2 = (t) FeO + SO2
В лаборатории SO2 получают реакцией сильных кислот на сульфиты. В ходе подобных реакций образуется сернистая кислота,
распадающаяся на сернистый газ и воду.
K2SO3 + H2SO4 = (t) K2SO4 + H2O + SO2↑
Сернистый газ получается также в ходе реакций малоактивных металлов с серной кислотой.
Cu + H2SO4(конц.) = (t) CuSO4 + SO2 + H2O
- Кислотные свойства
- Восстановительные свойства
- Как окислитель
С основными оксидами, основаниями образует соли сернистой кислоты – сульфиты.
K2O + SO2 = K2SO3
NaOH + SO2 = NaHSO3
2NaOH + SO2 = Na2SO3 + H2O

Химически сернистый газ очень активен. Его восстановительные свойства продемонстрированы в реакциях ниже.
Fe2(SO4)3 + SO2 + H2O = FeSO4 + H2SO4
SO2 + O2 = (t, кат. – Pt) SO3
В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства (понижать степень окисления).
CO + SO2 = CO2 + S
H2S + SO2 = S + H2O
Сернистая кислота
Слабая, нестойкая двухосновная кислота. Существует лишь в разбавленных растворах.
Получение
SO2 + H2O ⇄ H2SO3
Химические свойства
- Диссоциация
- Кислотные свойства
- Окислительные свойства
- Восстановительные свойства
Диссоциирует в водном растворе ступенчато.
H2SO3 = H+ + HSO3-
HSO3- = H+ + SO32-
В реакциях с основными оксидами, основаниями образует соли – сульфиты и гидросульфиты.
CaO + H2SO3 = CaSO3 + H2O
H2SO3 + 2KOH = 2H2O + K2SO3 (соотношение кислота – основание, 1:2)
H2SO3 + KOH = H2O + KHSO3 (соотношение кислота – основание, 1:1)
С сильными восстановителями сернистая кислота принимает роль окислителя.
H2SO3 + H2S = S↓ + H 2O
Как и сернистый газ, сернистая кислота и ее соли обладают выраженными восстановительными свойствами.
H2SO3 + Br2 = H2SO4 + HBr

Оксид серы VI – SO3
Является высшим оксидом серы. Бесцветная летучая жидкость с удушающим запахом. Ядовит.
Получение
В промышленности данный оксид получают, окисляя SO2 кислородом при нагревании и присутствии катализатора
(оксид ванадия – Pr, V2O5).
SO2 + O2 = (кат) SO3
В лабораторных условиях разложением солей серной кислоты – сульфатов.
Fe2(SO4)3 = (t) SO3 + Fe2O3
Химические свойства
- Кислотные свойства
- Окислительные свойства
Является кислотным оксидом, соответствует серной кислоте. При реакции с основными оксидами и основаниями образует ее соли – сульфаты и
гидросульфаты. Реагирует с водой с образованием серной кислоты.
SO3 + 2KOH = K2SO4 + 2H2O (основание в избытке – средняя соль)
SO3 + KOH = KHSO4 + H2O (кислотный оксид в избытке – кислая соль)
SO3 + Ca(OH)2 = CaSO4 + H2O

SO3 + Li2O = Li2SO4
SO3 + H2O = H2SO4
SO3 – сильный окислитель. Чаще всего восстанавливается до SO2.
SO3 + P = SO2 + P2O5
SO3 + H2S = SO2 + H2O
SO3 + KI = SO2 + I2 + K2SO4

© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
