Какими магнитными свойствами обладает молекула
Одним из серьезных преимуществ метода МО ЛКАО по сравнению с МВС является более правильное описание магнитных свойств молекул и ионов, и в частности объяснение парамагнетизма молекулярного кислорода.
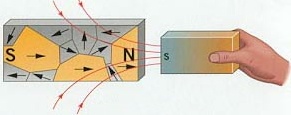
Взаимодействие химических веществ с магнитным полем порождает несколько эффектов. Среди них наиболее известным является ферромагнетизм. Намагниченные ферромагнетики (например, железо, кобальт, никель) магнитны — они обладают собственным магнитным нолем, которое проявляется во взаимодействии с другими ферромагнетиками. Ненамагни- ченные ферромагнетики притягиваются намагниченными.
Большая часть химических веществ (например, соли, оксиды, органические вещества) не относится к ферромагнетикам. Но и немагнитные в обычных условиях вещества взаимодействуют с внешним магнитным полем. Это проявляется в двух эффектах — парамагнетизме и диамагнетизме.
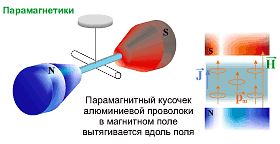
Парамагнетизм — явление втягивания немагнитного вещества в область сильного магнитного поля (вещество «притягивается магнитом»). Причина парамагнетизма — наличие в составе вещества частиц с собственным магнитным моментом. При воздействии внешнего поля хаотически расположенные из-за теплового движения магнитные моменты этих частиц ориентируются по полю и усиливают его.
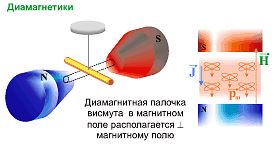
Диамагнетизм — явление выталкивания немагнитного вещества из области сильного магнитного поля (вещество «отталкивается магнитом»). Причина диамагнетизма — наличие в веществе движущихся электронов, которые под действием внешнего поля порождают наведенный магнитный момент, ориентированный против поля.
Основной вклад в собственный магнитный момент атомов и молекул вещества вносят магнитные моменты неспаренных электронов. Чем больше суммарный спин электронов в атоме или молекуле, тем сильнее проявляется парамагнетизм вещества.
Следует особо подчеркнуть, что сказанное относится именно к химическим веществам с атомно-молекулярной структурой. В случае веществ с металлической связью картина взаимодействия вещества с магнитным полем значительно усложняется из-за появления значительного количества свободных электронов и сложной структуры кристаллической решетки, в узлах которой расположены электрически заряженные «атомные остовы» металлов. Все вместе это приводит к существенному увеличению диамагнитного вклада магнитных моментов индукционных токов, и такие вещества, как висмут, медь, золото, серебро, цинк, свинец, будучи в атомарном состоянии парамагнетиками, в виде простых веществ становятся диамагнетиками.
Структура молекулы кислорода 02 по МВС такова, что все валентные электроны а- и л-связей в ней образуют электронные пары и суммарный спин электронов молекулы равен нулю. Модель предсказывает, что кислород должен быть диамагнитным (см. рис. 2.4).
Как следует из диаграммы, построенной по методу МО (рис. 2.14), в молекуле кислорода присутствуют два неспаренных электрона на разрыхляющих 71^л и я2/, орбиталях. Их магнитные моменты складываются и дают отличный от нуля суммарный магнитный момент молекулы. В соответствии с этим метод МО ЛКА О предсказывает, что молекулы кислорода обладают магнитными свойствами и, следовательно, вещество кислород обладает парамагнетизмом.
Рис. 2.14. Энергетическая диаграмма молекулы кислорода по методу МО ЛКАО
Эксперимент показывает, что магнитный момент молекулы кислорода равен 2,8 магнетонов Бора {магнетон Бора — единица элементарного магнитного момента). Собственный магнитный момент электрона, обусловленный его спином, равен одному магнетону Бора. Учитывая, что полный магнитный момент, кроме собственного электронного, включает в себя и орбитальный, связанный с движением электрона по орбитали, количественное совпадение весьма убедительно свидетельствует в пользу справедливости структуры молекулярных орбиталей на основании метода МО ЛКАО.
Кроме магнитных свойств анализ энергетических диаграмм МО ЛКАО дает возможность определить кратность Ксв, или порядок Псп химической связи:
где ЛГСВЯЗ — общее число электронов на связывающих орбиталях; ЛГразр — общее число электронов на разрыхляющих орбиталях.
Эта величина соответствует «количеству черточек» в графических формулах химических веществ по Льюису. Чем больше величина Ксв, тем прочнее связь в молекуле или ионе.
Источник
Молекулы, образованные двумя атомами с разной электроотрицательностью, полярны. Дипольный момент μ = e∙ℓ, где е – значение элементарного электрического заряда; ℓ – расстояние между зарядами. Если связь между атомами одинарная, то чем выше разница в электроотрицательности атомов, тем более полярна молекула. Если же атомы связаны кратной связью, то на основании электроотрицательности атомов нельзя однозначно сказать о полярности связи и направленности диполя молекулы. Это объясняется вкладом неподеленной электронной пары одного из атомов в общую полярность молекулы. Например, молекулы HCl и СО составлены атомами, у которых разность между электроотрицательностями примерно одинакова и равна единице. Однако дипольные моменты молекул разные: μ(HCl) >> μ(СО). И направленность диполя в молекуле СО другая: отрицательный конец диполя направлен в сторону менее электроотрицательного атома углерода. Объясняется это тем, что в молекуле СО тройная связь: две связи образуют неспаренные электроны по обменному механизму (общие электронные пары смещены к атому кислорода как более электроотрицательному), третья связь образуется по донорно-акцепторному механизму (атом кислорода предоставляет свою неподеленную электронную пару на свободную орбиталь атома углерода). Это приводит к смещению электронной плотности от атома кислорода к атому углерода и это смещение настолько велико, что избыточная электронная плотность оказывается на атоме углерода.
Молекулы, состоящие более чем из двух атомов, могут быть полярными или неполярными, даже если отдельные химические связи в ней полярные. Симметричное располажение даже полярных связей приводит к общей неполярности молекулы. Например, О=С=О – симметрично линейная неполярная молекула. В ней химические связи полярные, но центр тяжести и положительного и отрицательного зарядов находится в центре молекулы в силу ее симметричности.
Гибридизация связей приводит к неполярности молекул или ионов. Но не всегда, а только тогда когда гибридная орбиталь не занята неподеленной электронной парой. Если же на гибридной орбитали находится неподеленная электронная пара, то это приводит к сильному смещению центра тяжести отрицательных зарядов и к увеличению полярности молекулы.
Если ион или молекулу поместить в электрическое поле, то происходит деформация – смещение ядер и электронов относительно друг друга. Такая деформация называется поляризуемостью. В первую очередь испытывают смещение электроны внешнего слоя.
При одинаковом радиусе и заряде наибольшей поляризуемостью обладают ионы, которые имеют внешнюю заполненную 18 электронную оболочку; меньшей поляризуемостью обладают ионы с незаполненной 18-электронной оболочкой; еще меньшей – ионы с 8-электронной структурой.
При одинаковой структуре электронных оболочек поляризуемость иона уменьшается по мере увеличения положительного заряда иона.
Для электронных аналогов поляризуемость ионов увеличивается с ростом числа электронных слоев.
Электрическое поле может быть создано самим ионом, т.е. ион сам может оказывать поляризующее действие на другие ионы или молекулы. Поляризующее действие иона возрастает с увеличением заряда и уменьшением радиуса, а при одинаковом заряде и радиусе – по ряду 8-электронных структур; незаконченных 18-электронных структур; законченных 18-электронных структур. При этом катионы обладают большим поляризующим действием, чем анионы, т.к. они меньше по размерам.
Молекулы обладают поляризующим действием только, если они полярны, и это действие тем выше, чем больше μ.
По своим магнитным свойствам все вещества делятся на парамагнитные и диамагнитные.
Парамагнитные вещества – это те, в которых атомы или молекулы обладают постоянным магнитным моментом.
Диамагнитные – те, атомы или молекулы которых не обладают магнитным моментом.
Парамагнитные вещества обладают свойством втягиваться в магнитное поле, диамагнитные – выталкиваются магнитным полем.
Если в молекуле имеются неспаренные электроны, то она обладает парамагнитными свойствами, если неспаренных электронов нет, то молекула диамагнитна. Такой вывод дает МВС и он в основном верен. Но не всегда МВС в состоянии объяснить магнитные свойства веществ. Например, с точки зрения МВС молекула О2 должна быть диамагнитна, а она обладает парамагнитными свойствами. Этот факт объясняет другой метод описания химической связи – метод молекулярных орбиталей (ММО).
Ионная и водородная связь
Валентная связь, сопровождающаяся практически полным переходом электронной пары к одному из атомов и последующим сближением образовавшихся ионов (электрически заряженных частиц, образовавшихся из атомов или атомных групп вследствие потери или присоединения электронов), называется ионной связью.
Соединение по типу ионной связи происходит в тех случаях, когда реагирующие атомы обладают резко противоположным характером – элементы 1,2 групп с элементами 5-8 групп. Однако полностью ионной связи не существует.
Наиболее близкое к такому положению имеет место в кристаллах наиболее типичных солей.
Так как в основе ионной связи – электростатическое притяжение разных по знаку зарядов, то такая связь характеризуется насыщенностью.
Водородной называют такую связь, которая образуется посредством атома водорода, входящего в состав одной из двух связанных частиц (молекул или ионов).
О наличии такой особой связи свидетельствуют аномально высокие температуры кипения Н2О и НF по сравнению со своими аналогами H2S и др. и HCl и др. Такая связь препятствует отрыву молекул друг от друга, т.е. уменьшает испаряемость.
Водородная связь объясняется кулоновскими силами притяжения, действующими между эффективными +δ и –δ –зарядами разных молекул с сильно полярными связями. Атом водорода имеет эффективный +δ, а атом кислорода или фтора (в силу большой разницы в электроотрицательности) – -δ. Благодаря кулоновским силам молекулы притягиваются – это межмолекулярная связь. Водородная связь графически обозначается пунктирной линией:
Н+δ-F-δ—-Н+δ-F-δ
Энергия водородной связи примерно в 10 раз меньше, чем обычной ковалентной. Однако ее хватает для существования в парах димеров Н2О, НF и муравьиной кислоты.
Водородная связь может быть и внутримолекулярной, например в органических соединениях со смешанными функциями.
Источник
Магнитные свойства молекул и ионов. Диа- и парамагнитные молекулы и их свойства.
Все вещества делят на парамагнитные и диамагнитные. Вещество называют парамагнитным, если его атомы( или молекулы) обладают магнитным моментом, и диамагнитным, если его атомы не обладают постоянным магнитным моментом.
Парамагнитные вещества обладают свойством втягиваться в магнитное поле, а диамагнитные вещества выталкиваются им.
Магнитные моменты атомов определяются главным образом суммарным моментом электронов в атоме.
Магнитные свойства молекул и ионов. Диа- и парамагнитные молекулы.
— совокупность св-в, проявляющихся при взаимодействии вещества с магнитным полем. Важнейшим макроскопическим проявлением магнитных свойств является способность вещества создавать собственное магнитное поле.
Способность вещества взаимодействовать с внешним магнитным полем зависит от магнитных свойств, точнее, от магнитных моментов свободных атомов или молекул этого вещества, к-рые определяются главным образом их электронным строением. Магнитный момент атома состоит в основном из магнитного момента, обусловленного спином электрона (спин электрона — собственный механич. момент количества движения электрона), и из магнитного момента, обусловленного орбитальным движением электрона вокруг ядра атома. Магнитный момент ядра атома примерно в тысячу раз меньше магнитного момента электронной оболочки атома и при рассмотрении обычных магнитных свойств его можно не учитывать. Ядерный магнетизм проявляется в ядерном магнитном резонансе и в сверхтонкой структуре спектральных линий.
Диамагнетизм — один из видов магнетизма, который проявляется в намагничивании вещества навстречу направлению действующего на него внешнего поля.
Диамагнетизм можно рассматривать как следствие индукционных токов, наводимых в заполненных электронных оболочках ионов внешним магнитным полем. Идеальный диамагнетизм носит некооперативный характер и характеризуется отрицательной, не зависящей от температуры магнитной восприимчивостью. Диамагнетизм входит в состав любого магнитного состояния вещества. В частности, это имеет место в ионах и молекулах с целиком заполненными электронными оболочками, например в инертных газах, в молекулах.
Парамагнетики — вещества, которые намагничиваются во внешнем магнитном поле в направлении внешнего магнитного поля
Термин «Парамагнетизм» ввёл в 1845 году Майкл Фарадей, который разделил все вещества (кроме ферромагнитных) на диа- и парамагнитные.
Атомы (молекулы или ионы) парамагнетика обладают собственными магнитными моментами, которые под действием внешних полей ориентируются по полю и тем самым создают результирующее поле, превышающее внешнее. Парамагнетики втягиваются в магнитное поле. В отсутствие внешнего магнитного поля парамагнетик не намагничен, так как из-за теплового движения собственные магнитные моменты атомов ориентированы совершенно беспорядочно.
Парамагнитные молекулы и их свойства.
Парамагнетики — вещества, которые намагничиваются во внешнем магнитном поле в направлении внешнего магнитного поля
Термин «Парамагнетизм» ввёл в 1845 году Майкл Фарадей, который разделил все вещества (кроме ферромагнитных) на диа- и парамагнитные.
Атомы (молекулы или ионы) парамагнетика обладают собственными магнитными моментами, которые под действием внешних полей ориентируются по полю и тем самым создают результирующее поле, превышающее внешнее. Парамагнетики втягиваются в магнитное поле. В отсутствие внешнего магнитного поля парамагнетик не намагничен, так как из-за теплового движения собственные магнитные моменты атомов ориентированы совершенно беспорядочно.
Парамагнитные тела притягиваются к магниту.
Парамагнитные вещества увеличивают магнитный поток катушки т. к. у них магнитная проницаемость более 1. В парамагнитных веществах под действием внешнего магнитного поля элементарные токи ориентируются так, что направление их совпадает с направлением тока обмотки.
21.01.2014; 23:16 хиты: 5189 рейтинг:+1 | Естественные науки химия |
Источник
Магнетики – вещества, обладающие магнитными свойствами. Магнетиками являются все вещества, поскольку согласно гипотезе Ампера, магнитные свойства создаются элементарными токами (движением электрона в атоме).
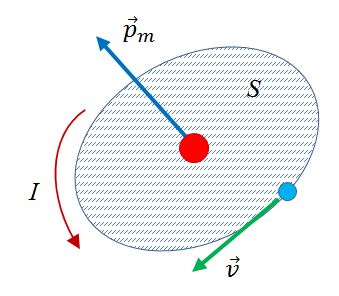
Электрон, вращающийся по замкнутой орбите, представляет собой ток, направление которого противоположно движению электрона. Тогда это движение создает магнитное поле, магнитный момент которого pm = IS направлен по правилу правой руки перпендикулярно плоскости орбиты.
Кроме того, независимо от орбитального движения, электроны обладают собственным магнитным моментом (спином). Таким образом, магнетизм атомов обусловлен двумя причинами: движением электронов по орбитам и собственным магнитным моментом.
При внесении магнетика во внешнее магнитное поле с индукцией В0 он намагничивается, то есть создает собственное магнитное поле с индукцией В’, которое складывется с внешним:
В = В0 + В’
Индукция собственного магнитного поля зависит как от внешнего поля, так и от магнитной восприимчивости χ вещества:
В’ = χ В0
Тогда В = В0 + χ В0 = В0 (1 + χ)
Но магнитная индукция внутри магнетика зависит от магнитной проницаемости вещевтва:
В = μ В0
Отсюда μ = 1 + χ.
Магнитная восприимчивость χ — физическая величина, характеризующая связь между магнитным моментом (намагниченностью) вещества и магнитным полем в этом веществе | Магнитная проницаемость μ — коэффициент (зависящий от свойств среды), характеризующий связь между магнитной индукцией и напряжённостью магнитного поля в веществе |
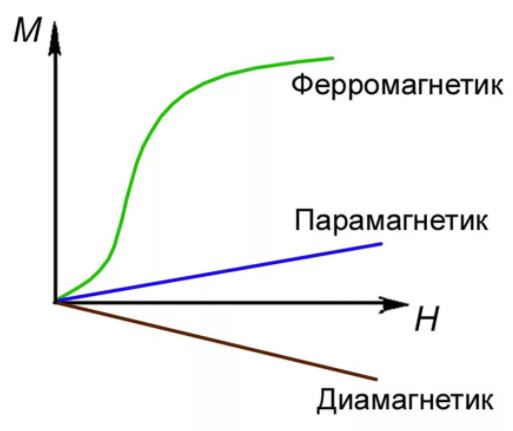
В отличие от диэлектрической проницаемости вещества, которая всегда больше единицы, магнитная проницаемость может быть как больше, так и меньше единицы. Различают диамагнетики (μ < 1), парамагнетики (μ > 1) и ферромагнетики (μ >> 1).
Диамагнетики
Диамагнетиками называются вещества, которые намагничиваются во внешнем магнитном поле в направлении, противоположном направлению вектора магнитной индукции поля.
К диамагнетикам относятся вещества, магнитные моменты атомов, молекул или ионов которых в отсутствие внешнего магнитного поля равны нулю. Диамагнетиками являются инертные газы, молекулярный водород и азот, цинк, медь, золото, висмут, парафин и многие другие органические и неорганические соединения.
В случае отсутствия магнитного поля диамагнетик немагнитен, поскольку в данном случае магнитные моменты электронов взаимно компенсируются, и суммарный магнитный момент атома равен нулю.
Т.к. диамагнитный эффект обусловлен действием внешнего магнитного поля на электроны атомов вещества, то диамагнетизм свойственен всем веществам.
Следует отметить, что магнитная проницаемость у диамагнетиков µ < 1. Вот, например, у золота µ = 0,999961, у меди µ = 0,9999897 и т.д.
В магнитном поле диамагнетики располагаются перпендикулярно силовым линиям внешнего магнитного поля.
Парамагнетики
Парамагнетики – вещества, намагничивающиеся во внешнем магнитном поле по направлению поля.
У парамагнитных веществ при отсутствии внешнего магнитного поля магнитные моменты электронов не компенсируют друг друга, и атомы (молекулы) парамагнетиков всегда обладают магнитным моментом. Однако вследствие теплового движения молекул их магнитные моменты ориентированы беспорядочно, поэтому парамагнитные вещества магнитными свойствами не обладают. При внесении парамагнетиков во внешнее магнитное поле устанавливается преимущественная ориентация магнитных моментов атомов по полю (полной ориентации препятствует тепловое движение атомов).
Таким образом, парамагнетик намагничивается, создавая собственное магнитное поле, совпадающее по направлению с внешним полем и усиливающее его.
При ослаблении внешнего магнитного поля до нуля ориентация магнитных моментов вследствие теплового движения нарушается и парамагнетик размагничивается.
Вот некоторые парамагнитные вещества: алюминий µ = 1,000023; воздух µ = 1,00000038.
Во внешнем магнитном поле парамагнетики располагаются вдоль силовых линий.
Ферромагнетики
Ферромагнетиками называются твердые вещества, обладающие при не слишком высоких температурах самопроизвольной (спонтанной) намагниченностью, которая сильно изменяется под влиянием внешних воздействий – магнитного поля, деформации, изменения температуры.
Ферромагнетики в отличие от слабомагнитных диа- и парамагнетиков являются сильномагнитными средами:
внутреннее магнитное поле в них может в сотни и тысячи раз превосходить внешнее поле.
Ферромагнитные материалы в большой или меньшей степени обладают магнитной анизотропией, т.е. свойством намагничиваться с различной степенью трудности в различных направлениях.
Магнитные свойства ферромагнитных материалов сохраняются до тех пор, пока их температура не достигнет значения, называемого точкой Кюри. При температурах выше точки Кюри ферромагнетик ведет себя во внешнем магнитном поле как парамагнитное вещество. Он не только теряет свои ферромагнитные свойства, но у него изменяется теплоемкость, электропроводимость и некоторые другие физические характеристики.
Точка Кюри для различных материалов различна:
| Железо (Fe) | 780 οС |
| Никель (Ni) | 350 οС |
| Кобальт (Co) | 1130 οС |
| Гадолиний (Gd) | 16 οС |
| Диспрозий (Dy) | -186 οС |
Природа ферромагнетизма:
Согласно представлениям Вейсса (1865-1940), его описательной теории ферромагнетизма, ферромагнетики при температурах ниже точки Кюри обладают спонтанной намагниченностью независимо от наличия внешнего намагничивающего поля. Однако это вносило некое противоречие, т.к. многие ферромагнитные материалы при температурах ниже точки Кюри не намагничены.
Для устранения этого противоречия Вейсс ввел гипотезу, согласно которой ферромагнетик ниже точки Кюри разбивается на большое число малых микроскопических (порядка 10-3– 10-2 см) областей – доменов, самопроизвольно намагниченных до насыщения.

При отсутствии внешнего магнитного поля магнитные моменты отдельных атомов ориентированы хаотически и компенсируют друг друга, поэтому результирующий магнитный момент ферромагнетика равен нулю, т.е. ферромагнетик не намагничен.
Внешнее магнитное поле ориентирует по полю магнитные моменты не отдельных атомов, как в парамагнетике, а целых областей спонтанной намагниченности. Поэтому с ростом H намагниченность J и магнитная индукция B уже в слабых полях растет довольно быстро.
Различные ферромагнитные материалы обладают неодинаковой способностью проводить магнитный поток. Основной характеристикой ферромагнитного материала является петля магнитного гистерезиса В(Н). Эта зависимость определяет значение магнитной индукции, которая будет возбуждена в магнитопроводе из данного материала при воздействии некоторой напряженности поля.
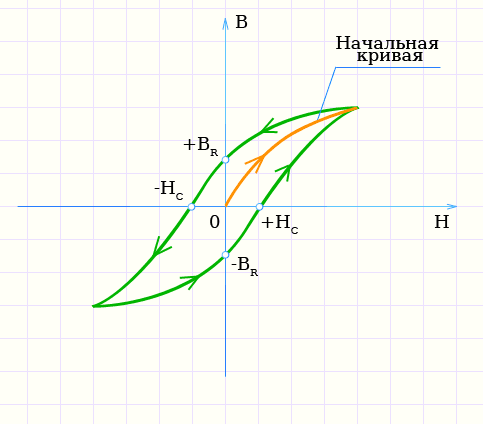
Рассмотрим процесс перемагничивания ферромагнетика. Пусть первоначально он был полностью размагничен. Сначала индукция быстро возрастает за счет того, что магнитные диполи ориентируются по силовым линиям поля, добавляя свой магнитный поток к внешнему. Затем ее рост замедляется по мере того, как количество неориентированных диполей уменьшается и, наконец, когда практически все они ориентируются по внешнему полю рост индукции прекращается и наступает режим насыщения.
Гистерезисом называют отставание изменения индукции от напряженности магнитного поля.
Симметричная петля гистерезиса, полученная при максимальной напряженности поля Hm, соответствующей насыщению ферромагнетика, называется предельным циклом.
Для предельного цикла устанавливают также значения индукции Br при H = 0, которое называется остаточной индукцией, и значение Hc при B = 0, называемое коэрцитивной силой. Коэрцитивная (удерживающая) сила показывает, какую напряженность внешнего поля следует приложить к веществу, чтобы уменьшить остаточную индукцию до нуля.
Форма и характерные точки предельного цикла определяют свойства ферромагнетика. Вещества с большой остаточной индукцией, коэрцитивной силой и площадью петли гистерезиса называются магнитнотвердыми.
Они используются для изготовления постоянных магнитов. Вещества с малой остаточной индукцией и площадью петли гистерезиса (кривая 2 рис.8а) называются магнитномягкими и используются для изготовления магнитопроводов электротехнических устройств, в особенности работающих при периодически изменяющемся магнитном потоке.
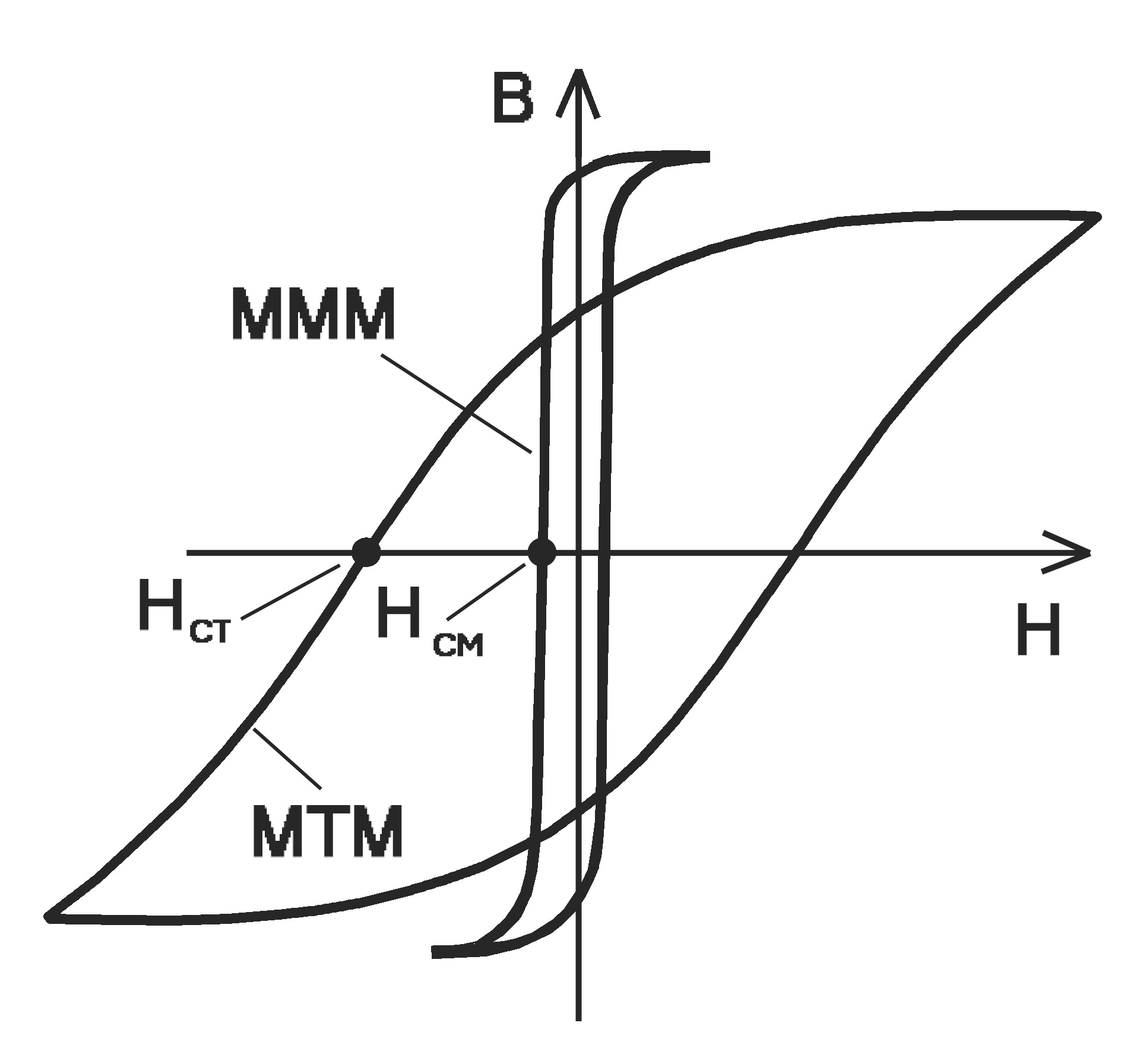
Площадь петли гистерезиса характеризует работу, которую необходимо совершить для перемагничивания ферромагнетика. Если по условиям работы ферромагнетик должен перемагничиваться, то его следует делать из магнито-мягкого материала, площадь петли гистерезиса которого мала. Из мягких ферромагнетиков делают сердечники трансформаторов.
Из жестких ферромагнетиков (сталь и ее сплавы) делают постоянные магниты.
Источник