Какими свойствами обладают твердые жидкие и газообразные вещества
Естественные науки, включающая химию и физику, обычно рассматриваются как науки, изучающие природу и свойства вещества и энергии в неживых системах. Вещество во Вселенной – атомы, молекулы и ионы, которые составляют все физические тела, все, что имеет массу и занимает пространство. Энергия — это способность вызывать изменения. Энергия не может быть создана или уничтожена; он может быть только сохранена и преобразована из одной формы в другую. Потенциальная энергия — это энергия, хранящаяся в объекте из-за его положения – например, ведро с водой, повешенное над дверью, может упасть. Кинетическая энергия — это энергия, движения, любой объект или частица, находящаяся в движении, обладает кинетической энергией, зависящей от массы и скорости тела. Кинетическая энергия может быть преобразована в другие виды энергии, такие как электрическая энергия и тепловая энергия.
Существует пять известных фаз или состояний вещества: твердое тело, жидкость, газ, плазма и бозе-эйнштейновский конденсат. Основное различие в структурах каждого состояния находится в плотностях частиц.
ТВЕРДОЕ ТЕЛО
В твердом теле частицы плотно упакованы, поэтому они не могут двигаться очень сильно. Частицы твердого вещества имеют очень низкую кинетическую энергию. Электроны каждого атома находятся в движении, поэтому атомы имеют небольшую вибрацию, но они фиксируются в своем положении. Твердые тела имеют определенную форму, и могут длительное время ее сохранять. У них также есть определенный объем. Частицы твердого тела уже настолько плотно упакованы вместе, что увеличивающееся давление не будет сжимать твердое тело до меньшего объема.
ЖИДКОСТИ
В жидкой фазе частицы вещества имеют большую кинетическую энергию, чем частицы в твердом теле. Частицы жидкости не удерживаются в регулярном расположении, но все еще очень близки друг к другу, поэтому жидкости имеют определенный объем. Жидкости, как и твердые тела, трудно сжимаемы. Частицы жидкости имеют достаточно места для обтекания друг друга, поэтому жидкости имеют неопределенную форму. Жидкость принимает форму емкости, в которую она помещена. Сила распределяется равномерно по всей жидкости, поэтому, когда объект помещается в жидкость, частицы жидкости перемещаются за объектом.
Величина восходящей плавучей силы равна весу жидкости, в объеме тела. Когда плавучая сила равна силе тяжести, объект будет плавать. Этот принцип плавучести был обнаружен греческим математиком Архимедом, который, согласно легенде, выпрыгнул из своей ванны и побежал обнаженным по улицам, крича «Эврика!», после того, как догадался о выталкивающих силах в жидкости. Эту силу еще называют силой Архимеда, как дань уважения и признания древнему ученому.
Частицы жидкости, как правило, удерживаются слабым межмолекулярным притяжением, а не свободно перемещаются, как частицы газа. Эта сила сцепления соединяет частицы вместе, образуя капли или потоки.
Ученые сообщили, что в апреле 2016 года они создали странное состояние материи, которое, как предполагалось, существовало, но никогда не было видно в реальной жизни. Хотя этот тип материи можно держать в руке, как если бы он был сплошным, увеличение материала выявило бы беспорядочные взаимодействия его электронов, более характерные для жидкости. Это тип материи называют квантовой спиновой жидкостью Китаева, в ней электроны входят в своеобразный квантовый танец, в котором они взаимодействуют или «разговаривают» друг с другом. Обычно, когда вещество остывает, спин его электронов имеет тенденцию выстраиваться в линию. Но в этой квантовой спиновой жидкости электроны взаимодействуют так, что они влияют на то, как другие вращаются и никогда не выравниваются независимо от того, насколько материал холодный. Материал будет вести себя так, как будто его электроны, считающиеся неделимыми, разрушались.
ГАЗЫ
Частицы газа находятся на большом расстоянии друг от друга и имеют высокую кинетическую энергию. Если пространство не ограничено, частицы газа будут разбросаны бесконечно; если оно ограничено, газ будет расширяться, чтобы заполнить весь объем. Когда газ оказывается под давлением, то есть уменьшается объем емкости, пространство между частицами уменьшается, а давление, оказываемое их столкновениями, увеличивается. Если объем сосуда поддерживается постоянным, но температура газа увеличивается, то давление также увеличивается. Частицы газа обладают достаточной кинетической энергией для преодоления межмолекулярных сил, которые удерживают твердые частицы и жидкости вместе, поэтому газ не имеет определенного объема и формы.
ПЛАЗМА
Плазма не является общим состоянием материи здесь, на Земле, но может быть самым распространенным состоянием материи во Вселенной. Плазма состоит из сильно заряженных частиц с чрезвычайно высокой кинетической энергией. Благородные газы (гелий, неон, аргон, криптон, ксенон и радон) часто используются для создания светильников, используя электричество для их ионизации в плазменное состояние. Звезды, по сути, являются перегретыми шарами плазмы.
КОНДЕНСАТ БОЗЕ-ЭЙНШТЕЙНА
В 1995 году технология позволила ученым создать новое состояние материи – конденсат Бозе-Эйнштейна (КБЭ). Используя комбинацию лазеров и магнитов, Эрик Корнелл и Карл Вейман охладили образец рубидия с точностью до нескольких градусов до абсолютного нуля. При этой чрезвычайно низкой температуре молекулярное движение очень близко к остановке. Так как кинетическая энергия почти не передается от одного атома к другому, атомы начинают сжиматься вместе. Уже не тысячи отдельных атомов, а один «супер атом». КБЭ используется для изучения квантовой механики на макроскопическом уровне. Свет, кажется, замедляется, когда он проходит через КБЭ, что позволяет изучать парадокс частиц/волн. КБЭ также обладает многими свойствами сверхтекучей жидкости без трения, также используются для моделирования условий, которые могут выполняться в черных дырах.
СМЕНА ФАЗЫ
Добавление энергии к веществу приводит к физическому изменению – материя переходит из одного состояния в другое. Например, добавление тепловой энергии – тепла – к жидкой воде приводит к тому, что она становится паром или газом. Извлечение энергии также приводит к физическим изменениям, например, когда жидкая вода становится льдом – твердой – при удалении тепла. Физическое изменение фазы также может быть вызвано движением и давлением.
ПЛАВЛЕНИЕ И ОТВЕРДЕВАНИЕ
Когда тепло прикладывается к твердому веществу, его частицы начинают быстрее вибрировать и склонны двигаться дальше друг от друга. Когда вещество при стандартном давлении достигает определенной точки, называемой точкой плавления, твердое вещество начинает превращаться в жидкость. Точку плавления чистого вещества часто можно определить с точностью до 0,1 градуса Цельсия, точкой, в которой твердая и жидкая фазы находятся в равновесии. Если вы продолжаете нагревать образец, температура не будет повышаться выше точки плавления, пока весь образец не будет сжижен. Тепловая энергия используется для преобразования твердого вещества в жидкую форму. Как только весь образец станет жидким, температура снова начнет расти. Соединения, которые в остальном очень похожи, могут иметь разные точки плавления, поэтому точка плавления может быть полезным способом различения среди них. Например, сахароза имеет точку плавления 186,1 градусов Цельсия, тогда как температура плавления глюкозы составляет 146 градусов Цельсия. Твердая смесь, такая как металлический сплав, часто может быть разделена на ее составные части путем нагревания смеси и извлечения жидкостей по мере достижения ими различных точек плавления.
Точка замерзания – это температура, при которой жидкое вещество достаточно охлаждается для образования твердого вещества. По мере охлаждения жидкости движение частиц замедляется. Во многих веществах частицы выравниваются точными геометрическими узорами для образования кристаллических твердых веществ. Большинство жидкостей сжимаются, когда они замерзают. Одной из важных характеристик воды является то, что она расширяется при замерзании, поэтому лед плавает. Если бы лед не плавал, не было бы жидкой воды под замерзшим льдом, и многие формы водной жизни были бы невозможны.
Температура замерзания часто близка к той же температуре, что и температура плавления, но не считается характерной для вещества, поскольку несколько факторов могут ее изменить. Например, добавление растворенных веществ в жидкость приведет к снижению температуры замерзания. Примером этого является использование суспензии соли для снижения температуры, при которой вода замерзает на наших дорогах. Другие жидкости можно охлаждать до температур, значительно ниже их температуры плавления, до того, как они начнут затвердевать. Такие жидкости называются суперохлаждаемыми и часто требуют наличия пылевой частицы или затравочного кристалла для начала процесса кристаллизации.
СУБЛИМАЦИЯ
Когда твердое вещество превращается непосредственно в газ без прохождения жидкой фазы, процесс известен как сублимация. Сублимация происходит, когда кинетическая энергия частиц больше атмосферного давления, окружающего образец. Это может произойти, когда температура образца быстро увеличивается за точку кипения (испарение вспышки). Чаще всего вещество может быть «высушено в замороженном состоянии» путем его охлаждения в условиях вакуума, так что вода в веществе подвергается сублимации и удаляется из образца. Несколько летучих веществ будут подвергаться сублимации при нормальной температуре и давлении. Наиболее известным из этих веществ является CO2 или сухой лед.
ПАРООБРАЗОВАНИЕ
Испарение представляет собой превращение жидкости в газ. Испарение может происходить путем испарения или кипения.
Поскольку частицы жидкости находятся в постоянном движении, они часто сталкиваются друг с другом, передавая при этом энергию. Этот перенос энергии имеет малое влияние внутри жидкости, но когда достаточная энергия передается частице вблизи поверхности, она может получить достаточную энергию, чтобы полностью удалиться из образца в виде частицы свободного газа. Этот процесс называется испарением, и он продолжается до тех пор, пока остается жидкость. Энергия, передаваемая поверхностным молекулам, вызывающая их вылет, уносится от оставшегося жидкого образца.
Когда к жидкости добавляется достаточно тепла, образуя пузырьки пара ниже поверхности, мы говорим, что жидкость кипит. Температура, при которой жидкость кипит, является переменной. Точка кипения зависит от давления вещества. Жидкость под более высоким давлением будет требовать больше тепла до того, как в ней могут образоваться пузырьки пара. На больших высотах атмосферном давлении ниже, чем при нормальных условиях, поэтому жидкость будет кипеть при более низкой температуре. Такое же количество жидкости на уровне моря находится под большим атмосферным давлением и будет кипеть при более высокой температуре.
КОНДЕНСАЦИЯ И ДЕСУБЛИМАЦИЯ
Конденсация – это когда газ превращается в жидкость. Конденсация происходит, когда газ охлаждается или сжимается до такой степени, что кинетическая энергия частиц больше не может преодолевать межмолекулярные силы. Первоначальный кластер частиц инициирует процесс, который имеет тенденцию дополнительно охлаждать газ, так что конденсация продолжается. Когда газ превращается непосредственно в твердое вещество, не проходя через жидкую фазу, процесс называется осаждением или десублимацией. Примером этого является то, как при пониженных температурах преобразуется водяной пар в атмосфере в иней и лед. Иней имеет тенденцию обрисовывать сплошные листья травы и веток, потому что воздух, касающийся этих твердых веществ, охлаждается быстрее, чем воздух, который не касается твердой поверхности.
Источник
Определение 1
Агрегатные состояния вещества(от лат. “aggrego” означает “присоединяю”, “связываю”) – это состояния одного и того же вещества в твердом, жидком и газообразном виде.
При переходе из одного состояния в другое наблюдается скачкообразное изменение энергии, энтропии, плотности и прочих свойств вещества.
Твердые и жидкие тела
Определение 2
Твердые тела – это тела, которые отличаются постоянством своей формы и объема.
В твердых телах межмолекулярные расстояния маленькие, а потенциальную энергию молекул можно сравнить с кинетической.
Твёрдые тела подразделяются на 2 вида:
- Кристаллические;
- Аморфные.
В состоянии термодинамического равновесия находятся только лишь кристаллические тела. Аморфные же тела по факту представляют собой метастабильные состояния, которые по строению схожи с неравновесными, медленно кристаллизующимися жидкостями. В аморфном теле происходит чересчур медленный процесс кристаллизации, процесс постепенного преобразования вещества в кристаллическую фазу. Разница кристалла от аморфного твердого тела состоит, в первую очередь, в анизотропии его свойств. Свойства кристаллического тела определяются в зависимости от направления в пространстве. Разнообразные процессы (например, теплопроводность, электропроводность, свет, звук) распространяются в разных направлениях твердого тела по-разному. А вот аморфные тела (например, стекло, смолы, пластмассы) изотропные, как и жидкости. Разница аморфных тел от жидкостей заключается лишь только в том, что последние текучие, в них не происходят статические деформации сдвига.
У кристаллических тел правильное молекулярное строение. Именно за счет правильного строения кристалл имеет анизотропные свойства. Правильное расположение атомов кристалла создает так называемую кристаллическую решетку. В разных направлениях месторасположение атомов в решетке различное, что и приводит к анизотропии. Атомы (ионы либо целые молекулы) в кристаллической решетке совершают беспорядочное колебательное движение возле средних положений, которые и рассматриваются в качестве узлов кристаллической решетки. Чем выше температура, тем выше энергия колебаний, а значит, и средняя амплитуда колебаний. В зависимости от амплитуды колебаний определяется размер кристалла. Увеличение амплитуды колебаний приводит к увеличению размеров тела. Таким образом, объясняется тепловое расширение твердых тел.
Определение 3
Жидкие тела – это тела, имеющие определенный объем, но не имеющие упругой формы.
Для вещества в жидком состоянии характерно сильное межмолекулярное взаимодействие и малая сжимаемость. Жидкость занимает промежуточное положение между твердым телом и газом. Жидкости, также как и газы, обладают изотpопными свойствами. Помимо этого, жидкость обладает свойством текучести. В ней, как и в газах, нет касательного напряжения (напряжения на сдвиг) тел. Жидкости тяжелые, то есть их удельные веса можно сравнить с удельными весами твердых тел. Вблизи температур кристаллизации их теплоемкости и прочие тепловые свойства близки к соответствующим свойствам твердых тел. В жидкостях наблюдается до заданной степени правильное расположение атомов, но только лишь в маленьких областях. Здесь атомы также проделывают колебательное движение около узлов квазикристаллической ячейки, однако в отличие от атомов твердого тела они периодически перескакивают от одного узла к другому. В итоге движение атомов будет весьма сложное: колебательное, но вместе с тем центр колебаний перемещается в пространстве.
Газ, испарение, конденсация и плавление
Определение 4
Газ – это такое состояние вещества, при котором расстояния между молекулами огромны.
Силами взаимодействия между молекулами при небольших давлениях можно пренебречь. Частицы газа заполоняют весь объем, который предоставлен для газа. Газы рассматривают как сильно перегретые либо ненасыщенные пары. Особый вид газа – плазма (частично или полностью ионизированный газ, в котором плотности положительных и отрицательных зарядов почти одинаковые). То есть плазма – это газ из заряженных частиц, взаимодействующих между собой при помощи электрических сил на большом расстоянии, но не имеющих ближнего и дальнего расположения частиц.
Как известно, вещества способны переходить из одного агрегатного состояния в другое.
Определение 5
Испарение – это процесс изменения агрегатного состояния вещества, при котором с поверхности жидкости либо твердого тела вылетают молекулы, кинетическая энергия которых преобразовывает потенциальную энергию взаимодействия молекул.
Испарение является фазовым переходом. При испарении часть жидкости или твердого тела преобразуется в пар.
Определение 6
Вещество в газообразном состоянии, которое находится в динамическом равновесии с жидкостью, называется насыщенным паром. При этом изменение внутренней энергии тела равняется:
∆U=±mr (1),
где m – это масса тела, r – это удельная теплота парообразования (Дж/кг).
Определение 7
Конденсация представляет собой процесс, обратный парообразованию.
Изменение внутренней энергии рассчитывается по формуле (1).
Определение 8
Плавление – это процесс преобразования вещества из твердого состояния в жидкое, процесс изменения агрегатного состояния вещества.
При нагревании вещества растет его внутренняя энергия, поэтому увеличивается скорость теплового движения молекул. При достижении веществом своей температуры плавления кристаллическая решетка твердого тела разрушается. Связи между частицами также разрушаются, растет энергия взаимодействия между частицами. Теплота, которая передается телу, идет на увеличение внутренней энергии данного тела, и часть энергии расходуется на совершение работы по изменению объема тела при его плавлении. У многих кристаллических тел объем увеличивается при плавлении, однако есть исключения (к примеру, лед, чугун). Аморфные тела не обладают определенной температурой плавления. Плавление представляет собой фазовый переход, который характеризуется скачкообразным изменением теплоемкости при температуре плавления. Температура плавления зависит от вещества и она остается неизменной в ходе процесса. Тогда изменение внутренней энергии тела равняется:
∆U=±mλ (2),
где λ – это удельная теплота плавления (Дж/кг).
Определение 9
Кристаллизация представляет собой процесс, обратный плавлению.
Изменение внутренней энергии рассчитывается по формуле (2).
Изменение внутренней энергии каждого тела системы при нагревании или охлаждении вычисляется по формуле:
∆U=mc∆T (3),
где c – это удельная теплоемкость вещества, ДжкгК, △T – это изменение температуры тела.
Определение 10
При рассматривании преобразований веществ из одних агрегатных состояний в другие нельзя обойтись без так называемого уравнения теплового баланса: суммарное количество теплоты, выделяемое в теплоизолированной системе, равняется количеству теплоты (суммарному), которое в данной системе поглощается.
Q1+Q2+Q3+…+Qn=Q’1+Q’2+Q’3+…+Q’k.
По сути, уравнение теплового баланса – это закон сохранения энергии для процессов теплообмена в термоизолированных системах.
Пример 1
В теплоизолированном сосуде находятся вода и лед с температурой ti=0°C. Масса воды mυ и льда mi соответственно равняется 0,5 кг и 60 г. В воду впускают водяной пар массой mp=10 г при температуре tp=100°C. Какой будет температура воды в сосуде после того, как установится тепловое равновесие? При этом теплоемкость сосуда учитывать не нужно.
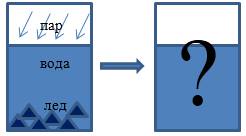
Рисунок 1
Решение
Определим, какие процессы осуществляются в системе, какие агрегатные состояния вещества мы наблюдали и какие получили.
Водяной пар конденсируется, отдавая при этом тепло.
Тепловая энергия идет на плавление льда и, может быть, нагревание имеющейся и полученной изо льда воды.
Прежде всего, проверим, сколько теплоты выделяется при конденсации имеющейся массы пара:
Qp=-rmp;Qp=2,26·106·10-2=2,26·104 (Дж),
здесь из справочных материалов у нас есть r=2,26·106 Джкг – удельная теплота парообразования (применяется и для конденсации).
Для плавления льда понадобится следующее количество тепла:
Qi=λmiQi=6·10-2·3,3·105≈2·104 (Дж),
здесь из справочных материалов у нас есть λ=3,3·105 Джкг – удельная теплота плавления льда.
Выходит, что пар отдает тепла больше, чем необходимо, только для расплавления имеющегося льда, значит, уравнение теплового баланса запишем следующим образом:
rmp+cmp(Tp-T)=λmi+c(mυ+mi)(T-Ti).
Теплота выделяется при конденсации пара массой mp и остывании воды, образуемой из пара от температуры Tp до искомой T. Теплота поглощается при плавлении льда массой mi и нагревании воды массой mυ+mi от температуры Ti до T. Обозначим T-Ti=∆T для разности Tp-T получаем:
Tp-T=Tp-Ti-∆T=100-∆T.
Уравнение теплового баланса будет иметь вид:
rmp+cmp(100-∆T)=λmi+c(mυ+mi)∆T;c(mυ+mi+mp)∆T=rmp+cmp100-λmi;∆T=rmp+cmp100-λmicmυ+mi+mp.
Сделаем вычисления с учетом того, что теплоемкость воды табличная
c=4,2·103 ДжкгК, Tp=tp+273=373 К, Ti=ti+273=273 К:∆T=2,26·106·10-2+4,2·103·10-2·102-6·10-2·3,3·1054,2·103·5,7·10-1≈3 (К),
тогда T=273+3=276 К
Ответ: Температура воды в сосуде после установления теплового равновесия будет равняться 276 К.
Пример 2
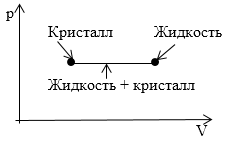
На рисунке 2 изображен участок изотермы, который отвечает переходу вещества из кристаллического в жидкое состояние. Что соответствует данному участку на диаграмме p,T?

Рисунок 2
Ответ: Вся совокупность состояний, которые изображены на диаграмме p,V горизонтальным отрезком прямой на диаграмме p,T показано одной точкой, которая определяет значения p и T, при которых происходит преобразование из одного агрегатного состояния в другое.
Источник
