Какое число молекул содержится в 100 г воды
1
Сколько молекул содержится в 1 см3 воды? Какова масса молекулы воды? Каков приблизительный размер молекулы воды?
Ответ и решение
n = 3,33·1022 1/см3; m = 2,99·10-26 кг; a = 3,11·10-10 м.
Масса 1 моля воды составляет 18 г, а его объем V — 18 см3. В 1 моле воды содержится число молекул, равное постоянной Авогадро NА = 6·1023. Число молекул в 1 см3n = NА/V = 3,33·1022. Масса одной молекулы m = 18/NА = 3·10-26 кг. Объем V0 одной молекулы приблизительно равен 1/n см3. Тогда размер молекулы составит
.
2
Хорошо откачанная лампа накаливания объемом 10 см3 имеет трещину, в которую ежесекундно проникает миллион частиц газа. Сколько времени понадобится для наполнения лампы до нормального давления, если скорость проникновения газа остается постоянной? Температура 0 °С.
Ответ и решение
t ≈ 8,5 млн. лет.
Найдем число частиц газа, необходимое для наполнения лампы:
N = VNЛ = 10·2,69·1019 см3·см-3 = 2,69·1020,
где V – объем лампы, NЛ – постоянная Лошмидта.
Время, необходимое для наполнения лампы со скоростью v = 106 с-1, равно:
t = N/v = 2,69·1020/(106·с-1) = 2,69·1014 c ≈ 8,5 млн. лет.
3
За 10 суток полностью испарилось из стакана 100 г воды. Сколько в среднем вылетало молекул с поверхности воды за 1 с?
Ответ и решение
≈ 3,8·1018 молекул в секунду.
Переведем время t испарения воды из суток в секунды:
t = 10 сут. = 8,64·105 с.
Поскольку 1 моль воды имеет массу 18 г, то, используя постоянную Авогадро, можно найти число N молекул в 100 г воды:
N = NА·100/18 = 3,3·1024 шт.
Теперь найдем скорость v испарения воды:
v = N/t ≈ 3,8·1018 c-1.
4
В озеро средней глубиной 10 м и площадью 10 км2 бросили кристаллик поваренной соли NaCl массой 0,01 г. Сколько ионов хлора оказалось бы в наперстке воды объемом 2 см3, зачерпнутом из этого озера, если считать, что соль, растворившись, равномерно распределилась в озере?
Ответ и решение
≈ 2·106 ионов.
1 моль поваренной соли имеет массу 58,5 г, из которых 23 г — масса натрия, а 35,5 г — масса хлора. Чтобы рассчитать массу хлора в брошенном кристаллике хлора, решим систему из двух уравнений:
m(Na) + m(Cl) = 0,01
m(Na)/m(Cl) = 0,65
Из системы получим, m(Cl) = 6·10-3 г.
Теперь можно вычислить число частиц хлора N(Cl):
N(Cl) = NA· 6·10-3/35,5 ≈ 1020 ионов хлора.
Число ионов хлора в наперстке будет меньше полученного числа во столько раз, во сколько раз объем наперстка меньше объема озера. Найдем это число:
N = 1020·2·10-6/108 = 2·106 ионов хлора в наперстке.
5
Кристаллы поваренной соли NaCl кубической системы состоят из чередующихся атомов (ионов) Na и Cl.

Определить наименьшее расстояние между их центрами. Молярная масса поваренной соли ν = 58,5 г/моль, а ее плотность ρ = 2,2 г/см3.
Ответ и решение
r = 2,83·10-8 см.
Найдем сторону a куба, который занимает объем одного моля поваренной соли:
a =  = 3 см.
= 3 см.
Найдем, какое число ионов натрия и хлора приходится на одно ребро куба (общее число ионов натрия и хлора в 1 моле поваренной соли равно удвоенному числу молекул NaCl, т.е. 2NА):
n = 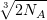 ≈ 108 ионов.
≈ 108 ионов.
Теперь найдем расстояние между ионами:
l = a/n = 2,83·10-8 см.
6
Кубическая кристаллическая решетка железа содержит один атом железа на элементарный куб, повторяя который, можно получить всю решетку кристалла. Определить расстояние между ближайшими атомами железа, если плотность железа ρ = 7,9 г/см3, атомная масса А = 56.
Ответ и решение
2,3·10-8 см.
Найдем сторону a куба, который занимает объем одного моля железа:
a =  = 1,9 см.
= 1,9 см.
Найдем, какое число атомов железа приходится на одно ребро куба (общее число атомов железа в 1 моле равно NА):
n = ≈ 8,4·107 атомов.
≈ 8,4·107 атомов.
Теперь найдем расстояние между атомами железа:
l = a/n = 2,3·10-8 см.
7
На пути молекулярного пучка стоит «зеркальная» стенка. Найти давление, испытываемое этой стенкой, если скорость молекул в пучке v = 103 м/с, концентрация n = 5·1017 1/м3, масса m = 3,32·10-27 кг. Рассмотреть три случая: а) стенка расположена перпендикулярно скорости пучка и неподвижна; б) пучок движется по направлению, составляющему со стенкой угол α = 45°; в) стенка движется навстречу молекулам со скоростью u = 50 м/с.
Ответ
а) pа ≈ 3,3·10-3 Па; б) pб ≈ 2,4·10-3 Па; в) pв ≈ pа.
8
Как изменилось бы давление в сосуде с газом, если бы внезапно исчезли силы притяжения между его молекулами?
Ответ
Источник
Грамм-атом и грамм-молекула являются химическими мерами веса, широко применяющимися в расчетах.
Грамм-атомом (г-атом) называется количество граммов элемента, численно равное его атомному весу. Например, если атомный вес кислорода равен 16 у.е., то грамм-атом кислорода равен 16 г. Если атомный вес серы равен 32 у.е., то ее грамм-атом равен 32 г. Грамм-атом водорода равен 1 г.
Если сравнить между собой грамм-атомы различных элементов, то нетрудна прийти к выводу, что в них содержится одинаковое число атомов. Например, возьмем 1 г водорода и 1 г кислорода. Если сравнить между собой атомы кислорода и водорода по весу, то атом кислорода в 16 раз тяжелее атома водорода, поэтому в 1 г водорода будет содержаться в 16 раз больше атомов, чем в 1 г кислорода, а чтобы иметь столько же атомов кислорода, сколько имеется атомов водорода в 1 г водорода, надо взять 16 г кислорода.
На 1г водорода — это грамм-атом водорода, а 16 г кислорода — это грамм-атом кислорода. Следовательно, в грамм-атомах водорода и кислорода содержится одинаковое количество атомов. Так как подобное рассуждение можно провести для любого элемента, то ясно, что в грамм-атоме любого элемента содержится одно и то же число атомов.
Грамм-молекулой (или молем) называется количество граммов вещества, численно равное его молекулярному весу. Например, 1 моль Н2O равен 18 г.
В 1 моле любого вещества содержится одно и то же число молекул. Это число, равное количеству атомов в грамм-атоме и высчитанное итальянским химиком Авогадро, равно 6,02-1023 частиц. Оно получило название числа Авогадро.
Если нужно вычислить, в каком количестве едкого натра NaOH содержится столько же молекул, сколько в 9 г воды, то поступают так:
1 моль NaOH = 23 + 16 + 1 = 40г 1 моль Н2О = 2+16=18г
Далее подсчитывают, какую долю грамм-молекулы воды составляют 9 г:
9:18 = 0,5 моля.
Так как в 1 моле любого вещества содержится одинаковое число молекул, то в равных долях грамм-молекул разных веществ также содержится одно и то же число молекул. Очевидно, чтобы иметь столько же молекул NaOH, сколько их содержится в 0,5 моля воды, мы должны взять 0,5 моля NaOH, т. е. 40 · 0,5 = 20 г едкого натра.
■ 1. Что такое грамм-атом? (См. Ответ)
2. Что такое грамм-молекула?
3. Правильно ли сказать: а) что 1 г кислорода и 1 грамм-атом кисло-
рода — это одно и то же; б) что 1 г водорода и 1 грамм-атом водорода — это одно и то же? Почему?
4. Как доказать, что в 1 грамм-атоме любого элемента содержится
одно и то же число атомов?
5. Что такое число Авогадро?
6. В каком количестве меди Си содержится столько же атомов, сколько их находится в 16 г серы S? (См. Ответ)
7. Сколько нужно взять серной кислоты H2SO4 чтобы иметь столько же молекул, сколько их содержится в 9 г воды? (См. Ответ)
2. Расчеты по формулам
Пользуясь понятием о грамм-атоме и грамм-молекуле, можно производить простейшие расчеты.
Пример 1. Рассчитайте, сколько железа Fe содержится в 116 г магнитной окиси железа Fe3O4.
Дано: 116 г Fe3O4
Найти: Fe (г) ?
Решение:
Атомный вес железа равен 56 у.е.; 1 грамм-атом = 56 г. Атомный вес кислорода равен 16 у.е.; 1 грамм-атом О = 16 г. Молекулярный вес магнитной окиси железа равен
56 · 3+ 16 · 4 = 232 у. е.
1 моль Fe3O4 = 232 г. Далее рассуждаем так: в 232 г Fe3O4 содержится 56-3 = 168 г Fe » 116 » Fe3O4 » х » Fe,
где за х принимается неизвестное количество железа, содержащееся в 116 г.
Составим и решим пропорцию: 232:116 = 168 : x
x = (168 · 116) : 232 = 84 г Fe
Ответ: в 116 г магнитной окиси железа содержится 84 г железа.
Пример 2. В каком количестве окиси ртути HgO содержится 100 г ртути Hg.
Дано: 100 г Hg
Найти: HgO (г) ?
Решение:
Атомный вес ртути равен 200 у.е.; 1 грамм-атом Hg = 200 г.
Атомный.вес кислорода равен 16 у.е.; 1 грамм-атом О = 16 г. Молекулярный вес окиси ртути равен 200 + 16 = 216 у.е.; 1 моль HgO = 216 г.
Примем неизвестное количество окиси ртути за х. Далее рассуждаем так: в 216 г HgO содержится 200 г Hg » x » HgO » 100 » Hg
Составим и решим пропорцию:
216 : x = 200:100
x = (100 · 216) : 200 = 108 г HgO
Ответ: 100 г ртути содержится в 108 г окиси ртути.
Пример 3. Сколько грамм-атомов железа Fe содержится в 4 молях сульфида железа FeS?
Дано: 4 моля FeS
Найти: Fe (г-атом)?
Решение:
Примем неизвестное количество грамм-атомов железа за х. Далее рассуждаем так.
В 1 молекуле сернистого железа содержится 1 атом железа.
Следовательно, в 1 моле FeS содержится 1 грамм-атом железа. Но у нас не один, а 4 моля FeS. В данном случае и без пропорции ясно, что в 4 молях FeS содержится 4 грамм-атома железа.
Пример 4. В каком количестве грамм-молекул медного купороса CuSO4 содержится 2 грамм-атома кислорода?
Дано: 2 грамм-атома О
Найти: CuSO4 (моль) ?
Решение:
Примем неизвестное количество грамм-молекул медного купороса за х. Далее рассуждаем так: в 1 молекуле CuSO4 содержится 4 атома О. Следовательно, в 1 моле CuSO4 содержится 4 грамм-атома О, а в х молях CuSO4 содержится 2 грамм-атома О.
Составим и решим пропорцию: 1 : x = 4 : 2;
x = (2 · 1) : 4 = 0,5 моля CuSO4
Ответ: в 0,5 моля медного купороса содержится 2 грамм-атома кислорода.
Пример 5. Сколько граммов натрия Na содержится в 6 молях поваренной соли NaCl?
Дано: 6 молей NaCl
Найти: Na (г) ?
Решение:
В 1 молекуле NaCl содержится 1 а том Na, а в 1 моле NaCl содержится 1 грамм-атом Na. Соответственно в 6 молях NaCl содержится 6 грамм-атомов Na.
Итак, мы определили количество натрия, но только в грамм-атомах, а нам требуется определить его в граммах. Для этого нужно проделать несложный расчет, чтобы перевести грамм-атомы в граммы. Атомный вес Na23 у.е.; 1 грамм-атом Na = 23 г, а у нас 6 грамм-атомов Na. Их вес 23 · 6 = 138 г.
Ответ: в 6 молях поваренной соли содержится 138 г натрия.
Пример 6. Сколько грамм-атомов железа Fe содержится в 304 г железного купороса FeSO4?
Дано: 304 г FeSO4
Найти: Fe (г-атом) ?
Решение:
Рассчитаем сначала, какое количество граммов железа содержится в 304 г FeSO4. Атомный вес железа равен 56 у.е.; 1 грамм-атом Fe равен 56 г.
Атомный вес серы равен 32 у.е.; 1 грамм-атом S равен 32 г. Атомный вес кислорода равен 16 у.е.; 1 грамм-атом кислорода равен 16 г.
Грамм-молекула FeSO4 равна 56 + 32 + 16 · 4 = 152 г.
в 152 г FeSO4 содержится 56 г Fe » 304 » FeSO4 » х » Fe
Составим и решим пропорцию: 152 : 304 = 56 : x.
x = (304 · 56) : 152 = 112 г Fe.
Теперь надо перевести граммы железа в грамм-атомы. 1 грамм-атом Fe = 56 г, следовательно, 112 г составляют 2 грамм-атома Fe.
Ответ: в 304 г железного купороса содержится 2 грамм-атома железа.
■ 8. Сколько граммов железа содержится в 44 г сульфида железа FeS? (См. Ответ)
9. В каком количестве карбоната меди CuCO3 содержится 32 г меди Сu?
10. Сколько грамм-атомов кислорода содержится в 5 молях воды?
11. Сколько граммов серебра содержится в 7 молях нитрата серебра AgNO3?
12. Сколько грамм-атомов ртути содержится в 434 г окиси ртути HgO? (См. Ответ)
3. Расчеты по уравнениям реакций
Пользуясь понятиями «грамм-атом» и «грамм-молекула», можно производить расчеты по уравнениям реакций.
По уравнениям реакций можно рассчитать количество образующегося продукта реакции или количество сырья, необходимого для получения того или иного продукта.
Пример 1. Определите, какое количество ртути Hg образуется при разложении 21,6 г окиси ртути HgO.
Дано: 21,6 г HgO
Найти: Hg (г) ?
Решение:
При решении таких задач прежде всего необходимо написать уравнение реакции:
2HgO = 2Hg + O2
Вещество, количество которого нам дано, мы подчеркнем одной чертой, а то вещество, которое требуется определить,— двумя чертами и под ними поставим грамм-молекулярный вес этих соединений. Если имеется коэффициент, грамм-молекулярный вес на него умножается:
2HgO : (216 · 2) = 2Hg : (200 · 2) + O2
Затем производим расчет. По нашему уравнению из 432 г HgO получается 400 r Hg, а из 21,6 г HgO получается х г Hg
x = (21,6 · 400) : 432 = 20 г Hg
Ответ. Из 21,6г HgO можно получить 20 г Hg.
Пример 2. Какое количество железа потребуется для вытеснения 0,5 грамм-атома меди Сu из медного купороса CuSO4?
Дано: 0,5 г-атома Сu
Найти: Fe (г) ?
Решение:
Последовательность решения совершенно такая же, как и в предыдущей задаче. Разница лишь в том, что в первой задаче нужно было определить вес продукта реакции по исходному веществу, а здесь, наоборот, определяется количество исходного вещества по продукту реакции. Составляем уравнение реакции и подчеркиваем нужные нам вещества:
Fe : (56г) + CuSO4 = FeSO4 + Cu : (64г)
Здесь за х мы примем неизвестное количество железа. Рассуждаем следующим образом. По уравнению реакции для вытеснения 1 грамм-атома меди требуется 1 грамм-атом железа. Соответственно для вытеснения 0,5 грамм-атома меди необходимо 0,5 грамм-атома железа, которые составляют 56 · 0,5 = 28 г.
Ответ: для вытеснения 0,5 грамм-атома меди требуется 28 г железа.
■ 13. Какое количество жженой магнезии MgO образуется при сжигании магния Mg в 5 молях кислорода O2? (См. Ответ)
14. Сколько алюминия Аl потребуется для получения 51 г окиси алюминия Аl2O3 при окислении алюминия кислородом воздуха?
15. Сколько сульфида ртути HgS получится при растирании с серой 2 г ртути Hg?
16. Сколько грамм-молекул воды получится при сжигании в кислороде 7 грамм-молекул водорода Н2? (См. Ответ)
Статья на тему Грамм атом грамм-молекула
Источник
Задачи на применение формул количества вещества
(А) Определите молярную массу ацетилена (С2Н2). (А) Какое количество вещества содержится в алюминиевом подстаканнике массой 100 г? (А) Определите массу водорода, взятого в количестве 103 моль. (А) Вычислите массу одной молекулы водорода и кислорода. (А) Определите плотность пропана (С3Н8) при нормальных условиях. (Объем любого газа, взятого в количестве 1 моль, при нормальных условиях равен 22,4 л.) (А) Какова температура газа, находящегося под давлением 0,5 МПа, если в сосуде объемом 15 л содержится 1,8 · 1024 молекул? Газ считать идеальным. (В) Современные вакуумные насосы позволяют понижать давление до значения, равного 1,33 · 10-10 Па. Сколько молекул газа содержится в 1 см3 при указанном давлении и температуре 48 0С? (В) Мельчайшая капелька воды имеет массу 10-10 г. Из скольких молекул она состоит? (В) Определите объем и диаметр атома алюминия, считая, что в твердом алюминии атомы имею форму шара. (В) В сосуде находится газ под давлением 150 кПа при температуре 273 0С. Какое количество молекул находится при этих условиях в единице объема сосуда? (В) За 10 суток полностью испарилось из стакана 100 г воды. Сколько в среднем вылетало молекул с поверхности воды за 1 с? (С) Сколько молекул газа содержится в колбе вместимостью 500 см3 при нормальных условиях? (С) Число молекул, содержащихся в единице объема неизвестного газа, при нормальных условиях равно 2,7 · 1025 м-3. Этот же газ при температуре 91 0С и давлении 800 кПа имеет плотность 5,4 кг/м3. Определите массу одной молекулы этого газа. (С) Диаметр молекулы азота примерно равен 3 · 10-8 см. Считая, что молекулы имеют сферическую форму, определите, какая часть (в %) объема, занимаемого газом, приходится на объем самих молекул при нормальных условиях. Газ считать идеальным.
Решение задач на применение формул количества вещества (физика 10)
Решение не комментирую. Кто желает понять, разберется. Можно поучить в учебнике «Физика 10, , Москва «Просвещение» 2004»
М(С2Н2) = Мr · 10-3 = (12 · 2 + 2 · 2) · 10-3 = 2,6 · 10-2 кг/моль
Дано: Решение:
m(Al) = 100 г = 0,1 кг М(Al) = 2,7 · 10-2 кг/моль
ν – ?
Ответ: 3,7 моль
Дано: Решение:
ν(Н2) = 103 моль m = νМ М(Н2) = 2 · 10-3 кг/моль
m = 103 · 2 · 10-3 = 2 кг
m(Н2) – ?
Ответ: 2 кг
Дано: Решение:
N(Н2) = 1 М = m0NА
N(О2) = 1 m0 = М/NA М(Н2) = 2 · 10-3 кг/моль
М(О2) = 3,2 · 10-2 кг/моль
m0(Н2) – ? m0(Н2) = 2 · 10-3/ 6 · 1023 = 3,3 · 10-27 кг
m0(О2) – ? m0(О2) = 3,2 · 10-2/ 6 · 1023 = 5,3 · 10-26 кг
Ответ: 3,3 · 10-27 кг; 5,3 · 10-26 кг
Дано:
V(С3Н8) = 22,4 л = 2,24 · 10-2 м3 Решение:
ν(С3Н8) = 1 моль ρ = m/V М(С3Н8) = 4,4 · 10-2 кг/моль
m(С3Н8) = νМ = 1 · 4,4 · 10-2 = 4,4 · 10-2 кг
ρ(С3Н8) – ? ρ = 4,4 · 10-2/ 2,24 · 10-2 = 1,96 кг/м3
Ответ: 1,96 кг/м3
Дано: Решение:
Р = 0,5 МПа = 5 · 105Па
V = 15 л = 1,5 · 10-2 м3
N = 1,8 · 1024
Т – ? T = 5 · 105 · 1,5 · 10-2 · 6 · 1023/ 1,8 · 1024 · 8,31
Т = 301 К
Ответ: 301 К
Дано: Решение:
Р = 1,33 · 10-10 Па
V = 1 см3 = 10-6 м3
t = 48 0С = 321 К N = 1,33 · 10-10 · 10-6 · 6 · 1023/8,31 · 321
N – ? N = 3 · 104
Ответ: 3 · 104
Дано: Решение:
m(Н2О) = 10-10 г = 10-13 кг N = mNA/M M(Н2О) = 1,8 · 10-2 кг/моль
N – ? N = 10-13 · 6 · 1023/1,8 · 10-2
N = 3 · 1012
Ответ: 3 · 1012
Дано: Решение:
атом Аl V = m/ρ m = NM/NA M(Аl) = 2,7 · 10-2 кг/моль
m = 1 · 2,7 · 10-2/6 · 1023
V -? m = 4,5 · 10-26 кг
d – ? ρ = 2700 кг/м3
V = 4,5 · 10-26/2,7 · 103
V = 1,7 · 10-29 м3
d = 7,6 · 10-11 м
Ответ: 1,7 · 10-29 м3; 7,6 · 10-11 м
Дано: Решение:
Р = 150 кПа = 1,5 · 105 Па
t = 273 0С = 546 К
V = 1 м3
N = 1,5 · 105 · 1 · 6 · 1023/8,31 · 546
N – ? N = 2 · 1025
Ответ: 2 · 1025
Дано: Решение:
t1 = 10 сут 10 сут = 864000 с
m = 100 г = 0,1 кг N = NAm/M M(Н2О) = 1,8 · 10-2 кг/моль
t2 = 1 с N = 6 · 1023· 0,1/ 1,8 · 10-2
N = 3,3 · 1024
N/t – ? N/t = 3,3 · 1024/8,64 · 105 = 3,8 · 1018
Ответ: 3,8 · 1018
Дано: Решение:
V = 500 см3 = 5 · 10-4 м3
T = 273 К
Р = 101325 Па
N = 101325 · 5 · 10-4 · 6 · 1023/8,31 · 273
N – ? N = 1,34 · 1022
Ответ: 1,34 · 1022
Дано: Решение:
V1 = 1 м3
T1 = 273 K m0 = m/N m = ρV P1V1/T1 = P2V2/T2
Р1 = 101325 Па
N = 2,7 · 1025 м-3 V2 = P1V1T2/P2T1
Т2 = 91 0С = 364 К V2 = 101325 · 1 · 364/8 · 105 · 273
Р2 = 800 кПа = 8 · 105 Па V2 = 0,17 м3
ρ = 5,4 кг/м3 m = 5,4 · 0,17 = 0,91 кг
m0 – ? N = 8 · 105 · 0,17 · 6 · 1023/8,31 · 364 = 2,68 · 1025
m0 = 0,91/2,68 · 1025 = 0,34 · 10-26 кг
Ответ: 0,34 · 10-26 кг
Дано: Решение:
d(N2) = 3 · 10-8 см = 3 · 10-10 м
V = 22,4 л = 2,2 · 10-2 м3 V1молекулы= 3,14 · (3 · 10-10)3/6 = 14,13 · 10-30
V1 моля = 14,13 · 10-30 · 6 · 1023 = 8,478 · 10-6 м3
φ – ? 2,24 · 10-2 — 100%
8,478 · 10-6 — φ%
φ = 8,478 · 10-6 · 100/2,24 · 10-2
φ = 0,0378%
Ответ: 0,0378%
Источник
Решениие задач по химии на закон Авогадро
Задача 53.
Сопоставить числа молекул, содержащихся в 1г NH3 и в 1г N2. В каком случае и во сколько раз число молекул больше?
Решение:
В одном моле любого вещества содержится 6,02 . 1023 молекул этого вещества.
Рассчитаем содержание количества вещества в 1г NH3 и N2 по формуле:
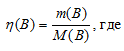
 (B) – количество вещества (В);
(B) – количество вещества (В);
m(B)- масса вещества (В);
M(B) – Молярная масса вещества (В).
М(NH3) = 17г/моль, M(N2) = 28г/моль.
Тогда
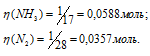
Число молекул NH3 больше числа молекул N2, так как  (NH3) >
(NH3) > (N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
(N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
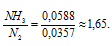
Ответ: в 1,65 раз число молекул NH3 больше числа молекул N2.
Задача 54.
Выразить в граммах массу одной молекулы диоксида серы.
Решение:
Находим молекулярную массу диоксида серы:
M(SO2) = 32 + (16 . 2) = 64г/моль.
Молекулярная масса численно составляет массу одного моля вещества, а значит, вес одного моля численно равен молекулярной массе и составляет 64г. Известно, что в одном моле любого вещества содержится 6,02 . 1023 молекул данного вещества. Исходя из этого, рассчитаем массу в граммах одной молекулы диоксида серы:
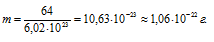
Ответ: масса одной молекулы диоксида серы равна.
Задача 55.
Одинаково ли число молекул в 0,001кг Н2 и в 0,001кг О2? В 1 моле Н2 и в 1 моле 02? В 1л Н2 и в 1л О2 при одинаковых условиях?
Решение:
Молекулярные массы водорода и кислорода равны соответственно 2г/моль и 32г/моль. Отсюда находим количество водорода и кислорода, зная их массы:
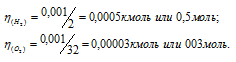
Один моль любого вещества содержит 6,02 .1023 молекул. Следовательно, в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул:

Так как имеется по одному молю водорода и кислорода, то количество молекул веществ будет одинаково:
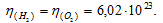
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1л водорода и в 1л кислорода:
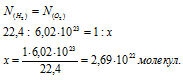
Ответ: а) в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул; б) в одном моле водорода и в одном моле кислорода содержится одинаковое число молекул: в) в одном литре водорода и в одном литре кислорода содержится одинаковое число молекул.
Задача 56.
Сколько молекул содержится в 1,00 мл водорода при нормальных условиях?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 .1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1мл водорода из пропорции:
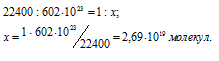
Ответ: 2,69 .1019 молекул.
Задача 57.
Какой объем при нормальных условиях занимают 27 .1021 молекул газа?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда находим какой объём при нормальных условиях занимают 27 .1021 молекул газа, составив пропорцию:
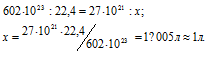
Ответ: V=1л.
Задача 58.
Каково соотношение объемов, занимаемых 1 молем О2 и 1 молем О3 (условия одинаковые)?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Следовательно соотношение объёмов, занимаемых одним молем О2 и одним молем О3 иметь вид:
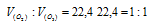
Ответ: 1:1
Задача 59.
Взяты равные массы кислорода, водорода и метана при одинаковых условиях. Найти отношение объемов взятых газов.
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Мольные массы кислорода, водорода и метана, соответственно равны 32 г/моль; 2г/моль; 16 г/моль.
Так как массы кислорода, водорода и метана одинаковы при одинаковых условиях, то отношение объёмов взятых газов находим из пропорции:
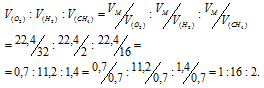
Ответ: 1:16:2.
Задача 60.
На вопрос, какой объем займет 1моль воды при нормальных условиях, получен ответ: 22,4л. Правильный ли это ответ?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Так как вода при нормальных условиях находится в жидкой, а не в газообразной фазе, то ответ, что 1моль воды займёт 22,4л не правильный. Учитывая, что молярная масса воды равна 18г/моль, а плотность равна единице, то правильный ответ будет равен:
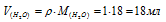
Ответ: 18мл.
Задача 61.
Сколько молекул диоксида углерода находится в 1л воздуха, если объемное содержание СО2 составляет 0,03% (условия нормальные)?
Решение:
При нормальных условиях углекислый газ, содержащийся в 1л воздуха, занимает объём 0,0003л. Зная, что мольный объём любого газа занимает 22,4л, рассчитаем число молей углекислого газа в 0,0003л из пропорции:
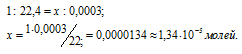
Учитывая, что в одном моле вещества содержится 6,02 . 1023 молекул, находим число молекул в 0,0003л газа:

Ответ: 8,07 .1018 молекул.
Источник
