Какое из веществ проявляет как свойства кислот так и свойства альдегидов
Химические свойства альдегидов и кетонов
Альдегидами называют соединения, молекулы которых содержат карбонильную группу, соединенную с атомом водорода, т.е. общая формула альдегидов может быть записана как
где R – углеводородный радикал, который может быть разной степени насыщенности, например, предельный или ароматический.
Группу –СНО называют альдегидной.
Кетоны – органические соединения, в молекулах которых содержится карбонильная группа, соединенная с двумя углеводородными радикалами. Общую формулу кетонов можно записать как:
где R и R’ – углеводородные радикалы, например, предельные (алкилы) или ароматические.
Гидрирование альдегидов и кетонов
Альдегиды и кетоны могут быть восстановлены водородом в присутствии катализаторов и нагревании до первичных и вторичных спиртов соответственно:
Окисление альдегидов
Альдегиды легко могут быть окислены даже такими мягкими окислителями, как гидроксид меди и аммиачный раствор оксида серебра.
При нагревании гидроксида меди с альдегидом происходит исчезновение изначального голубого окрашивания реакционной смеси, при этом образуется кирпично-красный осадок оксида одновалентной меди:
В реакции с аммиачным раствором оксида серебра вместо самой карбоновой кислоты образуется ее аммонийная соль, поскольку находящийся в растворе аммиак реагирует с кислотами:
Кетоны в реакцию с гидроксидом меди (II) и аммиачным раствором оксида серебра не вступают. По этой причине эти реакции являются качественными на альдегиды. Так реакция с аммиачным раствором оксида серебра при правильной методике ее проведения приводит к образованию на внутренней поверхности реакционного сосуда характерного серебряного зеркала.
Очевидно, что если мягкие окислители могут окислить альдегиды, то само собой это могут сделать и более сильные окислители, например, перманганат калия или дихромат калия. При использовании данных окислителей в присутствии кислот образуются карбоновые кислоты:
Химические свойства карбоновых кислот
Карбоновыми кислотами называют производные углеводородов, содержащие одну или несколько карбоксильных групп.
Карбоксильная группа:
Как можно видеть, карбоксильная группа состоит из карбонильной группы –С(О)- , соединенной с гидроксильной группой –ОН.
В связи с тем, что к гидроксильной группе непосредственно прикреплена карбонильная, обладающая отрицательным индуктивным эффектом связь О-Н является более полярной, чем в спиртах и фенолах. По этой причине карбоновые кислоты обладают заметно более выраженными, чем спирты и фенолы, кислотными свойствами. В водных растворах они проявляют свойства слабых кислот, т.е. обратимо диссоциируют на катионы водорода (Н+) и анионы кислотных остатков:
Реакции образования солей
С образованием солей карбоновые кислоты реагируют с:
1) металлами до водорода в ряду активности:
2) аммиаком
3) основными и амфотерными оксидами:
4) основными и амфотерными гидроксидами металлов:
5) солями более слабых кислот – карбонатами и гидрокарбонатами, сульфидами и гидросульфидами, солями высших (с большим числом атомов углерода в молекуле) кислот:
Систематические и тривиальные названия некоторых кислот и их солей представлены в следующей таблице:
| Формула кислоты | Название кислоты тривиальное/систематическое | Название соли тривиальное/систематическое |
| HCOOH | муравьиная/ метановая | формиат/ метаноат |
| CH3COOH | уксусная/ этановая | ацетат/ этаноат |
| CH3 CH2COOH | пропионовая/ пропановая | пропионат/ пропаноат |
| CH3 CH2 CH2COOH | масляная/ бутановая | бутират/ бутаноат |
Следует помнить и обратное: сильные минеральные кислоты вытесняют карбоновые кислоты из их солей как более слабые:
Реакции с участием ОН группы
Карбоновые кислоты вступают в реакцию этерификации с одноатомными и многоатомными спиртами в присутствии сильных неорганических кислот, при этом образуются сложные эфиры:
Данного типа реакции относятся к обратимым, в связи с чем с целью смещения равновесия в сторону образования сложного эфира их следует осуществлять, отгоняя более летучий сложный эфир при нагревании.
Обратный реакции этерификации процесс называют гидролизом сложного эфира:
Необратимо данная реакция протекает в присутствии щелочей, поскольку образующаяся кислота реагирует с гидроксидом металла с образованием соли:
Реакции замещения атомов водорода в углеводородном заместителе
При проведении реакций карбоновых с хлором или бромом в присутствии красного фосфора при нагревании происходит замещение атомов водорода при α-атоме углерода на атомы галогена:
В случае большей пропорции галоген/кислота может произойти и более глубокое хлорирование:
Реакции разрушения карбоксильной группы (декарбоксилирование)
Особые химические свойства муравьиной кислоты
Молекула муравьиной кислоты, несмотря на свои малые размеры, содержит сразу две функциональные группы:
В связи с этим она проявляет не только свойства кислот, но также и свойства альдегидов:
При действии концентрированной серной кислоты муравьиная кислота разлагается на воду и угарный газ:
Источник
Карбонильные соединения – это органические вещества, молекулы которых содержат карбонильную группу:

Карбонильные соединения делятся на альдегиды и кетоны. Общая формула карбонильных соединений: СnH2nO.
Строение, изомерия и гомологический ряд альдегидов и кетонов
Химические свойства альдегидов и кетонов
Способы получения альдегидов и кетонов
Альдегидами называются органические соединения, содержащие карбонильную группу, в которой атом углерода связан с радикалом и одним атомом водорода.
Структурная формула альдегидов:

Кетонами называются соединения, в молекуле которых карбонильная группа связана с двумя углеводородными радикалами.
Структурная формула кетонов:

1. Реакции присоединения
В молекулах карбонильных соединений присутствует двойная связь С=О, поэтому для карбонильных соединений характерны реакции присоединения по двойной связи. Присоединение к альдегидам протекает легче, чем к кетонам.
1.1. Гидрирование
Альдегиды при взаимодействии с водородом в присутствии катализатора (например, металлического никеля) образуют первичные спирты, кетоны — вторичные:


1.2. Присоединение воды
При гидратации формальдегида образуется малоустойчивое вещество, называемое гидрат. Оно существует только при низкой температуре.

1.3. Присоединение спиртов
При присоединении спиртов к альдегидам образуются вещества, которые называются полуацетали.
В качестве катализаторов процесса используют кислоты или основания.
Полуацетали существует только при низкой температуре.

Полуацетали – это соединения, в которых атом углерода связан с гидроксильной и алкоксильной (-OR) группами.
Полуацеталь может взаимодействовать с еще одной молекулой спирта в присутствии кислоты. При этом происходит замещение полуацетального гидроксила на алкоксильную группу OR’ и образованию ацеталя:

1.4. Присоединение циановодородной (синильной) кислоты
Карбонильные соединения присоединяют синильную кислоту HCN. При этом образуется гидроксинитрил (циангидрин):

2. Окисление альдегидов и кетонов
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
В зависимости от интенсивности и условий окисление можно условно разделить на каталитическое, мягкое и жесткое.
Альдегид → карбоновая кислота
Формальдегид→ муравьиная кислота→ углекислый газ
вторичные спирты → кетоны
Типичные окислители — гидроксид меди (II), перманганат калия KMnO4, K2Cr2O7, аммиачный раствор оксида серебра (I).
Кетоны окисляются только при действии сильных окислителей и нагревании.
2.1. Окисление гидроксидом меди (II)
Происходит при нагревании альдегидов со свежеосажденным гидроксидом меди, при этом образуется красно-кирпичный осадок оксида меди (I) Cu2O. Это — одна из качественных реакций на альдегиды.

Видеоопыт окисления муравьиного альдегида гидроксидом меди (II) можно посмотреть здесь.
Например, муравьиный альдегид окисляется гидроксидом меди (II)
HCHO + Cu(OH)2 = Cu + HCOOH + H2O
Чаще в этой реакции образуется оксид меди (I):
HCHO + 2Cu(OH)2 = Cu2O + HCOOH + 2H2O
2.2. Окисление аммиачным раствором оксида серебра
Альдегиды окисляются аммиачным раствором оксида серебра (реакция «серебряного зеркала»).

Поскольку раствор содержит избыток аммиака, продуктом окисления альдегида будет соль аммония карбоновой кислоты.
Например, при окислении муравьиного альдегида аммиачным раствором оксида серебра (I) образуется карбонат аммония

Например, при окислении уксусного альдегида аммиачным раствором оксида серебра образуется ацетат аммония
Образование осадка серебра при взаимодействии с аммиачным раствором оксида серебра — качественная реакция на альдегиды.
Упрощенный вариант реакции:

2.3. Жесткое окисление
При окислении под действием перманганатов или соединений хрома (VI) альдегиды окисляются до карбоновых кислот или до солей карбоновых кислот (в нейтральной среде). Муравьиный альдегид окисляется до углекислого газа или до солей угольной кислоты (в нейтральной среде).
Например, при окислении уксусного альдегида перманганатом калия в серной кислоте образуется уксусная кислота

Кетоны окисляются только в очень жестких условиях (в кислой среде при высокой температуре) под действием сильных окислителей: перманганатов или дихроматов.
Реакция протекает с разрывом С–С-связей (соседних с карбонильной группой) и с образованием смеси карбоновых кислот с меньшей молекулярной массой или СО2.
| Карбонильное соединение/ Окислитель | KMnO4, кислая среда | KMnO4, H2O, t |
| Метаналь СН2О | CO2 | K2CO3 |
| Альдегид R-СНО | R-COOH | R-COOK |
| Кетон | R-COOH/ СО2 | R-COOK/ K2СО3 |

2.4. Горение карбонильных соединений
При горении карбонильных соединений образуются углекислый газ и вода и выделяется большое количество теплоты.
CnH2nО + 3n/2O2 → nCO2 + nH2O + Q
Например, уравнение сгорания метаналя:
CH2O + O2 = CO2 + H2O
3. Замещение водорода у атома углерода, соседнего с карбонильной группой
Карбонильные соединения вступают в реакцию с галогенами, в результате которой получается хлорзамещенный (у ближайшего к карбонильной группе атома углерода) альдегид или кетон.
Например, при хлорировании уксусного альдегида образуется хлорпроизводное этаналя

Полученное из ацетальдегида вещество называется хлораль. Продукт присоединения воды к хлоралю (хлоральгидрат) устойчив и используется как лекарство.
4. Конденсация с фенолами
Формальдегид может взаимодействовать с фенолом. Катализатором процесса выступают кислоты или основания:

Дальнейшее взаимодействие с другими молекулами формальдегида и фенола приводит к образованию фенолоформальдегидных смол и воды:

Фенол и формальдегид вступают в реакцию поликонденсации.
Поликонденсация — это процесс соединения молекул в длинную цепь (полимер) с образованием побочных продуктов с низкой молекулярной массой (вода или др.).
5. Полимеризация альдегидов
Полимеризация характерна в основном для легких альдегидов. Для альдегидов характерна линейная и циклическая полимеризация.
Например, в растворе формалина (40 %-ного водного раствора формальдегида) образуется белый осадок полимера формальдегида, который называется полиформальдегид или параформ:

Источник
Добрый день, дорогие подписчики и гости моего канала. Сегодня вас ждет еще одна статья из цикла «школьный курс химии». На написание этой статьи, меня вдохновили пособия для подготовки учеников старшей школы к ЕГЭ, в которых основные классы органических соединений описаны очень слабо и приведены далеко не все реакции встречающиеся на экзамене. В сегодняшней статье, я постараюсь, как можно более подробно разобрать два класса органических веществ – Альдегиды и Кетоны. И начнем мы как всегда с определений.
Альдегиды – это органические вещества, которые содержат карбонильную группу (=С=O), соединенную с атомом водорода и углеводородным радикалом.
Таким образом, общая формула альдегидов:
Кетоны — это органические вещества, в молекулах которых карбонильная группа (=С=O) связана с двумя углеводородными радикалами.
Общая формула кетонов:
Таким образом, карбонильная группа (=С=O) определяет принадлежность вещества к классу альдегидов или кетонов. Частный случай фунциональной карбонильной группы – это альдегидная группа (-COH) и она уже определяет принадлежность вещества лишь к классу альдегидов.
Гомологический ряд альдегидов следующий:
Гомологический ряд кетонов несколько сложнее, в виду изомерии, однако его можно представить так:
Как вы видете, всем известный растворитель краски ацетон, является простейшим кетоном.
Ацетон – это бесцветная летучая жидкость с характерным запахом. В последнее время он широко применяется в различных сферах производства, таких как:
– Синтез поликарбонатов и полиуретанов.
– Производство эпоксидных смол.
– Производство лаков.
– Производство взрывчатых веществ.
– Производство лекарственных препаратов.
– Используется при экстракции многих растительных веществ.
Так же, более подробно стоит поговорить и о некоторых простейших представителях класса альдегидов.
Формальдегид (от лат. formica — «муравей») — это бесцветный газ с резким запахом, хорошо растворимый в воде и других органических растворителях, очень ядовит. Его применяют для:
– Производства фенолформальдегидных пластмасс.
– Для производства многих лекарственных препаратов, например уротропина. Кстати, спресованый в виде брикетов уротропин применяют в качестве горючего (сухой спирт).
– Раствор формальдегида в воде называют формалином. Его используют для хранения биопрепаратов, протравливания семян перед посевом, дубления кож.
Ацетальдегид (Уксусный альдегид) – это летучая жидкость, хорошо растворимая в воде, с характерным запахом. Основные сферы применения уксусного альдегида:
– Производство уксусной кислоты.
– Получение ацетатного волокна.
– Получение альдегидных полимеров (различных пластмасс).
Получение альдегидов и кетонов:
Существует большое колличество способов получения альдегидов и кетонов перечислим некоторые из них.
1. Окисление спиртов на медном катализаторе:
C2H5OH + CuO → CH3CHO + Cu + H2O
Окисление вторичных спиртов по этому же методу, приводит к образованию кетонов:
2. Реакция Кучерова.
При гидратации ацетилена получается уксусный альдегид:
При гидратации любых других алкинов получаются кетоны:
3. При окисление вторичных спиртов перманганатом калия получаем кетоны:
5CH3CH(OH)CH3 + 2KMnO4 + 3H2SO4 = CH3-C(O)-CH3 + K2SO4 + 2MnSO4 + 8H2O
4. В промышленности формальдегид получают путем окисления метана при 500 градусах Цельсия, с участием различных катализаторов.
CH4 + O2 = H-COH + H2O
Химические свойства Альдегидов и Кетонов:
1. Взаимодействие с водородом (Гидрирование)
Слово Альдегиды, происходит от латинских слов «alcohol dehydrogenatus» – «алкоголь дегидрированый» или «спирт лишенный водорода», а дегидрированый продукт способен вернуть себе водород. Таким образом альдегиды востанавливаются до первичных спиртов, а кетоны до вторичных:
2. Гидратация.
Данная реакция характерна только для формальдегида и ацетальдегида.
Для кетонов данная реакция не характерна.
3. Присоединение синильной кислоты:
Кстати, необходимо знать, что синильная кислота или же цианистоводородная кислота – это бесцветная, очень летучая, легкоподвижная ядовитая жидкость, имеющая характерный запах горького миндаля.
4. Присоединение спиртов:
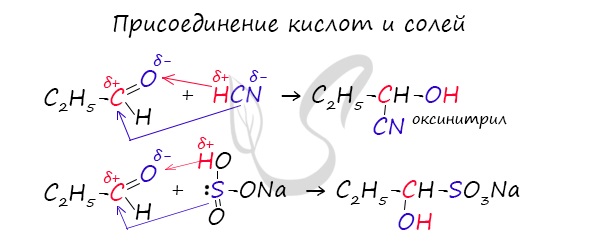
5. Взаимодействие с гидросульфитом натрия:
Данная реакция является качественной, так как образующаяся в результате нее соль выпадает в виде осадка.
6. Реакция «серебряного зеркала».
Это взаимодействие альдегида с аммиачным раствором оксида серебра или реактивом Толленса.
Данную реакцию можно записать так:
Однако, по факту кислота не может существовать с образовавшимся раствором аммиака, поэтому правильнее будет записать ее таким образом:
Данная реакция является качественной и для других веществ содержащих альдегидную группу, например для муравьинной кислоты, ее эфиров или для глюкозы.
Кетоны в реакцию серебряного зеркала не вступают.
7. Взаимодействие со свежеполученым осадком гидроксида меди II.
Эта реакция так же не характерна для кетонов.
Для альдегидов, эту реакцию можно записать так:
В результате реакции сначала произойдет образование желтого осадка, который затем постепенно начнет приобретать красно – оранжевый оттенок.
8. Взаимодействие с подкисленным раствором перманганата калия.
Надо отметить, что окисление формальдегида идет до углекислого газа:
HCOH + KMnO4 + H2SO4 = K2SO4 + MnSO4 + CO2 + H2O
Во всех остальных случаях образуется карбоновая кислота:
5CH3COH + 2KMnO4 + 3H2SO4 = 5CH3COOH + 2MnSO4 + K2SO4 + 3H2O
9. Реакция Тищенко.
Диспропорционирование альдегида – получение сложного эфира из альдегида – в присутствии алкоголята алюминия (1906 г.)
10. Реакция Фаворского.
Конденсация карбонильных соединений с алкинами с образованием ацетиленовых спиртов:
11. Реакция Бутлерова.
Получение углеводов из формальдегида в присутствие известкового раствора:
12. Галогенирование по альфа-атому углерода:
13. Полимеризация.
Полимериза́ция — это процесс образования высокомолекулярного вещества (полимера) путём многократного присоединения молекул низкомолекулярного вещества (мономера) к активным центрам в растущей молекуле.
Кетоны в эти реакции не вступают, а среди альдегидов имеет смысл лишь полимеризация формальдегида:
14. Поликонденсация.
Поликонденсация — процесс синтеза полимеров из органических соединений, обычно сопровождающийся выделением низкомолекулярных побочных продуктов (чаще всего воды).
Нам, особенно интересна поликонденсация формальдегида с фенолом, приводящая к образованию фенолформальдегидной смолы:
15. Реакция горения.
2 CH3COH + 5 O2 = 4 CO2 + 4 H2O
Вот пятнадцать химических реакций, которые могут встречаться на ЕГЭ по теме альдегидов. А я сейчас держу пособие для подготовки к ЕГЭ, где химических реакций перечислено только пять. К тому же забыли написать способы получения альдегидов. Так что качественно ищите материалы для подготовки к экзаменам.
Сдающим ЕГЭ, так же рекомендую к прочтению:
Карбоновые кислоты.
Фенолы.
То, что нужно знать о Спиртах.
Высоких балов тем, кто сдает ЕГЭ!
Источник
Альдегиды – летучие жидкости органического состава, являющиеся продуктом неполного окисления спиртов. Карбонильная группа
в молекулах альдегидов связана с одним атомом водорода и одной группой R.
Не часто встречаются в природе в отдельном виде, но, несомненно, играют важную роль в физиологических процессах растений и животных.
Общая формула альдегидов CnH2nO.
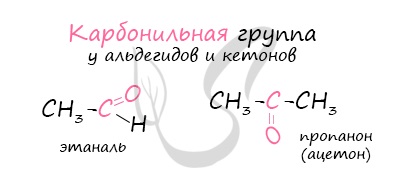
Многие альдегиды имеют специфический запах. Высшие альдегиды, в особенности непредельные, используются в пищевой промышленности и парфюмерии.
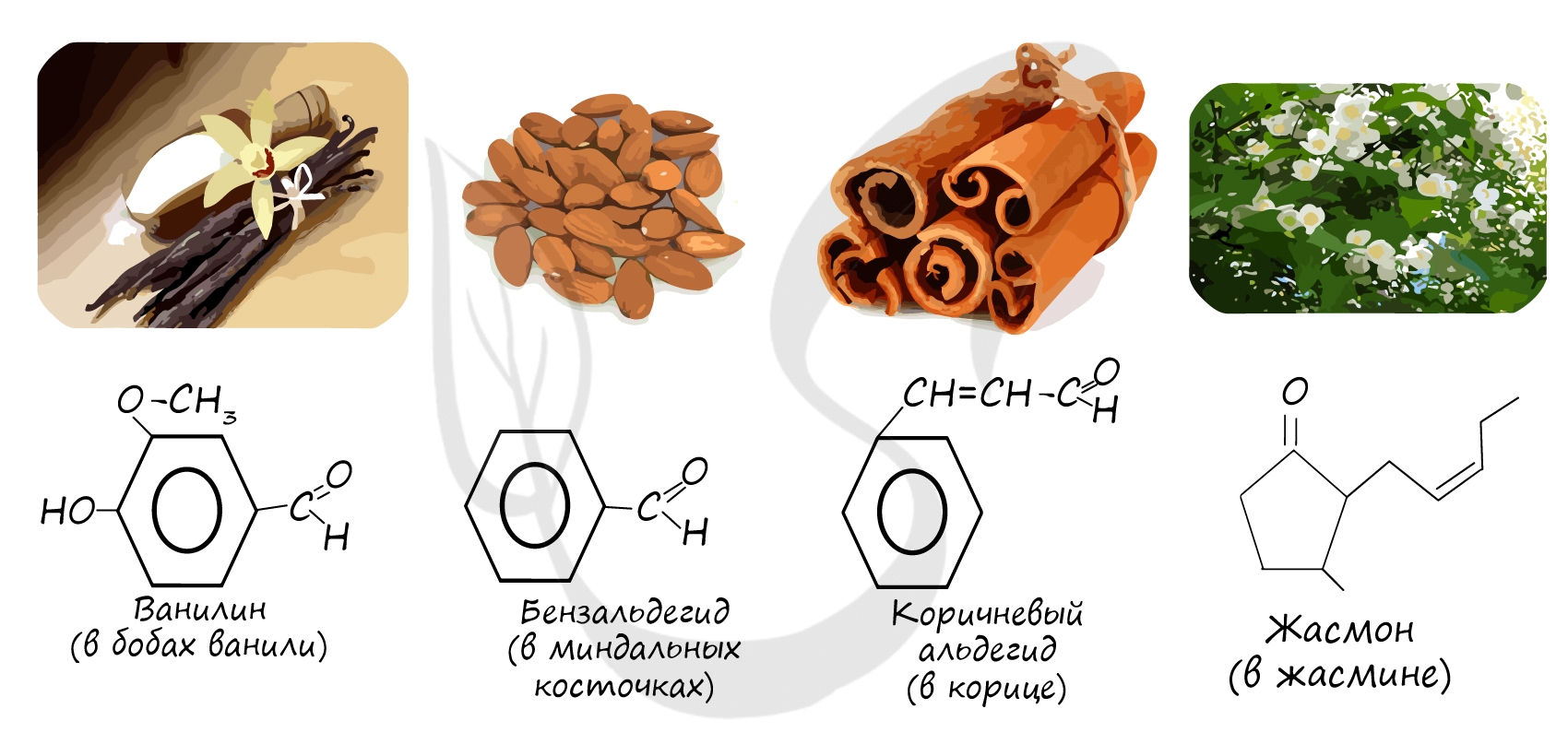
Номенклатура и изомерия альдегидов
Названия альдегидов формируются путем добавления суффикса “аль” к названию алкана с соответствующим числом атомов углерода: метаналь,
этаналь, пропаналь, бутаналь, пентаналь и т.д.
Вы можете встретить их молекулярные формулы, где группа OH записана наоборот – HO. Например: метаналь – HCHO, этаналь –
CH3CHO, пропаналь – C2H5CHO. Это делают специально для того, чтобы их было легче отличить от спиртов.
Многие альдегиды имеют тривиальные названия. Наиболее известные: метаналь – формальдегид, этаналь – ацетальдегид. Замечу, что формалином
называется 40% раствор формальдегида.
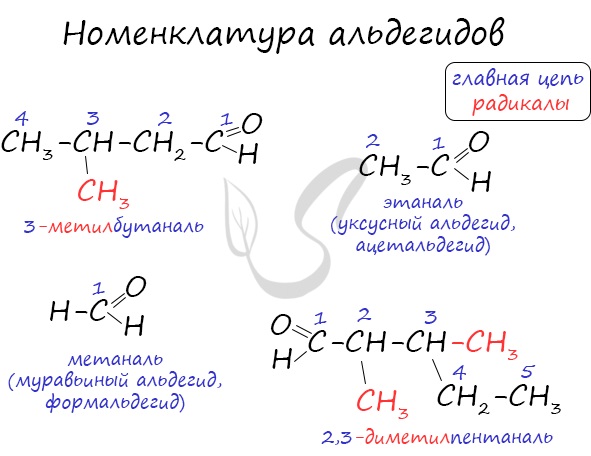
Для альдегидов характерна структурная изомерия: углеродного скелета, межклассовая изомерия с кетонами.
Получение альдегидов и кетонов
- Окисление спиртов
- Пиролиз солей карбоновых кислот
- Каталитическое дегидрирование спиртов
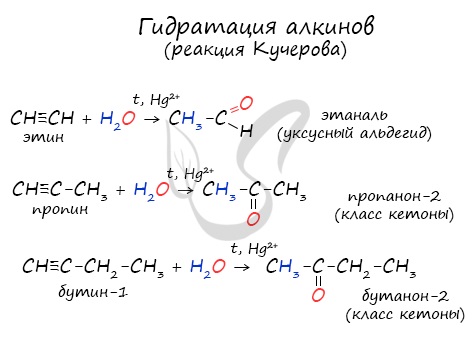
- Реакция Кучерова
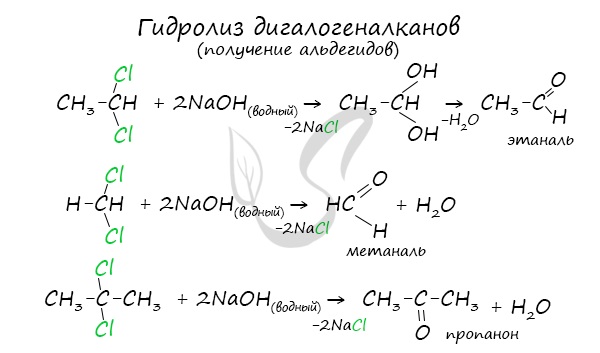
- Гидролиз дигалогеналканов
- Окисление метана
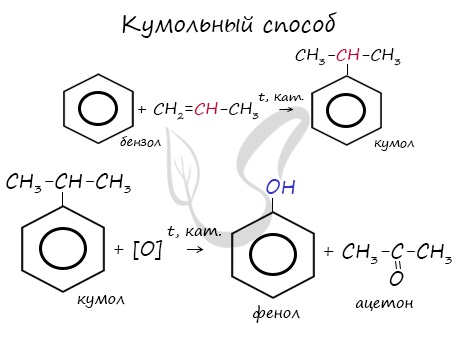
- Кумольный способ получения ацетона (и фенола)
Важно заметить, что при окислении первичных спиртов образуются альдегиды, при окислении вторичных спиртов – кетоны.
Окисление с помощью оксида меди относится к лабораторным способам получения альдегидов.
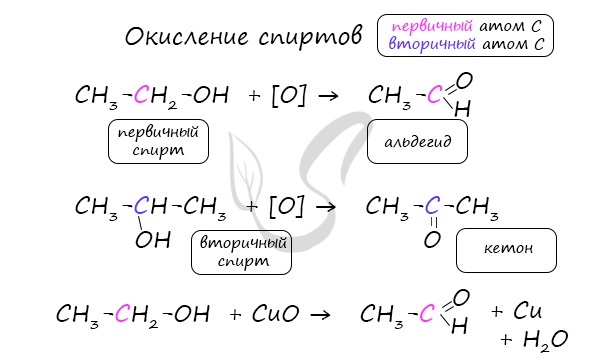
Этот способ также просто осуществить в лабораторных условиях. При пиролизе (нагревании без доступа кислорода) кальциевых или
бариевых солей карбоновых кислот возможно получение кетонов.

В присутствии катализатора и при нагревании спиртов от гидроксогруппы и прилежащего к ней атома углерода отщепляется по
атому водорода. В результате образуется карбонильная группа.
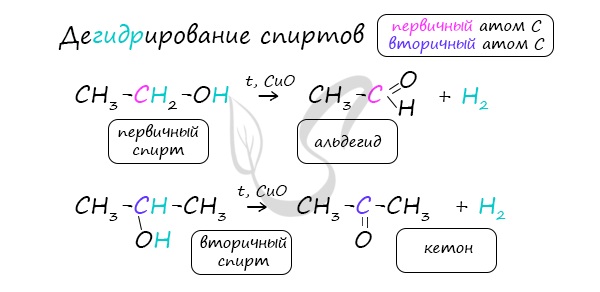
Реакцией Кучерова называют гидратацию алкинов в присутствии солей двухвалентной ртути.
В результате такой реакции ацетилен превращается в уксусный альдегид. Все остальные его гомологи: пропин, бутин, пентин и т.д. превращаются в
соответствующие кетоны.
Для получения альдегида два атома галогена должны находиться у первичного атома углерода, для получения кетонов – у вторичного.
В результате такого гидролиза образуются двухатомные спирты, в которых две OH-группы прилежат к одному атому углерода. Такие соединения неустойчивы
и распадаются на карбонильное соединение (альдегид или кетон) и воду.
В промышленности окислением метана при температуре 500 °C и в присутствии катализатора получают формальдегид.

В прошлой теме, посвященной фенолам, мы касались данного способа. В результате такой реакции образуется не только фенол, но и ацетон.
Химические свойства альдегидов и кетонов
Запомните, что для альдегидов и кетонов характерны реакции присоединения по карбонильной группе. Это является важным отличием альдегидов от карбоновых кислот, для которых реакции присоединения не характерны.
- Реакции присоединения
- Окисление альдегидов
Для понимания механизма реакции важно вспомнить об электроотрицательности. В карбонильной группе кислорд, как более электроотрицательный
элемент, тянет электронную плотность на себя от углерода. На атоме кислорода возникает частичный отрицательный заряд (δ-), а на атоме
углерода частичный положительный (δ+).
Основы школьного курса физики подсказывают, что отрицательный заряд притягивает положительный: именно так и будет происходить
при присоединении различных молекул к карбонильной группе альдегидов и кетонов.
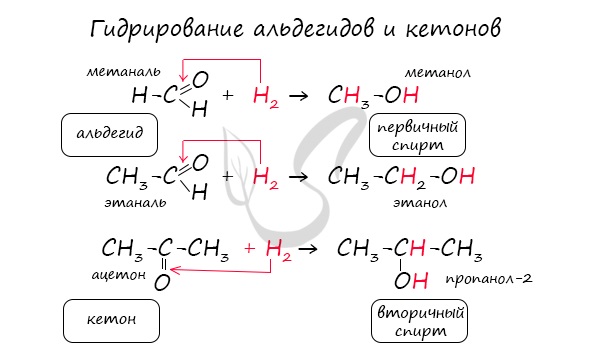
Реакция гидрирования альдегидов происходит по типу присоединения, сопровождается разрывом двойной связи в карбонильной группе.
Гидрирование альдегидов приводит к образованию первичных, а гидрирование кетонов – вторичных спиртов.
В результате полного окисления, горения, образуется углекислый газ и вода.
2CH3CHO + 5O2 → 4CO2 + 4H2O
Альдегиды легко окисляются до карбоновых кислот в лабораторных условиях. Это осуществляется с помощью известной реакции
серебряного зеркала. Данная реакция является качественной для альдегидов.
Кетоны, в отличие от альдегидов, в реакции окисления не вступают.

Обратите особое внимание, что при написании реакции с аммиачным раствором серебра в полном виде, правильнее будет указать не кислоту, а ее аммиачную соль. Это связано с тем, что выделяющийся аммиак, который обладает основными свойствами, реагирует с кислотой с образованием соли

Важно заметить, что при окислении метаналя, образовавшаяся муравьиная кислота тут же окисляется до угольной кислоты, которая
распадается на углекислый газ и воду. Это связано с интересным фактом – наличием альдегидной группы у муравьиной кислоты.

Окисление также возможно другим реагентом – гидроксидом меди II. Эта реакция также относится к качественным для
альдегидов, в результате образуется кирпично-красный осадок окс?
