Какое количество вещества в молях содержится в 1г воды

- Главная
- Вопросы & Ответы
- Вопрос 9446184

Пармезан Черница
более месяца назад
Просмотров : 3
Ответов : 1
Лучший ответ:


Мари Умняшка
дано m=1 г М=18 г/моль v- ?
v=m/M=1/18=0.056 моль
более месяца назад
Ваш ответ:
Комментарий должен быть минимум 20 символов
Чтобы получить баллы за ответ войди на сайт

Лучшее из галереи за : неделю месяц все время































Другие вопросы:

Пармезан Черница
Написать рассказ о добрых делах и добрых людях в годы великой отечественной войны Плиз СРОчНо!!!!
более месяца назад
Смотреть ответ
Просмотров : 2
Ответов : 1

Васян Коваль
У Пери и Исмаила всего 36 манат. у пери на 8 манат больше чем у исмаила. Сколько денег будет У ИСМАИЛА ЕСЛИ ОТЕЦ ДАСТ ЕМУ ЕЩЕ 7 МАНАТ? ПОЖАЛУЙСТА СДЕЛАЙТЕ С ИКСАМИ
более месяца назад
Смотреть ответ
Просмотров : 3
Ответов : 1

Энджелл
СРОЧНО!!! Какова мощность электродвигателя, который за время 1,5 часа совершил работу 1,2 кВт*ч.
более месяца назад
Смотреть ответ
Просмотров : 3
Ответов : 1

Энджелл
РЕШИТЕ СРОЧНО!! Академик В. С. Якоби в 1834 г. изобрел электродвигатель, с помощью которого можно было равномерно поднять груз массой 5 кг на высоту 0,6 м в течение 2 с. Определите мощность этого двигателя.
более месяца назад
Смотреть ответ
Просмотров : 4
Ответов : 1

Суррикат Мими
задача в альбоме 21 цветная фотография и 3 черно- белой. Во сколько раз больше цветных фотографий, чем черно- белых? Напишите обратную задачу…
более месяца назад
Смотреть ответ
Просмотров : 8
Ответов : 1
Источник
МБОУ гимназияг.
г. Сафоново Смоленской области
учитель Петрущенкова Людмила Павловна
Урок по химии 8 класс
Тема урока: Количество вещества. Молярная масса.
Цель урока: познакомить учащихся с понятием «количество вещества», «моль», сформировать представление о молярной массе вещества и научить учащихся переходить от понятия «относительная молекулярная масса» к понятию «молярная масса вещества».
Основные понятия: «закон Авогадро», «количество вещества», «молярная масса», «моль».
Оборудование: некоторые Ме и неМе количеством 1 Моль, 1мМоль, 1кМоль.
Ход урока.
- Постановка цели урока.
- Повторение домашнего задания.
Задание из рабочей тетради у доски.
Упр. 2.
а) калия 1S22S22P63S23P64S1
б) кальция 1s22s22p63s23p64s2
в) алюминия 1s22s22p63s23p1
Упр. 3. Схемы образования химической связи для Ме.
а) K0 -1e → K+
б) Ca0 -2e → Ca2+
в) Al0 -3e → Al3+
Задание из рабочей тетради, раздел «Неметаллы».
Упр. 2. а) 1s1; б) 1s22s22p63s23p5; в) 1s22s22p3.
Упр. 3. Схемы образования химической связи.
а) H∙ + ∙H → H : H
б) :Cl∙ + ∙Cl: → :Cl:Cl:
в) :N∙ + ∙N: → :N :: N:
Работа по карточкам.
Карточка №1.
- В какую частицу превращается атом, отдав или приняв электроны до завершения внешнего уровня?
Al0 -3e →…
О0 +2е →…
- Определите тип химической связи молекул: I2, CH4, AlCl3.
Карточка №2.
- В какую частицу превращается атом, отдав или приняв электроны до завершения внешнего уровня?
Na0 -1e → Na+
Cl0+1e →…
- Определите тип химической связи молекул: N2, H2O, MgCl2.
Карточка №3.
- В какую частицу превращается атом, отдав или приняв электроны до завершения внешнего уровня?
K0 -1e →…
S0 +2е →…
- Определите тип химической связи молекул: Cl2, CO2, NaI.
Фронтальный опрос:
- Где расположены элементы – Ме в таблице Д.И.Менделеева?
- Перечислите особенности строения атомов элементов – Ме.
- Название – свойство – область применения.
- Где расположены элементы – неметаллы в таблице Д.И.Менделеева?
- Что такое аллотропия? (Аллотропия углерода, кислорода, фосфора?)
Задания: Работа по ПС.
- Изучение нового материала.
Что изучает химия? (наука о веществах) А в чем измерять вещества?
Температура измеряется в градусах, путь в метрах, масса – в граммах, килограммах.
Какие бы вы предложили единицы измерения?
Может быть, вспомнить из каких частиц состоит вещество?
– из молекул, атомов.
Но отсчитать нужное число молекул и атомов технически невозможно из-за малого размера. Вот если бы найти способ, в котором объединились бы масса (её измерить просто) и число молекул (атомов). И ученые придумали. Если брать столько граммов вещества, какова его относительная молекулярная масса, сколько же там будет содержаться молекул?
Для О2 – 32г / Mr(O2) = 32 /
Для O3 – 48г / Mr(O3) = 48 /
Для H2O – 18г / Mr(H2O) = 18 /
Оказалось, что в 32г O2, в 48г О3, в 18г H2O и т.д. содержится одинаковое число молекул, равное 6∙1023. Это число назвали числом Авогадро (обозначается NA).
Сделаем вывод: если мы возьмём такую массу вещества, которая равна атомной массе по величине, но взята в граммах, то там будет всегда (для любого вещества) 6,02∙1023 атомов этого вещества.
Запись на доске.
NA = 6,02∙1023 – постоянная Авогадро
Вот это количество вещества, которое содержит 6,02∙1023 молекул какого – либо вещества, и назвали молем.
Что такое моль? (работа с учебником).
Моль – количество вещества, в котором содержится 6,02∙1023 молекул, атомов или ионов, т.е. структурных единиц.
Бывает моль молекул, моль атомов, моль ионов.
n = N/NA, N = NA ∙ n, NA = N/n,
где n – число молей, N – число атомов или молекул, NA – постоянная Авогадро.
кМоль = 103Моль, мМоль = 10-3Моль.
- 0,5 Moль – 3,01∙1023
- 10 Моль – 60,02∙1023
А что нужно сделать, чтобы отмерить 1 Моль вещества?
Ответ: нужно взять столько граммов этого вещества, какова его Mr.
Вопрос: Чему равна масса 1 Моля вещества?
Масса 1 Моль вещества называется молярной массой, обозначается М.
│Mr│=│M│
И вычисляется по формуле:
M = m/n, единицы измерения: г/Моль, кг/Моль, мг/Моль.
А в тысячу раз большая единица количества вещества (киломоль, кМоль). А в тысячу раз меньшая единица количества вещества (миллимоль, мМоль).
n = m/M, m = M ∙ n
Вывод: Масса Моль измеряется в г/Моль, масса кМоль измеряется в кг/кМоль, масса мМоль измеряется в мг/Моль.
Предлагается задача: Я взяла 64г О2. Какое количество вещества (сколько Молей) я взяла? (Два)
n = m/M, n = 64г/32г/Моль = 2Моль.
А сколько молекул кислорода будут содержать эти 64г его. Ответ: 4 Моль.
N = NA ∙ n, N = 6,02∙1023 ∙ 2Моль = 12,04∙1023 молекул.
- Закрепление.
Заполнить таблицу.
Вещество | Число молекул N = NA ∙ n | Молярная масса M = m/n | Число Молей n = m/M | Масса вещества m = M ∙ n |
H2 | N = 6,02∙1023∙ 5 = 31∙1023 | M(H2) =2г/Моль | 5Моль | m = 5∙2=10г |
H2SO4 | 60∙1023 | M(H2SO4) = 98г/Моль | 980/98 =10Моль | 980г |
FeCl2 | 12,04∙1023 | M(FeCl2) = 127г/Моль | 2 кМоль | 254г |
Задача №1. Сколько молей составляют и сколько молекул содержат 8 г кислорода О2?
Дано: m(O2) = 8г Решение: Mr(O2) = 16∙2=32.
M(O2)=16∙2=32г/моль
Найти: n(O2); N(O2) n(O2)=m(O2)/M(O2)=8г/32г/моль=0,25 моль
N(O2)= NA∙n(O2)= 6,02∙1023моль-1∙0,25 моль=1,505∙1023
Ответ: 8г кислорода составляют 0,25 моль и содержат 1,505∙1023 молекул.
Задача №2. Определите массу 0,25 моль серной кислоты.
Дано: Решение:
n (H2SO4) = 0,25 моль 1. Находим молярную массу серной кислоты
М(H2SO4)=2+32+64=98г/моль
Найти: m(H2SO4); 2. Найдем массу вещества m=n∙M;
M(H2SO4)=n(H2SO4)∙M(H2SO4)=0,25
моль∙98г/моль=24,5г
Ответ: масса 0,25 моль серной кислоты равна 24,5 г.
- Итоги урока.
Общий вывод (предлагается записать в тетрадях основные определения и некоторые выводы).
- Количество вещества – физическая величина, которая означает определённое число структурных элементов (молекул, атомов, ионов), обозначается n(эн), измеряется в Молях, в миллимолях, киломолях.
- 1Моль любого вещества содержит число молекул его, равное постоянной Авогадро NA(6,02∙1023).
- Чтобы отмерить 1Моль вещества, нужно взять столько граммов его, какова его относительная масса Mr.
- Масса 1Моль вещества называется молярной массой (М), она измеряется в г/Моль и численно равна Mr.
- Домашнее задание. §15. Упр. 1-3, задания из рабочей тетради: разделы Количество вещества и Молярная масса.
Источник
Решениие задач по химии на закон Авогадро
Задача 53.
Сопоставить числа молекул, содержащихся в 1г NH3 и в 1г N2. В каком случае и во сколько раз число молекул больше?
Решение:
В одном моле любого вещества содержится 6,02 . 1023 молекул этого вещества.
Рассчитаем содержание количества вещества в 1г NH3 и N2 по формуле:
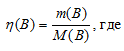
 (B) – количество вещества (В);
(B) – количество вещества (В);
m(B)- масса вещества (В);
M(B) – Молярная масса вещества (В).
М(NH3) = 17г/моль, M(N2) = 28г/моль.
Тогда
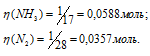
Число молекул NH3 больше числа молекул N2, так как  (NH3) >
(NH3) > (N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
(N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
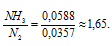
Ответ: в 1,65 раз число молекул NH3 больше числа молекул N2.
Задача 54.
Выразить в граммах массу одной молекулы диоксида серы.
Решение:
Находим молекулярную массу диоксида серы:
M(SO2) = 32 + (16 . 2) = 64г/моль.
Молекулярная масса численно составляет массу одного моля вещества, а значит, вес одного моля численно равен молекулярной массе и составляет 64г. Известно, что в одном моле любого вещества содержится 6,02 . 1023 молекул данного вещества. Исходя из этого, рассчитаем массу в граммах одной молекулы диоксида серы:
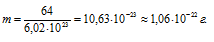
Ответ: масса одной молекулы диоксида серы равна.
Задача 55.
Одинаково ли число молекул в 0,001кг Н2 и в 0,001кг О2? В 1 моле Н2 и в 1 моле 02? В 1л Н2 и в 1л О2 при одинаковых условиях?
Решение:
Молекулярные массы водорода и кислорода равны соответственно 2г/моль и 32г/моль. Отсюда находим количество водорода и кислорода, зная их массы:
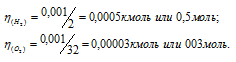
Один моль любого вещества содержит 6,02 .1023 молекул. Следовательно, в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул:

Так как имеется по одному молю водорода и кислорода, то количество молекул веществ будет одинаково:
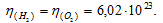
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1л водорода и в 1л кислорода:
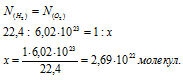
Ответ: а) в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул; б) в одном моле водорода и в одном моле кислорода содержится одинаковое число молекул: в) в одном литре водорода и в одном литре кислорода содержится одинаковое число молекул.
Задача 56.
Сколько молекул содержится в 1,00 мл водорода при нормальных условиях?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 .1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1мл водорода из пропорции:
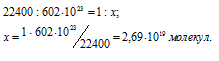
Ответ: 2,69 .1019 молекул.
Задача 57.
Какой объем при нормальных условиях занимают 27 .1021 молекул газа?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда находим какой объём при нормальных условиях занимают 27 .1021 молекул газа, составив пропорцию:
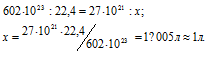
Ответ: V=1л.
Задача 58.
Каково соотношение объемов, занимаемых 1 молем О2 и 1 молем О3 (условия одинаковые)?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Следовательно соотношение объёмов, занимаемых одним молем О2 и одним молем О3 иметь вид:
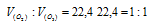
Ответ: 1:1
Задача 59.
Взяты равные массы кислорода, водорода и метана при одинаковых условиях. Найти отношение объемов взятых газов.
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Мольные массы кислорода, водорода и метана, соответственно равны 32 г/моль; 2г/моль; 16 г/моль.
Так как массы кислорода, водорода и метана одинаковы при одинаковых условиях, то отношение объёмов взятых газов находим из пропорции:
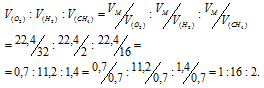
Ответ: 1:16:2.
Задача 60.
На вопрос, какой объем займет 1моль воды при нормальных условиях, получен ответ: 22,4л. Правильный ли это ответ?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Так как вода при нормальных условиях находится в жидкой, а не в газообразной фазе, то ответ, что 1моль воды займёт 22,4л не правильный. Учитывая, что молярная масса воды равна 18г/моль, а плотность равна единице, то правильный ответ будет равен:
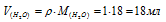
Ответ: 18мл.
Задача 61.
Сколько молекул диоксида углерода находится в 1л воздуха, если объемное содержание СО2 составляет 0,03% (условия нормальные)?
Решение:
При нормальных условиях углекислый газ, содержащийся в 1л воздуха, занимает объём 0,0003л. Зная, что мольный объём любого газа занимает 22,4л, рассчитаем число молей углекислого газа в 0,0003л из пропорции:
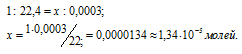
Учитывая, что в одном моле вещества содержится 6,02 . 1023 молекул, находим число молекул в 0,0003л газа:

Ответ: 8,07 .1018 молекул.
Источник
