Какое свойство не характерно для всех металлов электропроводность

Общие физические свойства мекталлов:
1) Пластичность – способность изменять форму при ударе, вытягиваться в проволоку, прокатываться в тонкие листы. В ряду – Au, Ag, Cu, Sn, Pb, Zn, Fe уменьшается.
2) Блеск, обычно серый цвет и непрозрачность. Это связано со взаимодействием свободных электронов с падающими на металл квантами света.
3) Электропроводность. Объясняется направленным движением свободных электронов от отрицательного полюса к положительному под влиянием небольшой разности потенциалов. В ряду – Ag, Cu, Al, Fe уменьшается. При нагревании электропроводность уменьшается, т. к. с повышением температуры усиливаются колебания атомов и ионов в узлах кристаллической решетки, что затрудняет направленное движение “электронного газа”.
4) Теплопроводность. Закономерность та же. Обусловлена высокой подвижностью свободных электронов и колебательным движением атомов, благодаря чему происходит быстрое выравнивание температуры по массе металла. Наибольшая теплопроводность – у висмута и ртути.
5) Твердость. Самый твердый – хром (режет стекло) ; самые мягкие – щелочные металлы – калий, натрий, рубидий и цезий – режутся ножом.
6) Плотность. Она тем меньше, чем меньше атомная масса металла и чем больше радиус его атома (самый легкий – литий (r=0,53 г/см3); самый тяжелый – осмий (r=22,6 г/см3).
Металлы, имеющие r < 5 г/см3 считаются “легкими металлами”.
7) Температуры плавления и кипения. Самый легкоплавкий металл – ртуть (т. пл. = -39°C), самый тугоплавкий металл – вольфрам (t°пл. = 3390°C).
Металлы с t°пл. выше 1000°C считаются тугоплавкими, ниже – низкоплавкими.
Все металлы являются восстановителями. Для металлов главных подгрупп восстановительная активность (способность отдавать электроны) возрастает сверху вниз и справа налево. Например, Натрий и кальций вытесняют водород из воды уже при обычных условиях:
Ca + 2H2O Ca(OH)2 + H2¬ ; 2Na + 2H2O 2NaOH + H20
А магний при повышении температуры:
Mg + H2O –t MgO + H2
Восстановительная способность и химическая активность элементов побочных подгрупп увеличивается снизу вверх по группе (например, серебро на воздухе окисляется, а золото нет; медь вытесняет серебро из его соли) :
Cu + 2AgNO3 → 2Ag ↓ + Cu(NO3)2
Cu0 -2 ē → Cu+2 1 О. О. В.
Ag+ + ē → Ag0 2 В. В. О.
Высшая положительная степень окисления для металлов главных подгрупп в их соединениях равна номеру группы (например, NaCl, MgCl2, AlCl3, SnCl4), а для металлов побочных подгрупп в их кислородосодержащих соединениях также часто совпадает с номером группы (например, ZnO, TiO2, V2O5, CrO3, KMnO4).
Свойства оксидов металлов слева направо по периоду и снизу вверх по группе изменяются от основных к амфотерным для металлов главных подгрупп (Na2O и MgO – основные оксиды, Al2O3 и BeO – амфотерные) . Для металлов побочных подгрупп свойства оксидов, в которых металлы проявляют свою высшую степень окисления, изменяются от основных через амфотерные к кислотным ( CuO – основной, ZnO – амфотерный, CrO3 – кислотный) .
Сила оснований, образуемых металлами главных подгрупп увеличивается справа налево по периоду и сверху вниз по группе ( Be(OH)2 и Al(OH)3– амфотерные гидроксиды, Mg(OH)2 – слабое основание, NaOHи – Ca(OH)2 сильные основания) . Гидраты оксидов металлов побочных подгрупп с высшими степенями окисления металла вдоль периода слева направо меняют свои свойства от оснований через амфотерные гидроксиды к кислотам ( Cu(OH)2 – основание, Zn(OH)2 – амфотерный гидроксид, H2CrO4 – кислота) .
В природе металлы встречаются в основном в виде соединений – оксидов или солей. Исключение составляют такие малоактивные металлы, как серебро, золото, платина, которые встречаются в самородном состоянии.
Все способы получения металлов основаны на процессах их восстановления из природных соединений.
Источник
Слово «металл» заимствовано из немецкого языка и окончательно усвоено в Петровскую эпоху. Первоначально имело общее значение «минерал, руда, металл», а разграничение этих понятий произошло во времена М.В.Ломоносова.
Немецкое слово «metall» произошло от латинского «metallum» — «рудник, металл».
В латинский язык слово пришло из греческого — μεταλλον: «рудник, копь».
В современном понимании, металлы — группа химических элементов, в виде простых веществ, обладающих характерными металлическими свойствами: высокая тепло- и электропроводность, положительный температурный коэффициент сопротивления, высокая пластичность и металлический блеск.
Однако в астрофизике термин «металл» может иметь другое значение и обозначать все химические элементы тяжелее гелия.
Как химические элементы металлы очень распространены. Из 118 химических элементов, открытых на данный момент (из них не все официально признаны), к металлам относят:
6 элементов в группе щелочных металлов,
6 в группе щёлочноземельных металлов,
38 в группе переходных металлов,
11 в группе лёгких металлов,
7 в группе полуметаллов,
14 в группе лантаноиды + лантан,
14 в группе актиноиды (физические свойства изучены не у всех элементов) + актиний,
вне определённых групп — бериллий и магний.
Таким образом, к металлам относится 96 элементов из всех открытых.
Свойства металлов
Характерные свойства металлов
Металлический блеск (характерен не только для металлов: его имеют и неметаллы иод и углерод в виде графита)
Хорошая электропроводность (из неметаллов электропроводностью обладает также углерод)
Возможность лёгкой механической обработки (см.: пластичность; однако некоторые металлы, например, германий и висмут, непластичны)
Высокая плотность (обычно металлы тяжелее неметаллов)
Высокая температура плавления (исключения: ртуть, галлий и щелочные металлы)
Большая теплопроводность
В реакциях чаще всего являются восстановителями
Физические свойства металлов
Все металлы (кроме ртути и, условно, франция) при нормальных условиях находятся в твёрдом состоянии, однако обладают различной твёрдостью.
Температуры плавления чистых металлов лежат в диапазоне от −39°C (ртуть) до 3410°C (вольфрам). За исключением щелочных, металлы плавятся при высокой температуре, однако некоторые, например, олово и свинец, можно расплавить на обычной электрической или газовой плите.
В зависимости от плотности, металлы делят на лёгкие (плотность 0,53 ÷ 5 г/см³) и тяжёлые (5 ÷ 22,5 г/см³). Самым лёгким металлом является литий (плотность 0.53 г/см³). Самый тяжёлый металл в настоящее время назвать невозможно, так как плотности осмия и иридия — двух самых тяжёлых металлов — почти равны (около 22.6 г/см³ — ровно в два раза выше плотности свинца), а вычислить их точную плотность затруднительно: требуется полностью очистить металлы, так как любые примеси снижают их плотность.
Большинство металлов пластичны, то есть металлическую проволоку можно согнуть, и она не сломается. Это происходит из-за смещения слоёв атомов металлов без разрыва связи между ними. Самыми пластичными являются золото, серебро и медь. Из золота можно изготовить фольгу толщиной 0,003 мм, которую используют для золочения изделий. Однако проволока из цинка или олова хрустит при сгибании, марганец и висмут почти не сгибаются, а сразу ломаются. Пластичность зависит и от чистоты металла. Очень чистый хром весьма пластичен, но, загрязнённый даже незначительными примесями, становится хрупким и более твёрдым.
Все металлы хорошие проводники. Это обусловлено наличием в их кристаллических решётках подвижных электронов, перемещающихся под действием электрического поля. Серебро, медь и алюминий имеют наибольшую электропроводность. По этой причине последние два металла чаще всего используют в качестве материала для проводов. Очень высокую электропроводность имеет также натрий, в экспериментальной аппаратуре известны попытки применения натриевых токопроводов в форме тонкостенных труб из нержавеющей стали, заполненных натрием. Благодаря малому удельному весу натрия, при равном сопротивлении натриевые «провода» получаются значительно легче медных и даже несколько легче алюминиевых.
Высокая теплопроводность металлов также зависит от подвижности свободных электронов. Поэтому ряд теплопроводностей похож на ряд электропроводностей, и лучшим проводником тепла, как и электричества, является серебро. Натрий также находит применение как хороший проводник тепла. Широко известно, например, применение натрия в клапанах автомобильных двигателей для улучшения их охлаждения.
Цвет у большинства металлов примерно одинаковый — светло-серый с голубоватым оттенком. Золото, медь и цезий соответственно жёлтого, красного и светло-жёлтого цвета.
Металлы в природе. Добыча и обогащение
Источник
Анонимный вопрос
3 апреля 2018 · 15,9 K
Свойства металлов делятся на несколько групп: физические, химические, механические и технологические.
1) Физические свойства: цвет, удельный вес, плавкость, электропроводность, магнитные свойства, теплопроводность.
2) Химические свойства: окисляемость, растворимость и коррозионная стойкость.
3) Механические свойства: прочность, твердость, упругость, пластичность.
4) Технологические свойства: прокаливаемость, жидкотекучесть, ковкость, обрабатываемость резанием.
Слишком примитивно, кое-что неверно, что-то устарело (терминология). Не советую использовать.
Как различаются типы кристаллической решетки? Какие способы определения?
Человек науки, полиглот, энтузиаст. Химия, компьютерные технологии, нейропсихоло…
Существует 4 типа кристаллических решеток: ионные, молекулярные, атомные и металлические.
В узлах ионных кристаллических решеток находятся ионы, как можно понять из названия. Такой тип решетки характерен для солей, оксидов и некоторых гидроксидов. Например, самый яркий представитель – NaCl. Вещества подобного строения характеризуются высокой твердостью, тугоплавкостью и нелетучестью.
В молекулярных кристаллических решетках в узлах находятся молекулы. Такие решетки могут быть полярные и неполярные. Например, I2 или N2 – неполярные, а HCl или H2O – полярные. Характерны для жидких и газообразных веществ (при н.у.). Так как молекулярные взаимодействия слабые, то и кристаллические решетки эти будут нетвердые, летучие и с низкой температурой плавления. К таким решеткам относят твердую органику (сахар, глюкоза, нафталин).
В атомных кристаллических решетках в узлах находятся атомы, связанные друг с другом прочными ковалентными связями. Такая решетка характерна простым веществам неметаллам, которые при нормальных условиях находятся в твердом состоянии, например алмаз. Температура плавления у подобных веществ очень высокая, они прочные, твердые и нерастворимы в воде.
Металлические решетки характеризуются тем, что в узлах находятся атомы или ионы одного или нескольких металлов (у сплавов). Для металлических решеток характерно наличие так называемого общего электронного облака. Так как непрерывно происходит процесс перехода валентных электронов одного атома к другому с образованием иона, то можно говорить о том, что электроны свободно двигаются в объеме всего металла. Этим свойством объясняется электро- и теплопроводность металлов. Вещества такого строения ковки и пластичны.
Вообще в материаловедении для изучения кристаллических структур существует множество методов, основанных на свойствах рентгеновского излучения (дифракция, интерференция), электронографический анализ и другие. Но если вы хотите просто определить тип решетки вещества известного состава, нужно понять к какому классу веществ оно относится и какие физико-химические свойства имеет.
Прочитать ещё 1 ответ
Как на практике используют пластичность металлов?
Невское Оборудование поставщик металлообрабатывающего оборудования и станков · spbstanki.ru
Пластичность металов – это одно из самых важных свойств, благодаря которому металлы, стли и сплавы получили такой широкое распространение в мире. Благодаря этому свойству из металлов и сталей возможно изготовление очень широкого спектра изделий: металлы и стали хорошо куются и штампуются (некоторые как в горячем, так и в холодном виде), металлы отлично загибаются и им можно придать практически любую форму прокаткой (как горячей так и холодной).
Как закалить сталь?
Первое – ст.3 или сталь 3 (содержание углерода – 0.3 %, легированные добавки отсутствуют) – не закаляется. Ст.3 – самая распространённая марка. Из нее чаще всего делают трубы отопления, квадратные профили и арматуру круглую, массив квадрата.
Второе – выясняем какая сталь у вас в наличии. Например, прижинная сталь – это 50ХГ. Напильник – У8 (У10). Подшипник – ШХ-15.
Третье – открываем “Справочник термиста” (Яндекс в помощь) и находим режимы термообработки. Важно ! Сталь необходимо не только закалить, но в последующем и отпустить – снять температурные напряжения. Режимы отпуска сталей также прописаны в справочнике.
Благодарю за внимание.
Прочитать ещё 5 ответов
Почему нержавейка ржавеет?
ООО “Скантел” – поставщик импортного нержавеющего металлопроката
· scantel.ru
“Нержавейка” это условное название коррозионностойкой стали. Любая сталь, в основе которой лежит железо (Fe), ржавеет. Нержавейкой называют сталь, легированную хромом (Cr). Благодаря наличию в составе хрома, поверхность металла покрывается оксидной пленкой, которая препятствует ржавлению. При нарушении целостности пленки (химическом или механическом) металл начинает ржаветь.
Прочитать ещё 2 ответа
Какие металлы относятся к драгоценным?
Engineer – programmer ⚡⚡ Разбираюсь в компьютерах, технике, электронике, интернете и… · zen.yandex.ru/gruber
Драгоценные металлы — это металлы, чья стоимость существенно выше стоимости других металлов из-за сложности их добычи или малого количества.
К драгоценным металлам относятся следующие:
- Золото;
- Серебро;
- Платина;
- Палладий.
- Иридий
- Родий;
- Осмий;
- Рутений.
Прочитать ещё 3 ответа
Источник
Глава 2. Металлы
Из курса химии 9 класса вы уже имеете представление о природе химической связи, существующей в кристаллах металлов, — металлической связи. Напомним, что в узлах металлических кристаллических решёток располагаются атомы и положительные ионы металлов, связанные посредством обобществлённых внешних электронов, принадлежащих всему кристаллу. Эти электроны компенсируют силы электростатического отталкивания между положительными ионами и тем самым связывают их, обеспечивая устойчивость металлической решётки.
Металлическая связь обусловливает все важнейшие физические свойства металлов: пластичность, электро- и теплопроводность, металлический блеск и другие свойства, характерные для этого класса простых веществ.
Пластичность — это свойство вещества изменять форму под внешним воздействием и сохранять принятую форму после прекращения этого воздействия.
Способность расплющиваться от удара или вытягиваться в проволоку под действием силы составляет важнейшее механическое свойство металлов. Оно лежит в основе такой уважаемой большинством народов мира профессии, как профессия кузнеца. Недаром покровителем кузнечного дела у разных народов был бог огня: у греков — Гефест, у римлян — Вулкан, у славян — Сварог.
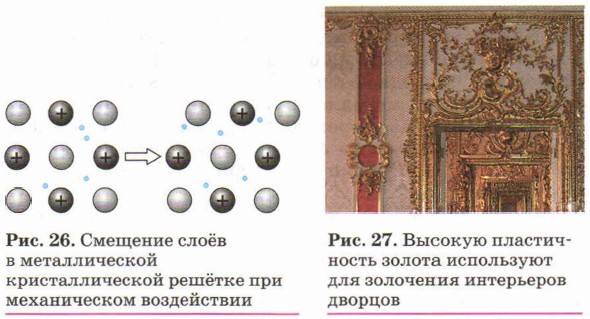
Пластичность металлов обусловлена способностью одних слоёв атом-ионов в кристаллах под внешним воздействием легко смещаться (как бы скользить) по отношению к другим слоям без разрыва связей между ними (рис. 26). Наиболее пластичны золото, серебро и медь. Например, из золота можно изготовить «золотую фольгу» толщиной 0,003 мм, которую используют для золочения изделий (рис. 27).
Высокая электропроводность большинства металлов обусловлена присутствием в их кристаллических решётках подвижных электронов, которые направленно перемещаются под действием электрического поля (рис. 28).
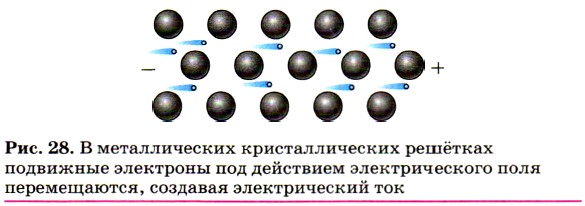
При нагревании колебательные движения ионов в кристалле усиливаются, что затрудняет направленное движение электронов и ведёт к снижению электрической проводимости. При охлаждении электропроводность металлов увеличивается и вблизи абсолютного нуля переходит в сверхпроводимость. Наибольшую электропроводность имеют серебро и медь, наименьшую — марганец, свинец, ртуть и вольфрам.
Такое свойство, как теплопроводность металлов, также связано с высокой подвижностью свободных электронов: сталкиваясь с колеблющимися в узлах решётки ионами, электроны обмениваются с ними энергией. С повышением температуры колебания ионов при посредстве электронов передаются другим ионам, и температура всего металлического предмета быстро выравнивается.
Для гладкой поверхности металлов характерен металлический блеск — результат отражения световых лучей. В порошкообразном состоянии большинство металлов теряет блеск, приобретая чёрную или серую окраску, и только алюминий и магний сохраняют блеск в порошке. Из алюминия, серебра и палладия, обладающих наиболее высокой отражательной способностью, изготовляют зеркала, в том числе и применяемые в прожекторах.
Для большинства металлов характерен белый или серый цвет. Золото и медь окрашены соответственно в жёлтый и жёлто-красный цвет.
Из других физических свойств металлов наибольший практический интерес представляют твёрдость, плотность и температура плавления.
Для большинства металлов характерен белый или серый цвет. Золото и медь окрашены соответственно в жёлтый и жёлто-красный цвет.
Из других физических свойств металлов наибольший практический интерес представляют твёрдость, плотность и температура плавления.
Для всех металлов (кроме ртути) при обычных условиях характерно твёрдое агрегатное состояние. Однако твёрдость их различна. Наиболее твёрдые — металлы побочной подгруппы VI группы (VIB группы) Периодической системы Д. И. Менделеева. Так, хром по твёрдости приближается к алмазу. Самые мягкие — металлы главной подгруппы I группы (IA группы) Периодической системы Д. И. Менделеева — щелочные металлы. Например, натрий и калий легко режутся ножом.

По плотности металлы делят на лёгкие (плотность меньше 5 г/см3) и тяжёлые (плотность больше 5 г/см3). К лёгким относят щелочные, щёлочноземельные металлы и алюминий. Из переходных металлов сюда включают скандий, иттрий и титан. Эти металлы, благодаря лёгкости и тугоплавкости, всё шире применяют в различных областях техники.
Самый лёгкий металл — это литий (р = 0,53 г/см3). Самый тяжёлый — осмий (р = 22,6 г/см3).
Лёгкие металлы обычно легкоплавки, галлий может плавиться уже на ладони руки, а тяжёлые металлы — тугоплавки. Наибольшей температурой плавления, которая равна 3380 °С, обладает вольфрам. Это свойство вольфрама используют для изготовления ламп накаливания (рис. 29, 2). Кроме него в конструкцию лампы входят ещё семь металлов.
В Российской Федерации в настоящее время, как и ранее в Евросоюзе и США, на государственном уровне принято решение о замене привычных ламп накаливания на более экономичные и долговечные современные лампы, например галогенные, люминесцентные и светодиодные. Галогенная лампа (рис. 29, 2) — это та же лампа накаливания с вольфрамовой нитью, заполненная инертными газами с добавкой паров галогенов (брома или иода).

Люминесцентные (рис. 29, 3) — это хорошо знакомые вам лампы дневного света, имеющие один существенный недостаток — они содержат ртуть, а потому нуждаются в соблюдении особых правил утилизации на специальных пунктах приёма. Светодиодные лампы (рис. 29, 4) — самые экономичные и самые долговечные (срок работы до 100 тыс. ч), но пока и самые дорогие из ламп.
В технике, как вы уже знаете, металлы делят на чёрные (железо и его сплавы) и цветные (все остальные, более подробно о них будет рассказано в следующем параграфе) (рис. 30). Золото, серебро, платину и некоторые другие металлы относят к драгоценным металлам (рис. 31). 1


1. Обратитесь к электронному приложению. Изучите материал урока и выполните предложенные задания.
2. Найдите в Интернете электронные адреса, которые могут служить дополнительными источниками, раскрывающими содержание ключевых слов и словосочетаний параграфа. Предложите учителю свою помощь в подготовке нового урока — сделайте сообщение по ключевым словам и слово-сочетаниям следующего параграфа.

1. Назовите самый легкоплавкий металл.
2. Какие физические свойства металлов используют в технике?
3. Фотоэффект, т. е. свойство металлов испускать электроны под действием лучей света, характерен для щелочных металлов, например для цезия. Почему? Где это свойство находит применение?
4. Какие физические свойства вольфрама лежат в основе его применения в лампах накаливания?
5. Какие свойства металлов лежат в основе образных литературных выражений: «серебряный иней», «золотая заря», «свинцовые тучи»?
- Физические свойства металлов. Ответы
Источник
