Какой продукт образуется при окислении этанола

Окисление спиртов и фенолов
Для окисления гидроксисоединений используются соединения марганца(IV), марганца(VII), хрома(VI), оксиды металлов (Cu, Zn, Ag) и др.
Легкость окисления одноатомных спиртов уменьшается в ряду:
CH3OHМетанол CH3OH – сильный яд. Его высокая токсичность обусловлена лёгкой окисляемостью с образованием ядовитых продуктов (попадание в организм 5-10 г метанола приводит к слепоте, а 25-30 г – к смерти). > первичные ≥ вторичные >> третичные.
Первичные спирты при окислении образуют альдегиды, которые затем легко окисляются до карбоновых кислот. В реакции участвует ближайшая к гидроксильной группе связь С–Н, по которой происходит внедрение атома кислорода. От образовавшегося при этом неустойчивого алкандиола-1,1Алкандиолы-1,1 – двухатомные спирты с ОН-группами при одном и том же атоме углерода R–CH(OH)2 и R2C(OH)2. Неустой-чивые соединения. Подобно угольной кислоте (O=C(OH)2 → CO2 + H2O) они легко отщепляют воду и превращаются в альдегиды R–CH=O или кетоны R2C=O. отщепляется вода с разрывом связей О–Н и С–ОH.
Окисления альдегида в карбоновую кислоту можно избежать, удаляя его из реакционной смеси путем отгонки
(альдегид кипит при более низкой температуре, так как его молекулы не ассоциированы за счет водородных связей).
При окислении вторичных спиртов получают кетоны.
Промышленное значение имеет реакция окисления вторичного алициклического спирта циклогексанола до кетона циклогексанона:

Это одна из стадий в многостадийном синтезе ε-капролактама, из которого получают поликапролактам (капрон).
Окисление первичных и вторичных спиртов происходит также в результате реакции дегидрирования (отщепления водорода) при пропускании паров спирта над нагретым катализатором (Cu, соединения Ag, Cr, или Zn). В этих условиях процесс идёт как внутримолекулярная окислительно-восстановительная реакция.
Данный метод позволяет превращать первичные спирты в альдегиды без их дальнейшего окисления до кислот.
Третичные спирты более устойчивы к действию окислителей. Если первичные и вторичные спирты окисляются в кислой, нейтральной и щелочной средах, то третичные спирты реагируют лишь в жестких условиях – кислая среда, повышенная температура. Это приводит к разрушению углеродного скелета молекулы и образованию смеси продуктов – карбоновых кислот и кетонов с меньшим числом углеродных атомов.
- Процесс идет через стадию дегидратации спирта с последующим деструктивным (жестким) окислением алкена. Например:
- Устойчивость третичных спиртов при окислении позволяет отличить их от первичных и вторичных спиртов по реакции с разбавленным щелочным раствором перманганата калия.
Многоатомные спирты при окислении образуют различные вещества, поскольку в реакцию могут вступать одна или несколько гидроксильных групп. Состав продуктов окисления зависит от взаимного положения ОН-групп в молекулах полигидроксильного соединения и природы окислителя.
Соединения с ОН-группами у соседних атомов углерода (1,2-диолы, 1,2,3-триолы и т.п.) окисляются наиболее легко. В зависимости от условий их окисление происходит с сохранением
C–C-связей
углеродного скелета (пример 1) или с их разрывом (пример 2) вплоть до полного разрушения С-скелета (пример 3).
Пример 1. Окисление этиленгликоля при действии CrO3 или HNO3

Пример 2. Окисление раствором перманганата калия в кислой среде при нагревании
Кетон R2C=O образуется из фрагмента, содержащего третичную спиртовую группу, а карбоновая кислота R’COOH – из фрагмента с вторичной группой ОН.
При наличии фрагмента с первично-спиртовой группой –CH2OH образуется CO2:
Пример 3. Взаимодействие глицерина с кристаллическим перманганатом калия (видео)
Реакция глицерина HOCH2–CH(OH)–CH2OH с тонко измельчённым кристаллическим KMnO4 начинается самопроизвольно и идёт с высокой скоростью при выделении большого количества тепла. При этом глицерин окисляется полностью до углекислого газа и воды:
2С3Н8О3 + 7О2 → 6СО2 + 8Н2О + Q
Характерной реакцией многоатомных спиртов с соседними ОН-группами является окисление водным раствором иодной кислоты HIO4, которая не окисляет одноатомные спирты и многоатомные спирты других типов. Подробнее…
Реакция протекает через стадию образования циклического сложного эфира иодной кислоты (иодата), который расщепляется далее по связи С–С с выделением иодноватой кислоты:
В отличие от деструктивного окисления перманганатом калия, продуктами реакции с иодной кислотой являются альдегиды и (или) кетоны.
В случае трёх соседних C–ОН-групп средняя группа окисляется до муравьиной кислоты НСООН:
Данная реакция, называемая гликольным расщеплением, используется для установления числа и положения ОН-групп в полигидроксильных соединениях (главным образом, в углеводах) путём определения количества израсходованного окислителя и анализа продуктов окисления.
Кроме иодной кислоты для гликольного расщепления применяют также тетраацетат свинца (CH3COO)4Pb в органическом растворителе.
Фенолы окисляются легче спиртов. Эти реакции протекают многоступенчато с образованием довольно сложной смеси продуктов. Многие из фенолов, являясь бесцветными веществами, при стоянии на воздухе приобретают окраску за счёт примеси продуктов окисления.
Действие на фенол сильных окислителей (CrО3, хромовая смесь) приводит к образованию пара-бензохинона (наряду с другими продуктами окисления). Реакция идёт с отщеплением наиболее подвижного атома водорода в пара-положении бензольного кольца.
Значительно легче окисляются многоатомные фенолы.
Поэтому они являются более сильными восстановителями, чем одноатомные фенолы. Например, двухатомный фенол гидрохинон применяется как антиоксидант и ингибитор радикальной полимеризации, а также как проявитель в классической фотографии:

Наиболее сильными восстановителями являются трёхатомные фенолы, легко окисляющиеся даже кислородом воздуха. На этом основано применение в газовом анализе щелочного раствора пирогаллола, количественно поглощающего кислород.
Предельное окисление гидроксисоединений до CO2 и Н2О происходит при их горении, например:
2CH3OH + 3O2 2CO2 + 4H2O
Полное окисление метанола идет схеме:
При сгорании спиртов выделяется большое количество тепла.
C2H5OH + 3O2 2CO2 + 3H2O + 1370 кДж
Благодаря высокой экзотермичности реакции горения этанола, он считается перспективным и экологически чистым заменителем бензинового топлива в двигателях внутреннего сгорания. В лабораторной практике этанол применяется как горючее для “спиртовок”.
- Видеоопыт “Взаимодействие глицерина с кристаллическим перманганатом калия”.
Источник
В организм поступают и в результате метаболизма образуются в клетках головного мозга и печени, в других тканях, при жизнедеятельности микрофлоры кишечника различные спирты (алифатической, ароматической, стероидной природы, ретиноиды, фарнезол и др.) и альдегиды (ароматические, алифатические, продукты пероксидации липидов и др.), которые могут являться промежуточными метаболитами или конечными продуктами.
Взаимопревращение спиртов и альдегидов осуществляют алкогольдегидрогеназы. Их существует 6 подклассов, в каждом подклассе имеются многочисленные изоферменты, обнаруженные во многих тканях.
С медицинской и социальной точки зрения определенный интерес вызывает метаболизм этилового спирта в организме человека.
Этанол является энергетически богатым соединением: при метаболизме 125 г этанола количество образующегося НАДН такое же, как при окислении 500 г глюкозы. При полноценном питании и частом потреблении этилового спирта, например, в виде пива, “этанольный” ацетил-SКоА не столько сгорает в ЦТК, сколько используется для синтеза холестерола и триацилглицеролов, то есть происходит переход энергии этанола в запасную форму, что приводит к гиперлипидемии, “пивному ожирению” и жировой инфильтрации печени.
Обезвреживание этанола
Метаболизм поступающего этанола в организме происходит преимущественно в печени тремя способами.
Первый путь начинается в цитозоле и заключается в окислении спирта по алкогольдегидрогеназному пути до ацетальдегида, который переходит в митохондрии и окисляется до уксусной кислоты. Последняя в виде ацетил-SКоА поступает в ЦТК. Через этот путь проходит 80-90% всего этанола.
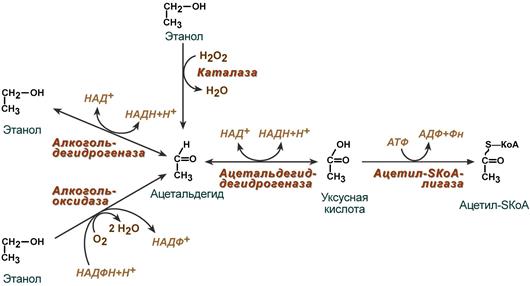
Реакции окисления этанола и ацетальдегида
За окисление 10-20% этанола отвечает алкогольоксидаза (цитохром P450), также называемая микросомальная этанолокисляющая система (МЭОС). При регулярном поступлении этанола доля микросомального окисления возрастает (до 7 раз), так как этанол является индуктором алкогольоксидазы и количество ее молекул увеличивается.
Третий способ – реакция окисления этанола каталазой с использованием перекиси водорода. Протекает реакция в пероксисомах и цитозоле, главным образом, нервных клеток, значение ее не велико, не более 2%.
Побочные эффекты обезвреживания этанола
Поскольку при утилизации этанола образуется большое количество НАДН, то в цитозоле гепатоцитов активируется 11-я реакция гликолиза (превращение пирувата в лактат) и восстановление диоксиацетонфосфата в глицерол-3-фосфат. Это приводит к гипогликемии в постабсорбтивный период, так как пировиноградная кислота и диоксиацетонфосфат являются субстратами глюконеогенеза.
Одновременно накопление “алкогольного” ацетил-SКоА ингибирует пируватдегидрогеназу, что еще больше усиливает накопление лактата. Накопление молочной кислоты в крови обусловливает лактатацидемию (лактоацидоз).
Одновременно из-за относительной недостаточности оксалоацетата, использованного в глюконеогенезе, избыток “алкогольного” ацетил-SКоА не успевает окислиться в цикле трикарбоновых кислот и перенаправляется на синтез кетоновых тел, что обеспечивает возникновение кетоацидоза.
Если запасы гликогена в печени изначально невелики (голодание, недоедание, астеническое телосложение) или израсходованы (после физической работы), то при приеме алкоголя натощак гипогликемия наступает быстрее и может быть причиной резкого ухудшения самочувствия и потери сознания. К этому стоит добавить сильный диуретический эффект этанола (подавление секреции вазопрессина), ведущий к быстрому обезвоживанию организма и снижению кровоснабжения головного мозга со всеми вытекающими последствиями.
Токсичность ацетальдегида
Ацетальдегид может неферментативно связывать сульфгидрильные (HS-) группы белков и гетерополисахаридов, и аминогруппы (NH2-) белков, нуклеиновых кислот, фосфолипидов и других соединений:
1. Повреждение нативной структуры белков, например
- ведет к изменению активности ферментов дыхательной цепи и разобщению окислительного фосфорилирования,
- снижает полимеризацию тубулина микротрубочек, что проявляется как возникновение телец Мэллори в гепатоцитах (алкогольный гиалин),
- ацетальдегид-белковые комплексы запускают цитотоксические механизмы иммунокомпетентных клеток по отношению к печени и к другим органам.
2. Изменение структуры мембранных фосфолипидов – активация перекисного окисления и повышение текучести мембран. Возрастает проницаемость мембран для воды и электролитов, происходит набухание клеток и их дисфункция.
3. Появление мутаций в ДНК и, как следствие, снижение репарации, стимулированный апоптоз клеток или канцерогенез, особенно для клеток печени,
Ацетальдегид вступает в неферментативную реакцию конденсации с катехоламинами, а продукты реакции обладают морфино- и опиатоподобным действием. Выявлено, что большинство проявлений алкоголизма связано с воздействием на организм не самого этанола, а ацетальдегида. Под его действием увеличивается образование дофамина и норадреналина в нервной системе и органах, и с накоплением дофамина часто связано развитие абстинентного синдрома и белой горячки.
Спиртовое брожение
Образование этилового спирта из глюкозы происходит в анаэробных условиях в дрожжах и некоторых видах плесневых грибков. Суммарное уравнение реакции:
C6H12О6→ 2 CО2 + 2 С2Н5ОН
До стадии образования пирувата реакции спиртового брожения совпадают с реакциями гликолиза. Отличия заключаются только в дальнейшем превращении пировиноградной кислоты. Цель этих превращений у указанных организмов та же, что и в гликолизе (молочнокислом брожении) – удалить пируват из клетки и окислить НАДН, который образовался в 6-й реакции.
Специфические реакции спиртового брожения
Источник
