Какой продукт преимущественно образуется при присоединении одной молекулы бромоводорода к

Реакции присоединения к сопряжённым диенам
Гидрирование (присоединение водорода)
При взаимодействии бутадиена-1,3 с водородом в момент выделения (например, в реакции натрия со спиртомC2H5OH + Na• → C2H5O–Na+ + H•) получается бутен-2, то есть происходит 1,4-присоединение. Формально этот процесс можно представить следующим образом: при действии реагента двойные связи разрываются, к крайним атомам углерода С(1) и С(4) присоединяются атомы водорода (H•), а свободные валентности (неспаренные электроны) образуют π-связь между атомами С(2) и С(3):

В присутствии катализатора Ni образуется продукт полного гидрирования:
 (н-бутан)
(н-бутан)
Изопрен реагирует аналогично:
CH2=С(CH3)–CH=CH2 + 2H (CH3)2C=CH–CH3 (2-метилбутен-2)
CH2=С(CH3)–CH=CH2 + 2H2 (Ni, t) (CH3)2CH–CH2–CH3 (2-метилбутан)
Галогенирование (присоединение галогенов)
Хлор и бром легко присоединяются к алкадиенам по электрофильному механизмуЭлектрофильный механизм характерен для реакций, в которых молекула органического вещества подвергается действию электрофильного реагента (электрофила) – частицы (катиона или молекулы), имеющей свободную орбиталь на внешнем электронном уровне и способной принять пару электронов при образовании ковалентной связи по донорно-акцепторному механизму. подобно алкенам.
При взаимодействии эквимолярных количеств бутадиена-1,3 и брома образуются продукты как 1,2-, так и 1,4-присоединения:

Примечание. По правилам систематической номенклатуры при составлении названий ненасыщенных галогеноуглеводородов нумерацию углеродной цепи начинают от конца, ближайшего к кратной связи. Именно поэтому продукт 1,2-присоединения в данной реакции имеет название 3,4-дибромбутен-1.
Cостав смеси образующихся продуктов зависит от температуры
При +40°C смесь продуктов реакции содержит 80% 1,4-дибромбутена-2 (1,4-присоединение) и 20% 3,4-дибром-бутена-1 (1,2-присоединение), а при -80°C соотношение продуктов 1,4- и 1,2-присоединения обратное (20% и 80%, соответственно).
реакции. При пониженной температуре преобладает продукт 1,2-присоединения, которое происходит с бóльшей скоростью, чем 1,4-присоединение.
Это объясняется тем, что образующиеся на лимитирующей стадии реакции промежуточные частицыО роли промежуточных частиц см. здесь.
– вторичные карбокатионы  (при 1,2-присоединении) более стабильны и поэтому легче образуются, чем первичные
(при 1,2-присоединении) более стабильны и поэтому легче образуются, чем первичные  (при 1,4-присоединении). Повышение температуры реакции смещает равновесие в сторону образования более термодинамически устойчивыхЧем больше заместителей при двойной связи, тем выше термодинамическая стабильность вещества:CH2=CHR 2C=CR2. продуктов 1,4-присоединения.
(при 1,4-присоединении). Повышение температуры реакции смещает равновесие в сторону образования более термодинамически устойчивыхЧем больше заместителей при двойной связи, тем выше термодинамическая стабильность вещества:CH2=CHR 2C=CR2. продуктов 1,4-присоединения.
Следует отметить, что 1,4-присоединение реагентов (кроме водорода) к бутадиену-1,3 приводит к образованию смеси цис- и транс-изомеров (например, изомеры 1,4-дибромбутена-2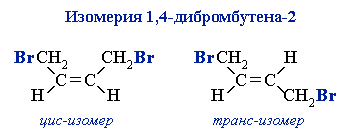 ).
).
В избытке брома присоединяется еще одна его молекула по месту оставшейся двойной связи с образованием 1,2,3,4-тетрабромбутана1,2,3,4-Тетрабромбутан образуется в этой реакции в виде смеси стереоизомеров, так как в молекуле содержатся два асимметрических атома углерода: С(2) и С(3).:
CH2Br–CHBr–CHBr–CH2Br
В случае изопрена, кроме реакций 1,2- и 1,4-присоединения, возможно также 3,4-присоединение:
CH2=С(CH3)–CH=CH2 + Br2 CH2=С(CH3)–CHBr–CH2Br
При облучении УФ-светом или в присутствие соединений – источников свободных радикалов (например, пероксидов ROOR) галогены присоединяются к сопряжённым диенам по радикальному механизму с образованием 1,2- (3,4-), 1,4-дигалогеналкенов и 1,2,3,4-тетрагалогеналканов.
Гидрогалогенирование (присоединение галогеноводородов)
Присоединение HCl и HBr к сопряженным диенам происходит также в 1,2- (3,4-) и 1,4-положения и подчиняется тем же закономерностям: с повышением температуры увеличивается доля продукта 1,4-присоединения.

1,2-присоединение – кинетически контролируемая реакция;
1,4-присоединение – термодинамически контролируемая реакция.
Энергетическая диаграмма (интерактивная анимация)
Присоединение воды и других полярных реагентов происходит по электрофильному механизму (как в алкенах). В реакциях несимметричных соединений соблюдается правило Марковникова.
Диеновый синтез (реакция Дильса-Альдера)
В органическом синтезе широко применяется реакция присоединения к сопряженным диенам соединений, содержащих кратные связи (так называемых диенофилов).
Реакция идет как 1,4-присоединение и приводит к образованию циклического продукта (такие реакции называют реакциями циклоприсоединения):
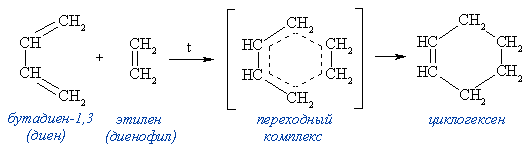
Этилен является слабым диенофилом и данная реакция идёт с невысоким выходом. Обычно в качестве диенофилов используют алкены и алкины, кратная связь у которых активирована электроноакцепторной группой (например, CH2=CHCOOH, CH2=CHCHO, CH2=CHCN, CH2=CHCOOR и т.п.), а также вещества, содержащие в молекуле группы —C=N, =C=N—, =С=О, — N=N—, =S=О и др.
К реакциям присоединения относится также характерная для диенов реакция полимеризации. Этот процесс имеет важное значение в производстве синтетических каучуковКаучуки – это эластичные высоко-молекулярные вещества (эластомеры), из которых путём вулканизации (например, нагреванием с серой) получают резину..
Источник
ПРАВИЛО МАРКОВНИКОВА
- При взаимодействии пропена с бромом при обычных условиях преимущественно образуется:
- 1-бромпропан
- 2-бромпропан
- 1,1-дибромпропан
- 1,2-дибромпропан
2.При взаимодействии пропена с хлором при 500℃ преимущественно образуется:
1) 1,2-дихлорпропан
2) 3-хлорпропан
3) 3-хлорпропен
4) 1,1-дихлорпропан
3. При взаимодействии пропена с бромоводородом преимущественно образуется:
1) 1-бромпропан
2) 2-бромпропан
3) 1,1-дибромпропан
4)1,2-дибромпропан
4. При гидратации бутена-1 преимущественно образуется:
1) бутанол-1
2) бутанол-2
3) бутаналь
4) бутанон
5. При гидратации бутена-2 преимущественно образуется:
1) бутанол-1
2) бутанол-2
3) бутаналь
4) бутановая кислота
6. При взаимодействии бромоводорода с 2-бромпропеном преимущественно образуется:
1) 1,1-дибромпропан
2) 1,2-дибромпропан
3) 2,2-дибромпропан
4)1,3 -дибромпропан
7. При взаимодействии 1 моль пропина с 1 моль хлороводорода преимущественно образуется:
1) 2-хлорпропан
2) 2-хлорпропен
3) 1-хлорпропан
4) 1-хлорпропен
8. Один и тот же продукт образуется при гидратации каждого из двух веществ:
1) бутена-1 и бутена-2
2) бутена-1 и бутина-1
3) бутина-1 и бутена-2
4) бутена-1 и пропина
9. При взаимодействии акриловой кислоты с бромоводородом преимущественно образуется:
1)1-бромпропановая кислота
2) 2-бромпропановая кислота
3) 3-бромпропановая кислота
4) α-бромпропионовая кислота
10. Взаимодействие бутена-1 с бромоводородом в присутствии пероксида водорода приводит к преимущественному образованию:
1) 1-бромбутана
2) 2-бромбутана
3) 1-бромбутена-1
4) 2-бромбутена-2
11. По правилу Марковникова происходит взаимодействие:
1) пропена и бромоводорода:
2) бутена-1 и воды
3) бутена-1 и брома
4) бутена-2 и водорода
5) бутена-1 и хлороводорода
6) этилена и кислорода
12. Для взаимодействия пропена и бромоводорода справедливы утверждения:
1) в ходе реакции образуется 1,2-дибромпропан
2) реакция протекает по правилу Зайцева
3) реакция протекает по правилу Марковникова
4) в ходе реакции образуется 2-бромпропан
5) реакция относится к реакциям замещения
6) реакция идет по иному механизму
13. Для взаимодействия бутена-1 и хлороводорода справедливы утверждения:
1) в ходе реакции образуется 1,2-дихлорбутан
2) реакция протекает по правилу Марковникова
3) реакция является эндотермической
4) в ходе реакции образуется 2-хлорбутан
5) реакция относится к реакциям замещения
6) реакция идет по ионному механизму
14. Правило Марковникова не используют для объяснения хода реакции между:
1) бутеном-1 и бромоводородом
2) пропеном и водородом
3) пропеном и водой
4) бутеном-2 и бромоводородом
5) бутеном-1 и бромом
6) бутеном-1 и водой
15.Бромирование метана:
1) осуществляется по правилу Марковникова
2) относится к радикальным реакциям
3) начинается с процесса разрыва связи в молекуле брома
4) протекает по схеме: CH4 + Br2 →CH2Br2+H2
5) протекает не так энергично, как реакция хлорирования
6) относится к реакциям присоединения
16. Радикал этил C2H5- :
1) образует заряд -1
2) образуется при присоединении HCl к этилену
3) имеет нечетное число электронов
4) содержит атомы углерода в состоянии sp3-гибридизации
5) образуется при присоединении Cl2 к этену
6) электронейтрален
17. Карбокатион CH3-CH+-CH3:
1) образуется при хлорировании пропана
2) образуется при присоединении НВr к молекуле прпена
3) более устойчив, чем кабокатион CH3-CH2-CH2+
4) содержит атомы углерода только в sp3-гибридном состоянии
5) содержит центральный атом углерода в состоянии sp2-гибридизации
6) имеет линейное строение
18. Карбокатион CH3-CH2-CH2+:
1) образуется при бромировании пропана
2) образуется как основной промежуточный продукт при присоединении HBr к молекуле пропена
3) менее устойчив, чем карбокатион CH3-CH+-CH3
4) содержит атомы углерода только в sp3-гибридном состоянии
5) содержит атомы углерода в состоянии sp3- и sp2-гибридизации
6) содержит четное число электронов
19. При присоединении бромоводорода к пропену :
1) преимущественно образуется 2-бромпропавн
2) образуется 1-бромпропан и 2-бромпропан в равных соотношениях
3) происходит промежуточное образование катиона CH3-CH+-CH3
4) происходит промежуточное образование радикала CH3-CH2-CH2-
5) правило Марковникова не соблюдается
6) разрывается π-связь в молекуле пропена
20. При присоединении воды к пропену :
1) преимущественно образуется пропанол-1
2) образуется пропанол-1 и пропанол-2 в равных соотношениях
3) разрывается π-связь в молекуле пропена
4) происходит промежуточное образование катиона CH3-CH+-CH3
5) правило Марковникова соблюдается
6) происходит промежуточное образование радикала CH3-CH2-CH2-
ОТВЕТЫ:
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
4 | 3 | 2 | 2 | 2 | 3 | 2 | 1 | 3 | 1 |
11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
125 | 346 | 246 | 245 | 235 | 346 | 235 | 356 | 136 | 345 |
Источник
Рассмотрите реакцию присоединения бромоводорода к 2-метилбутену-2, Какой продукт образуется Рассмотрите механизм этой реакции и объясните, почему образуется именно этот продукт [c.218]
В результате присоединения бромоводорода к этилену образуется бромэтан (У) [c.201]
На метилциклопропан подействовали последовательно бромоводородом, цианидом калия, разбавленным раствором серной кислоты при нагревании. Напищите уравнения реакций и назовите полученные соединения. Объясните механизм реакции присоединения бромоводорода. [c.121]
Рассмотрите реакцию присоединения бромоводорода к 2-метилбутену-1. Рассмотрите механизм этой реакции и объясните, почему атом брома будет присоединяться ко второму, я не к первому атому С. [c.218]
Если органический синтез исходит из ахиральных соединений и проводится в нехиральной среде (под хиральной средой понимают, например, хиральный растворитель или хиральны катализатор), то нельзя получить один-единственный антипод. Результатом реакции всегда будет рацемическая форма. Это объясняется тем, что вероятности образования обоих антиподов совершенно одинаковы, так что они появляются в одинаковом количестве. В качестве примера приведем реакцию присоединения бромоводорода к бутену-1 [c.95]
При Присоединении бромоводорода по тройной связи также может наблюдаться эффект Караша. [c.157]
Таким образом, изменение механизма реакции с гетеролитического на гомолитический приводит к изменению ее результата бромоводород в условиях гомолиза связи Н—Вг присоединяется к алкену вопреки правилу Марковникова. Этот эффект был открыт Харашем, поэтому такое присоединение бромоводорода часто называют гидробромированием по Харашу. [c.54]
Двойная связь С = С в ациклических или циклических соединениях— это то место, по которому протекают различные реакции, чаще всего —присоединение, как электрофильное, так и радикальное. В качестве примера рассмотрим присоединение бромоводорода и водорода. Большое практическое значение имеют также окисление и полимеризация алкенов. [c.121]
Напишите уравнения реакций присоединения бромоводорода к пропилену и трифторпропилену СРз—СН = СН2. Объясните направления реакций, ис-пользуя электронную теорию. [c.21]
Реакция присоединения бромоводорода к пропену может протекать в двух направлениях [c.297]
Циклопропан получают в промышленных масштабах по реакции Густавсона действием цинка на 1-хлор-З-бромпропан, который синтезируют присоединением бромоводорода к аллнлхлориду в присутствии кислорода воздуха. Напишите уравнения соответствующих реакций и рассмотрите механизм присоединения бромоводорода к аллилхлориду в присутствии кислорода воздуха. [c.119]
Эту реакцию можно использовать как метод синтеза первичных бромидов из а-алкенов по конечному результату она похожа на присоединение бромоводорода к алкенам против правила Марковникова. [c.69]
Электрофильное присоединение бромоводорода [c.121]
Если присоединение бромоводорода к несимметрично замещенным алкенам проводится на свету в присутствии кислорода или пероксида, то реакция протекает непо ионному, а по радикальному механизму и приводит к продукту, отличному от продукта электрофильного замещения [c.124]
Если гидробромирование диенового углеводорода проводят при низкой температуре, обратная реакция дегидробромирования не протекает. В этих условиях реакция контролируется кинетикой и основным продуктом реакции оказывается продукт 1,2-присоединения. Речь идет, таким образом, о кинетически контролируемой реакции. Энергетическая диаграмма присоединения бромоводорода к 1,3-бутадиену показана на рис. 7.3. [c.348]
В несимметрично замещенных алкинах присоединение бромоводорода протекает по правилу Марковникова [c.127]
Реакция. Присоединение бромоводорода по терминальной двойной связи С=С. В описанных условиях реакции (отсутствие кислорода и света) должен образоваться 2-бромгептан (продукт присоединения по правилу Марковникова), но образуется только 1-бромгептан (исключе- [c.65]
Изучение кинетики реакции присоединения бромоводорода к олефинам показало, что реакция третьего порядка [c.496]
Присоединение бромоводорода по терминальной двойной и све описанных условиях реакции (отсутствие кислорода [c.65]
Химические свойства углеводородов определяются реакционной способностью углерод-углеродных и углерод-водородных связей, т.е. связей ковалентных и малополярных. Введение в углеродный скелет органической молекулы заместителя приводит к образованию связи углерод-элемент, которая, как правило, полярна, поскольку атомы углерода и элемента обычно заметно различаются по электроотрицательности (см. разд. 1.1.3). В полученных производных реакционным центром чаще всего являются атомы углерода, связанного с заместителем, или самого заместителя. При изучении реакционной способности органических соединений, содержащих заместители в углеродном скелете, следует обращать особенное внимание на взаимное влияние замещающей группы (или атома) и углеводородного радикала. Простейшими соединениями, при рассмотрении которых могут быть выявлены особенности такого-влияния, являются галогенпроизводные углеводородов. Введение атомов галогена в молекулу углеводорода отражается на свойствах углеродного скелета. Примерами могут служить присоединение бромоводорода к [c.116]
Напишите уравнение реакции присоединения бромоводорода к 3,3,3-трифторпропену. [c.303]
Выход продуктов 1,4- или 1,2-присоединения определяется характером реагента и условиями проведения реакции. Например, присоединение бромоводорода в присутствии пероксидных соединений идет в 1,4-положение, а в отсутствие— в положение 1,2. [c.73]
При присоединении галогеноводородов к несимметричным алкенам возможно образование двух продуктов. Присоединение бромоводорода к пропену может приводить к образованию 2-бромпропана или 1-бром-пропана [c.586]
Если кольцо циклопропана находится в сопряжении с кратной связью, то присоединение веществ типа НХ происходит – вопреки правилу Марковникова. Напишите уравнение реакции присоединения бромоводорода к бензоилциклопропану и объясните ее направление. [c.122]
В сим метрично замещенных алкенах присоединение бромоводорода приводит к единственному продукту [c.121]
Однако присоединение бромоводорода к несимметрично замещенным алкенам может протекать двумя способами, так что, например, в случае пропена образуется или 2-бромопропан, или [c.121]
Объясните механизм реакции электрофиль-вого присоединения бромоводорода (по стадиям) а) к изобутену б) к трнметилэтилену в) к а,р-ди-этилэтилену. В каких случаях следует руководствоваться правилом Марковникова [c.22]
Напишите уравнения реакций присоединения бромоводорода к следующим кислотам а) акриловая б) метакриловая. Объясните порядок присоединения галогенозодорода. [c.82]
Стереоспецифичное анти-присоединение бромоводорода характерно прежде всего для циклоалкенов. Арилалкены, для которых возможна стабилизация промежуточно образующегося карбкатиона за счет сопряжения с соседним фрагментом арена, как и в реакции присоединения галогенов, реагируют со значительным участием схемы син-присоединения. [c.257]
В результате присоединения бромоводорода к этолену образуется бромэтан (Y) [c.201]
Столь же селективно может быть выполнено получение а М-аддукта 127 с помощью последовательности неизогипсических стадий — гидробори-рования (восстановления) и окисления. Отметим также, что, если на второй стадии использовать п качестве окислителя не пероксид водорода, а бром, то продуктом реакции будет аМ-бромид 128. Кстати, этот же продукт может быть получен непосредственно из алкена путем гомолитиче-ского присоединения бромоводорода. [c.138]
Опишите механизм реакции присоединения бромоводорода к 2-метил-пропену Почему образуется только один из двух возможных продуктов [c.89]
Однако наблюдается и отклонение от правила Марковникова. Так, если реакция идет по радикальному механизму (в присутствии пероксидных соединений или кислорода), то, как показал М. Ха-раш (1933), порядок присоединения бромоводорода будет обратным правилу Марковникова ( пероксидный эффект Хараша) [c.67]
Пероксидный эффект имеет место только в случае присоединения бромоводорода. При присоединении к алкенам НР, Н1, Нг804, НгО и частично НС пероксиды не влияют на направление присоединения. [c.67]
Источник
Гидрирование и галогенирование. Двойные связи дивинила реагируют не каждая сама по себе, а как единая p-система; атака мезомерного катиона нуклеофилом Вr- приводит к продуктам 1,2- и 1,4-присоединения, поскольку именно второй и четвертый атомы углерода сопряженной системы двойных связей несут в этом катионе положительный заряд:
Присоединение второй молекулы реагента дает один насыщенный продукт – 1,2,3,4-тетрабромбутан.
Аналогично, ступенчатое гидрирование бутадиена-1,3 протекает через образование бутена-1 (продукт 1,2-присоединения) и бутена-2 (продукт 1,4-присоединения), а полное гидрирование приводит к бутану.
Взаимодействие бутадиена-1,3 с хлороводородом происходит по механизму электрофильного присоединения (АЕ). При разрыве единой p-электронной системы сопряженного диена могут образовываться два карбкатиона:
Катион (I) представляет собой мезомерный катион, так как p-электроны двойной связи взаимодействуют с образующимся положительным центром, в результате чего происходит перераспределение электронной плотности:
Образовавшийся ион более устойчив, чем ион (II), в котором л-связь непосредственно не участвует во взаимодействии с карбкатионным центром и, кроме того, индуктивный эффект соседнего насыщенного атома углерода уменьшен под влиянием ненасыщенной винильной группы. Поэтому преимущественно образуется карбкатион (I), который на втором этапе реакции может связаться с хлорид-анионом через один из двух атомов углерода (центральный атом аллильного катиона не может образовывать новую связь):
Соотношение количеств изомеров (III) и (IV) зависит от условий проведения процесса. При обычных условиях преобладает продукт (III). Согласно общему механизму реакций присоединения анион хлора должен атаковать карбкатионный центр с противоположной стороны по отношению к той, где образовалась связь С-Н, поэтому более доступным для атаки оказывается самый удаленный концевой атом углерода аллильного иона.
2-метилбутадиена-1,3 гидрохлорирование эквимолярным количеством HCl
преимущественно дает 4-хлор-2-метилбутен-2.
Гибридный катион (I) имеет положительный заряд частично на третичном атоме углерода; в гибридном катионе (II) положительный заряд распределен между вторичным и первичным С-атомами. Таким образом гибрид (I) более стабилен и будет промежуточно образующимся в реакции карбкатионом. 1,4-Присоединение хлороводорода к изопрену дает
Электрофильное и радикальное присоединение к сопряженным диенам протекает легче, чем у алкенов. Это объясняется тем, что из диенов легче образуются карбкатионы или радикалы аллильного типа, которые стабильнее насыщенных карбкатионов или радикалов.
Диеновая конденсация (реакция Дильса-Альдера).При наличии у диенов цис-сопряженной системы двойных связей происходит их взаимодействие с непредельными соединениями (диенофилами) по типу 1,4-циклоприсоеди-нения, причем образующиеся с высокими выходами вещества (аддукты) содержат шестичленный цикл.
бутадиен-1,3 малеиновый аддукт
ангидрид
(диенофил)
Полимеризация и сополимеризация. Сопряженные диены более склонны к полимеризации, чем алкены. В зависимости от строения исходного сопряженного диена, условий реакции, катализатора возможно образование полимерной цепи как за счет 1,4-, так и 1,2-присоединения. Практическое значение имеют полимеры, полученные в результате 1,4-присоединения.
полимер
Натуральный каучук является полимером 2-метилбутадиена-1,3 (Х = СН3) и по строению он представляет собой цис-полиизопрен.
При сшивании линейных макромолекул каучука, как правило, сульфидными мостиками, он превращается в резину, теряет пластичность и приобретает упругость. Процесс превращения каучука в резину называется вулканизацией:
В настоящее время налажено производство различных видов каучуков, основанные на сополимеризации сопряженных диенов с прочими мономерами:
сополимер (например: Х = С6Н5 – бутадиен-стирольный каучук;
CN – бутадиен-нитрильный каучук и др.)
Контрольные вопросы к главе 3 «Диеновые углеводороды»
№ 1. Почему в случае присоединения хлороводорода к бутадиену-1,3 образуется смесь 3-хлорбутена-1 и 1-хлорбутена-2, в которой преобладает второе из названных соединений.
№ 2. При 1,4-присоединении хлороводорода к 2-метилбутадиену-1,3 (изопрену) в качестве основного продукта образуется 1-хлор-3-метилбутен-2, а не 1-хлор-2-метилбутен-2. Почему ?
№ 3. Какой из диенов – бутадиен-1,3 , изопрен (2-метилбутадиен-1,3) или пиперилен (пентадиен-1,3) при взаимодействии с 1 моль бромоводорода при 25 0С дает только один продукт?
№ 4. Изобразите конфигурации цепей полимеров, полученных из бута-диена-1,3 в результате: (а) цис-1,4-присоединения; (б) транс-1,4-присоединения.
Что образуется в результате озонолиза полученных полимерных продуктов?
№ 5. При термической полимеризации бутадиена-1,3 в качестве побочного продукта образуется циклический димер, не склонный к дальнейшей полимеризации. Это вещество при гидрировании дает этилциклогексан; способно присоединять 2 моль брома; в результате деструктивного окисления образует 3-карбоксигександиовую кислоту. Какое строение имеет молекула димера бутадиена-1,3?
№ 6.Напишите уравнения реакций диеновой конденсации: (а) бутадиена-1,3 с тетрацианоэтиленом; (б)1-винилциклопентена с акролеином СH2=CH-CN; (в) 2-метилпентадиена-2,4 с малеиновым ангидридом; (г) c 1,2-диметиленциклогексана с акролеином (д)циклогексадиена-1,3 с диметиловым эфиром ацетилендикарбоновой кислоты.
№ 7. Из каких реагентов можно получить следующие соединения по реакции Дильса—Альдера: № 8.Проведите озонолиз следующих соединений: (а)2-метилгептадиена-2,5; (б) 2,3-диметилциклогексадиена-1,3;
(в) мирцена (выделен из листьев лавра) (г) цингиберена
№ 9.Установите строение углеводородаС11Н20, если при окисление его хромовой смесью приводит к смеси бутанона-2, бутандиовой кислоты и пропионовой кислоты.
№ 10. Витамин D2 представляет собой непредельный спирт С28Н44О, в котором нет тройных связей. При каталитическом гидрировании он дает соединение С28Н52О. Сколько двойных связей содержит молекула витамина D2 ?
АЛКИНЫ
Определение.Алкины – ненасыщенные углеводороды, содержащие тройную связь и образующие гомологический ряд общей формулы СnH2n-2.
Изомерия.Обусловлена как разветвлением углеродного скелета (а), так и положением тройной связи (б); межклассовая изомерия с диенами (в).
CH3
|
(а) НC≡C–CH2–CH2–CH3 и НC≡C–CH–CH3
пентин-1 2-метилпропен-1
(б) НC≡C–CH2–CH2–CH3 и CH3–C≡C–CH2–CH3
пентин-1 пентин-2
(в) НC≡C–CH2–CH2–CH3 и CH2=CН–CН=CH–CH3
пентин-1 пентадиен-1,3
Геометрическая изомерия для алкинов не существует, т.к. атомы углерода при тройной связи и соседние углеродные атомы лежат на одной прямой.
Номенклатура.Простейший представитель имеет тривиальное название – ацетилен. По рациональной номенклатуре алкины рассматривают как замещен-ный ацетилен.По номенклатуре IUPAC название алкина происходит от названия соответствующего алкана заменой суффикса «-ан» на «-ин». Положение тройной связи обозначают цифрой, указывающей наименьший номер атома углерода главной цепи, при котором она находится.
СH3–CH2-CºC-CH2–CH2–CH2–CH3 этилбутилацетилен (рац.); октин-3 (IUPAC)
Строение.Атом углерода в ацетиленовых углеводородах находится в sp-гибридном состоянии. Две гибридные sp-орбитали каждого атома углерода (состоящие из одной s- и одной p-орбиталей) участвуют в образовании двух σ-связей: c cоседними атомами углерода и водорода. Две σ-связи расположены в одной плоскости под углом 1800 по отношению друг к другу. При этом у каждого атома углерода остается по два свободных негибридизованных р-электрона. Негибридизованные p-орбитали перекрываются в плоскостях, перпендикулярных плоскости σ-связи. Связи, образованные за счет такого перекрывания, являются π-связями. Таким образом, тройную связь рассматривают как состоящую из одной σ-связи и двух π-связей.
Источник
