На каких клетках содержится рецепторы к
Наиболее активно
синтезируемый и потребляемый Ig.
Хотя его концентрация
в сыворотке невелика (2-4 г/л) тотальная
продукция составляет 60% от всего объема
Ig.
Это связано с его постоянной экскрецией
ч/з слизистые барьеры.
Он покрывает
наружные оболочки кишечника, бронхов,
ротовой и носовой полости, влагалища,
глаза. За сутки во взрослом организме
производится до 15г Ig
А, в молозиве-
до 18г/л
Подклассы Ig
А1 и 2(секреторный)
Ig
А2 локализуется
в секретах слизистых оболочек и участвует
в нейтрализации патогенов, проникающих
в организм этим путем. Димеры
иммуноглобулина А секретируются
плазматическими клетками неинкапсулированной
лимфоидной ткани слизистых оболочек.
Затем они связываются с полииммуноглобулиновым
рецептором на базолатеральной поверхности
эпител-х кл-к и путем эндоцитоза
поглощаются этими клетками.
А2- устойчивый, за
счет секреторного компонета. Не проходит
через плаценту. Активен в противогельминтном
иммунитете.
21. Охарактеризуйте структуру IgE. На каких клетках содержатся рецепторы к данному иммуноглобулину?
IgE.
Концентрация этого класса иммуноглобулинов
в сыворотке исчезаюше мала, но он
выявляется на поверхностной мембране
базофилов и тучных клеток у любого
человека. Кроме того, IgE сенсибилизированы
клетки слизистых оболочек, в частности
носовой полости, бронхов и конъюнктивы.
Возможно, IgE имеют существенное значение
в ангигельминтозном иммунитете, однако
в развитых странах с ними чаще всего
связан патогенез аллергических
заболеваний, например бронхиальной
астмы и сенной лихорадки.
Ig
E содержится
в сыворотке в очень небольшом количестве.
Ig E не активирует систему
комплемента.
Его особенность состоит в том, что он
СПОСОБЕН ФИКСИРОВАТЬСЯ НА БАЗОФИЛАХ
И
ТУЧНЫХ КЛЕТКАХ, что объясняется наличием
в большом количестве на указанных
клеткахù
рецепторов
к Fc-фрагментам Ig E (см.
рис. на стр. 6). При последующем соединении
фиксированных
на тучных клетках или базофилах Ig E с
антигеном возникает дегрануляция этих
клеток
с высвобождением гистамина. Ig E называют
цитофильным
иммуноглобулином,
или
РЕАГИНОМ
за способность фиксироваться на названных
клетках. Он играет ведущую роль в
патогенезе
ал-лергических заболеваний (1 тип) и в
противогельминтном иммунитете.
IgE.
Молекула IgE состоит из более крупных
е-цеᴨȇй, содержащих большее число
аминокислотных остатков и образующих
пять доменов.
22. Понятие о моноклональных Ат. Применение в медицинской практике.
Моноклональные
антитела (мАТ).
Моноклональные антитела разработаны
на основе
гибридомной
технологии. Такие антитела моноспецифичны
и направлены к одному эпитопу
(антигенной
детерминанте) антигена.
Принцип
гибридомной технологии.
Первоначально проводят иммунизацию
мышей антигеном.
Из
селезенки иммунизированных животных
получают В-лимфоциты. Затем проводят
слияние этих
антителообразующих
В-клеток, которые долго не живут на
искусственных средах, с клетками опухоли
– плазмоцитомы
(миеломы), которые обладают способностью
опухолевых клеток непрерывно
делиться,
«бессмертные» клетки. Слияние
этих
клеток с помощью полиэтиленгликоля,
приводит
к появлению гибридных клеток – гибридом.
Получившаяся гибридома приобретает
способность к синтезу специфических
антител (от иммунных В-лимфоцитов) и
становится долгоживущей, непрерывно
делящейся (как миеломные). Накопившийся
клон клеток продуцирует моноклональные
АТ направленные к
единственной
антигенной детерминанте изучаемого
антигена. Масштабное
культивирование и
длительное
рекультивирование гибридомного клона
клеток позволяет получать мАТ в больших
количествах.
мАТ
оказались исключительно удобным и
широко применяемым в настоящее время
диагностическим
средством. С их помощью определяют
маркеры
клеточных популяций, гормоны,
медиаторы,
опухолевые маркеры и
т.д. даже в очень низких концентрациях.
мАТ широко
применяются
в ИФА.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
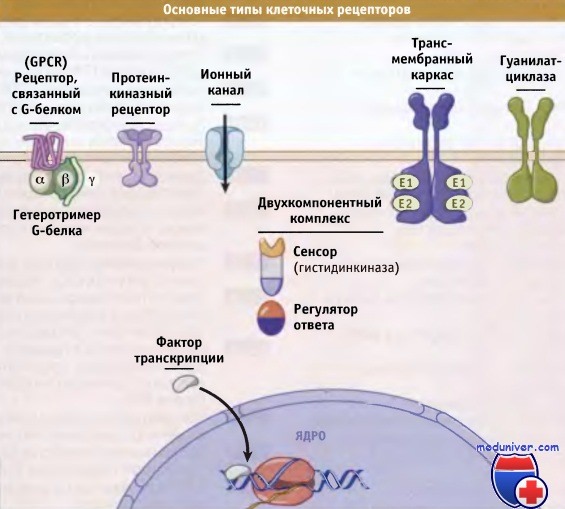
Строение и функции рецепторов клетки
• Рецепторы содержат домен, связывающий лиганд и эффекторный домен
• Модульный принцип организации рецептора позволяет использовать для самых разнообразных сигналов ограниченное число регуляторных механизмов
• Клетка может экспрессировать различные рецепторы для одного и того же лиганда
• В зависимости от эффекторного домена рецептора, один и тот же лиганд может по-разному действовать на клетку
Рецепторы обеспечивают реакцию клетки на огромное количество внеклеточных информационных молекул; поэтому клетка должна экспрессировать много разнообразных рецепторов, каждый из которых способен связываться со своим лигандом.
Вместе с тем, каждый рецептор должен быть способен инициировать ответную реакцию клетки. Таким образом, рецепторы содержат два функциональных домена: домен, связывающий лиганд, и эффекторный домен. Иногда они соответствуют определенным структурным доменам в молекулах белков.
Разделение связывающей и эффекторной функций позволяет рецепторам различных лигандов, посредством нескольких эффекторных доменов, генерировать ограниченное число эволюционно-консервативных внутриклеточных сигналов.
Фактически существует лишь ограниченное число семейств рецепторов, близких друг к другу по своему строению и сигнальным функциям.
Доменная природа рецепторов обеспечивает их другие полезные характеристики. Например, клетка может регулировать свою способность реагировать на внешний сигнал, изменяя интенсивность синтеза, деградацию рецептора, или его активность.
Наряду с этим, природа клеточного ответа обычно определяется рецептором и его эффекторным доменом, а не физико-химическими свойствами лиганда. Рисунок ниже иллюстрирует положение, согласно которому лиганд может связываться более чем с одним типом рецепторов и обеспечивать несколько типов ответа клетки и несколько разных лигандов могут действовать одинаковым образом, связываясь с функционально-близкими рецепторами.
Например, нейромедиатор ацетилхолин связывается с двумя классами рецепторов. К одному классу относятся ионные каналы, представители другого регулируют G-белки. Аналогичным образом стероидные гормоны связываются с ядерными рецепторами, которые ассоциируют с хроматином и регулируют транскрипцию, и с другими рецепторами на плазматической мембране.
Наоборот, когда множество лигандов связывается с рецепторами одного биохимического класса, они генерируют аналогичный клеточный ответ.
Например, достаточно часто клетка экспрессирует несколько разных рецепторов, стимулирующих образование внутриклеточных сигнальных молекул цАМФ.
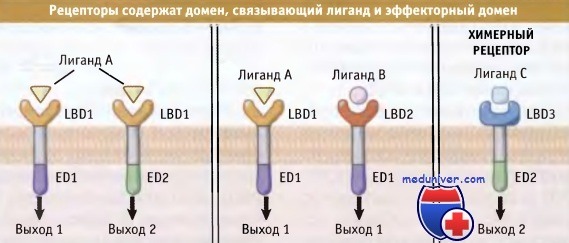
Рецепторы состоят из двух функциональных доменов, домена, связывающего лиганд (LBD), и эффекторного домена (ED).
Такая структура предполагает, что два рецептора, реагирующие с разными лигандами (в середине),
могут инициировать одинаковый ответ за счет активации сходных эффекторных доменов.
Возможно также, что клетка экспрессирует две изоформы рецептора (слева),
которые узнают один и тот же лиганд и обеспечивают развитие различных ответных реакций за счет различных эффекторных доменов.
Не исключено, что может образоваться искусственный химерный рецептор, обладающий новыми свойствами.
Влияние рецептора на клетку также будет в существенной степени зависеть от ее биологии и состояния в каждый данный момент времени.
В зависимости от специфики внешнего сигнала, домен связывания лиганда и эффекторный домен могут разобщаться. Например, родопсины млекопитающих и беспозвоночных передают сигналы через различные эффекторные G-белки (G1 и Gq соответственно).
Другим примером служит калмодулин, небольшой регуляторный белок млекопитающих, связывающий кальций. У растений он представлен отдельным доменом в составе больших белков.
Двухдоменная природа рецепторов позволяет клетке независимо регулировать связывание лиганда и ответ на него. Сродство лиганда к рецептору и/или способность связанного лиганда генерировать сигнал может измениться за счет его ковалентной модификации или при аллостерической регуляции.
Рецепторы можно классифицировать в зависимости или от природы связываемого ими лиганда, или характера генерируемого сигнала. Сигнал на выходе, который определяется эффекторным доменом, обычно лучше всего коррелирует с общим характером и последовательностью событий его передачи.
Однако особенно ценной для понимания организации эндокринной и нервной системы и для классификации многочисленных физиологических реакций, связанных с применением лекарств, оказывается фармакологическая классификация рецепторов в соответствии с их специфичностью к лигандам.
Экспрессии рецептора, который обычно в клетке отсутствует, часто оказывается достаточно для того, чтобы она приобрела чувствительность к соответствующему лиганду. Такая чувствительность развивается часто, и клетка экспрессирует другие компоненты, необходимые для дальнейшей передачи сигнала от рецептора.
Природа ответной реации клетки определяется ее биологией. В эксперименте реакцию клетки на то или иное соединение можно индуцировать с помощью кДНК, кодирующей рецептор. Например, рецепторы клеток млекопитающих могут экспрессироваться в дрожжах, и последние приобретают чувствительность к соответствующим лигандам.
Таким образом, пользуясь этой моделью, можно обнаруживать новые химические соединения (лекарственные средства), активирующие рецепторы.
Наконец, можно создавать химерные рецепторы путем слияния домена, связывающего лиганд от одного рецептора, с эффекторным доменом другого. Подобные химерные рецепторы при присоединении лиганда могут обеспечивать принципиально новый характер ответа.
За счет генетической модификации домена, связывающего лиганд, можно создать рецепторы, чувствительные к новым лигандам. Таким образом, исследователи могут управлять функциями клетки и ее чувствительностью к совершенно чужеродным химическим соединениям.

Рецепторы группируются в относительно небольшую группу семейств,
которые характеризуются общими механизмами действия и общностью структуры.
– Также рекомендуем “Рецепторы как катализаторы и амплификаторы”
Оглавление темы “Внутриклеточные системы передачи сигнала”:
- Строение и функции рецепторов клетки
- Рецепторы как катализаторы и амплификаторы
- Механизм изменения конформации рецептора лигандом
- Механизм дивергенции и конвергенции внутриклеточных сигналов
- Внутриклеточные сигналы как биохимические логические цепи
- Пути передачи сигнала каркасных структур клетки
- Модульные домены в передаче сигнала клетки
- Механизмы адаптации путей передачи сигнала клетки
- Формы сигнальных белков клетки
- Механизмы контроля реакций активации и инактивации сигнальными белками
Источник
Рецепторная функция — это важнейшая способность клетки адекватно реагировать на сигналы внешней и внутренней среды, позволяющая приспосабливаться к меняющимся условиям существования.
Сигналы — это различные вещества или виды энергии, передающие в клетку определенную информацию. Сигналы могут быть:
— химическими — гормоны, медиаторы, факторы роста, цитокины и др.; пахучие вещества или отличающиеся вкусом;
— физическими — свет, звук, температура, давление, электрические потенциалы;
— физико-химическими — осмотическое давление, напряжение О2 или СО2;
— сложными.
Клеточные рецепторы — это генетически детерминированные макромолекулы, локализованные в различных областях клетки и специализированные на восприятии биологически значимых специфических сигналов химической и физической природы. По своей структуре рецептор состоит из 3 доменов:
1) внемембранного — обеспечивает связывание с сигнальным веществом — лигандом;
2) трансмембранного — переносит сигнал, способен к трансформации;
3) цитоплазматического — обеспечивает внутриклеточные процессы — реакцию на сигнал.
Клеточные рецепторы делят на 2 группы:
— рецепторы плазматической мембраны;
— внутриклеточные рецепторы – цитоплазматические и ядерные.
Рецепторы плазматической мембранырасположены на поверхности плазмолеммы и способны высокоспецифически связываться с лигандами. По химической природе это преимущественно гликопротеины.
Рецепторы выполняют функции:
1) регулируют проницаемость плазмолеммы, изменяя конформацию белков и ионных каналов;
2) регулируют поступление некоторых молекул в клетку;
3) действуют как датчики, превращая внеклеточные сигналы во внутриклеточные;
4) связывают молекулы внеклеточного матрикса с цитоскелетом; эти рецепторы называются интегринами, они обеспечивают формирование контактов между клетками и клеткой и межклеточным веществом.
Рецепторы плазматической мембраны можно разделить на 5 семейств:
— рецепторы, связанные с каналами, взаимодействуют с лигандом — нейромедиатором, который временно открывает или закрывает воротный механизм, в результате чего начинается или блокируется транспорт ионов через канал. Каналообразующие рецепторы состоят из ассоциированных белковых субъединиц, специфически пропускающих ионы. С этими рецепторами взаимодействуют глютаминовая кислота, γ-аминомасляная кислота, глицин, циклические мононуклеотиды (цАМФ, цГМФ);
— каталитические рецепторы включают внеклеточную часть (собственно рецептор, который воспринимает сигнал) и цитоплазматическую часть, которая работает как протеинкиназа. Информация сигнальной молекулы приводит к началу каскада биохимических изменений в клетке, что приводит к определенному физиологическому ответу. На такие рецепторы воздействует инсулин, эпидермальный и тромбоцитарный фактор роста, фактор роста нервов.
— рецепторы, связанные с G-белками — это трансмембранные белки, связанные с ионным каналом или ферментом. Это целый комплекс молекул, который включает:
1) сам рецептор, взаимодействующий с сигнальной молекулой (первый посредник) — это интегральный белок, который 7 раз прошивает плазмолемму, внутриклеточные петли этих рецепторов содержат центры связывания G-белка (например, β-адренорецептор);
2) G-белок (гуанозин трифосфат-связывающего регуляторный белок, состоящий из нескольких компонентов), который передает сигнал на связанный с мембраной фермент (аденилатциклазу) или ионный канал, после чего активируется;
3) второй внутриклеточный посредник — чаще циклический АМФ или ГМФ (цАМФ, гАМФ) или Са2+.
Через такие рецепторы реализуются эффекты 80 % нейромедиаторов, пептидных гормонов;
— иммуноглобулиновые рецепторы — это рецепторы-иммуноглобулины на поверхности макрофагов и иммунокомпетентных клеток, обеспечивающие распознавание всего чужеродного и иммунный ответ организма.
— интегрины — клеточные адгезионные молекулы — трансмембранные белки, которые служат рецепторами для внеклеточных фибриллярных макромолекул — фибронектина и ламинина. Фибронектин связывается с клетками и молекулами внеклеточного матрикса (коллагеном, гепарином, фибрином). Фибронектин как адгезионный мостик между клеткой и межклеточным веществом. Внутриклеточная часть интегрина соединяется через другие белки (винкулин, талин, α-актинин) с цитоскелетом.
Таким образом, рецепторы плазмолеммы воспринимают различные сигналы, которые при необходимости изменяют метаболизм в клетке, инициируют и регулируют сокращения, секрецию клетки, модулируют электрический потенциал на поверхности мембраны.
Внутриклеточные рецепторы. Внутриклеточные рецепторы являются белками, регулирующими генную активность клетки. Они располагаются:
— в цитоплазме и в мембране органелл. Цитоплазматические рецепторы обнаружены для стероидных гормонов, например, для глюко- и минералокортикоидов, андрогенов и прогестерона. Митохондрии имеют рецепторы к тиреоидным гормонам;
— в ядре — ядерные рецепторы для тиреоидных гормонов, рецепторов для эстрогенов, витамина Д, ретиноевой кислоты.
Рецепторы для стероидных гормонов имеют 3 домена (части):
1) гормон-связывающий — для взаимодействия с лигандом;
2) ДНК-связывающий;
3) домен, активирующий транскрипцию.
Сигнальные молекулы для таких рецепторов гидрофобные и свободно диффундируют через плазмолемму, затем связываются с внутриклеточными белками-рецепторами. После этого изменяется конформация белка, происходит его активация, повышается сродство к ДНК. Такие гормон-рецепторные комплексы связываются со специфическими генами в ядре, и, регулируя их экспрессию, обеспечивают биосинтез ряда ферментов, изменяющих функциональное состояние клетки.
ТЕМА 5
МЕЖКЛЕТОЧНЫЕ СОЕДИНЕНИЯ, ТИПЫ И СТРУКТУРНО-
ФУНКЦИОНАЛЬНАЯ КЛАССИФИКАЦИЯ
Межклеточные соединения — это специальные структуры, которые вместе с плазмолеммой обеспечивают взаимодействие между клетками. Межклеточные контакты обеспечиваются гликокаликсом и связанными с ним белками. Межклеточные соединения можно подразделить на 2 основных вида:
1. Механические соединения — обеспечивают механическую связь клеток друг с другом. К ним относят простые и сложные соединения: плотные соединения (плотный контакт), десмосомы, интердигитации.
2. Коммуникационные соединения — обеспечивают химическую связь между клетками. К ним относят щелевые соединения.
Механические соединения
I. Простое межклеточное соединение — сближение плазмолемм соседних клеток на расстояние 15–20 нм. При этом гликопротеиды соседних клеток специфичны и «узнают» друг друга, то есть являются рецепторами (кадгерины, интегрины). Обязательным условием соединения является наличие ионов Са2+. Например, Е-кадгерины обеспечивают соединение эпителиальных клеток по всей контактирующей поверхности (рисунок 3).
Рисунок 3 — Простое межклеточное соединение (схема):
Не нашли то, что искали? Воспользуйтесь поиском гугл на сайте:
Источник
Гистамин – это органическое, т.е. происходящее из живых организмов, соединение, имеющее в своей структуре аминные группы, т.е. биогенный амин. В организме гистамин выполняет множество важных функций, о чем дальше. Избыток гистамина приводит к различным патологическим реакциям. Откуда берется избыточный гистамин и как с ним бороться?
Источники гистамина
- Гистамин синтезируется в организме из аминокислоты гистидин: Такой гистамин называется эндогенный.
- Гистамин может попадать в организм с продуктами питания. В этом случае он называется экзогенный
- Гистамин синтезируется собственной микрофлорой кишечника, и может всасываться в кровь из пищеварительного тракта. При дисбактериозе бактерии могут вырабатывать излишне большое количество гистамина, который вызывает псевдоаллергические реакции.
Установлено, что эндогенный гистамин значительно активнее экзогенного.
Синтез гистамина
В организме под воздействием гистидиндекарбоксилазы при участии витамина В-6 (пиридоксальфосфата) от гистидина отщепляется карбоксильный хвост, так аминокислота превращается в амин.

Синтез происходит:
- В желудочно-кишечном тракте в клетках железистого эпителия, где в гистамин превращается поступающий с пищей гистидин.
- В тучных клетках (лаброцитах) соединительной ткани, а также других органах. Тучных клеток особенно много в местах потенциального повреждения: слизистые дыхательных путей (нос, трахея, бронхи), эпителий, выстилающий кровеносные сосуды. В печени и селезенке синтез гистамина ускорен.
- В клетках белой крови – базофилах и эозинофилах
Произведенный гистамин либо запасается в гранулах тучных клеток или клетках белой крови, либо быстро разрушается ферментами. При нарушении баланса, когда гистамин не успевает разрушиться, свободный гистамин ведет себя, как бандит, учиняя погромы в организме, называемые псевдоаллергическими реакциями.
Механизм действия гистамина
Гистамин оказывает действие, связываясь с особыми гистаминовыми рецепторами, которые обозначаются H1, H2, H3, H4. Аминная голова гистамина взаимодействует с аспарагиновой кислотой, находящейся внутри клеточной мембраны рецептора, и запускает каскад внутриклеточных реакций, которые проявляются в определенных биологических эффектах.
Гистаминовые рецепторы

- Н1 рецепторы находятся на поверхности мембран нервных клеток, клеток гладкой мускулатуры дыхательных путей и сосудов, эпителиальных и эндотелиальных клеток (клеток кожи и выстилки кровеносных сосудов), клеток белой крови, ответственных за обезвреживание чужеродных агентов
Их активация гистамином вызывает внешние проявления аллергии и бронхиальной астмы: спазм бронхов с затруднением дыхания, спазм гладкой мускулатуры кишечника с болью и профузным поносом, повышается проницаемость сосудов, в результате чего возникают отеки. Повышается выработка медиаторов воспаления – простагландинов, которые повреждают кожу, что ведет к кожным высыпаниям (крапивнице) с покраснением, зудом, отторжением поверхностного слоя кожи.
Рецепторы, находящиеся в нервных клетках, ответственны за общую активацию клеток головного мозга, гистамин включает режим бодрствования.
Препараты, блокирующие действие гистамина на Н1 рецепторы, используются в медицине для торможения аллергических реакций. Это димедрол, диазолин, супрастин. Так как они блокируют рецепторы, находящиеся в головном мозгу наряду с другими Н1 рецепторами, побочным эффектом этих средств является чувство сонливости.
- Н2 рецепторы содержатся в мембранах париентальных клеток желудка – тех клеток, которые вырабатывают соляную кислоту. Активация этих рецепторов приводит к повышению кислотности желудочного сока. Данные рецепторы задействованы в процессах переваривания пищи.
Существуют фармакологические препараты, селективно блокирующие Н2 гистаминовые рецепторы. Это циметидин, фамотидин, роксатидин и др. Их используют в лечении язвенной болезни желудка, поскольку они подавляют выработку соляной кислоты.
Кроме влияния на секрецию желез желудка, Н2 рецепторы запускают выделение секрета в дыхательных путях, что провоцирует такие симптомы аллергии, как насморк и выделение мокроты в бронхах при бронхиальной астме.
Кроте того стимуляция Н2 рецепторов оказывает влияние на реакции иммунитета:
Угнетаются IgE – иммунные белки, подбирающие чужеродный белок на слизистых, тормозит миграцию эозинофилов (иммунных клеток белой крови, ответственных за аллергические реакции) к месту воспаления, усиливает угнетающее действие Т-лимфоцитов.
- Н3 рецепторы находятся в нервных клетках, где они принимают участие в проведении нервного импульса, а также запускают освобождение других нейромедиаторов: норадреналина, допамина, серотонина, ацетилхолина. Некоторые антигистаминные препараты, такие как димедрол, наряду с Н1 рецепторами, действуют на Н3 рецепторы, что проявляется в общем торможении центральной нервной системы, которая выражается в сонливости, торможении реакций на внешние раздражители. Поэтому неселективные антигистаминные препараты следует принимать с осторожностью лицам, чья деятельность требует быстроты реакций, например, водителям транспортных средств. В настоящее время разработаны препараты селективного действия, которые не оказывают влияния на работу Н3 рецепторов, это астемизол, лоратадин и др.
- Н4 рецепторы находятся в клетках белой крови – эозинофилах и базофилах. Их активация запускает реакции иммунного ответа.
Биологическая роль гистамина
Гистамин имеет отношение к 23 физиологическим функциям, ибо это высокоактивное химическое вещество, которое легко вступает в реакции взаимодействия.
Основными функциями гистамина являются:
- Регуляция местного кровоснабжения
- Гистамин – медиатор воспаления.
- Регуляция кислотности желудочного сока
- Нервная регуляция
- Другие функции

Регуляция местного кровоснабжения
Гистамин регулирует местное кровоснабжение органов и тканей. При усиленной работе, например, мышцы, возникает состояние нехватки кислорода. В ответ на местную гипоксию ткани высвобождается гистамин, который заставляет капилляры расширяться, приток крови увеличивается, а с ним увеличивается и приток кислорода.
Гистамин и аллергия
Гистамин является основным медиатором воспаления. С этой функцией связано его участие в аллергических реакциях
Он содержится в связанном виде в гранулах тучных клеток соединительной ткани и базофилов и эозинофилов – клеток белой крови. Аллергическая реакция – это реакция иммунного ответа на вторжение чужеродного белка, называемого антигеном. Если этот белок уже поступал в организм, клетки иммунологической памяти сохранили информацию о нем и передали на особые белки – иммуноглобулины Е (IgE), которые называют антитела. Антитела обладают свойством специфичности: они узнают и реагируют лишь на свои антигены.
При повторном поступлении в организм белка – антигена, их узнают антитела-иммуноглобулины, которых прежде были сенсибилизированы этим белком. Иммуноглобулины – антитела связываются с белком-антигеном, образуя иммунологический комплекс, и весь этот комплекс прикрепляется к мембранам тучных клеток иили базофилов. Тучные клетки иили базофилы реагируют на это путем высвобождения гистамина из гранул в межклеточную среду. Вместе с гистамином из клетки выходят другие медиаторы воспаления: лейкотриены и простагландины. Все вместе они дают картину аллергического воспаления, которое проявляется по-разному, в зависимости от первичной сенсибилизации.

- Со стороны кожи: зуд, покраснение, отечность (Н1 рецепторы)
- Дыхательные пути: сокращение гладкой мускулатуры (Н1 и Н2 рецепторы), отек слизистой (Н1 рецепторы), повышенная продукция слизи (Н1 и Н2 рецепторы), уменьшение просвета кровеносных сосудов в легких (Н2 рецепторы). Это проявляется в чувстве удушья, нехватки кислорода, кашле, насморке.
- Желудочно-кишечный тракт: сокращение гладкой мускулатуры кишечника (Н2 рецепторы), что проявляется в спастических болях, поносе.
- Сердечно-сосудистая система: падение артериального давления (Н1 рецепторы), нарушение сердечного ритма (Н2 рецепторы).
Выход гистамина из тучных клеток может осуществляться экзоцитарным способом без повреждения самой клетки или происходит разрыв мембраны клетки, что приводит к одномоментному поступлению в кровь большого количества как гистамина, так и других медиаторов воспаления. В результате возникает такая грозная реакция, как анафилактический шок с падением давления ниже критического, судорогами, нарушением работы сердца. Состояние опасно для жизни и даже неотложная врачебная помощь спасает не всегда.
В повышенных концентрациях гистамин выделяется при всех воспалительных реакциях, как связных с иммунитетом, так и неимунных.
Регуляция кислотности желудочного сока
Энтерохромафинные клетки желудка высвобождают гистамин, который через Н2 рецепторы стимулирует обкладочные (париентальные) клетки. Обкладочные клетки начинают поглощать воду и углекислый газ из крови, которые посредством фермента карбоангидразы превращаются в угольную кислоту. Внутри обкладочных клеток угольная кислота распадается на ионы водорода и бикарбонат-ионы. Бикарбонат-ионы отправляются обратно в кровоток, а ионы водорода поступают в просвет желудка через К+ Н+ насос, понижая рН в кислую сторону. Транспорт ионов водорода идет с затратой энергии, высвобождающейся из АТФ. Когда рН желудочного сока становится кислой, высвобождение гистамина прекращается.
Регуляция деятельности нервной системы
В центральной нервной системе гистамин высвобождается в синапсы – места соединения нервных клеток между собой. Гистаминовые нейроны обнаружены в задней доле гипоталамуса в туберомаммилярном ядре. Отростки данных клеток расходятся по всему головному мозгу, через медиальный пучок переднего мозга они идут в Кору больших полушарий. Основной функций гистаминовых нейронов является поддерживание головного мозга в режиме бодрствования, в периоды расслабленияусталости их активность снижается, а в период быстрой фазы сна они неактивны.
Гистамин обладает защитным действием на клетки центральной нервной системы, он снижает предрасположенность к судорогам, защищает от ишемических повреждений и последствий стресса.
Гистамин контролирует механизмы памяти, способствуя забыванию информации.
Репродуктивная функция
Гистамин связан с регуляцией полового влечения. Инъекция гистамина в пещеристое тело мужчин с психогенной импотенцией восстанавливало эрекцию у 74% из них. Выявлено, что антагонисты Н2 рецепторов, которые обычно принимают при лечении язвенной болезни в целью снижения кислотности желудочного сока, вызывают потерю либидо и эректильную дисфункцию.
Разрушение гистамина
Выделившийся в межклеточное пространство гистамин после соединения с рецепторами частично разрушается, но по большей части поступает обратно в тучные клетки, накапливаясь в гранулах, откуда опять может высвобождаться при действии активирующих факторов.
Разрушение гистамина происходит под действием двух основных ферментов: метилтрансферазы и диаминооксидазы (гистаминазы).

Под воздействием метилтрансферазы в присутствии S-аденозилметионина (SAM) гистамин превращается в метилгистамин.
Эта реакция в основном происходит в центральной нервной системе, слизистой оболочке кишечника, печени, тучных клетках (мастоцитах, лаброцитах). Образовавшийся метилгистамин может накапливаться в тучных клетках и при выходе из них, взаимодействовать с Н1 гистаминовыми рецепторами, вызывая все те же эффекты.
Гистаминаза превращает гистамин в имидазолуксусную кислоту. Это основная реакция инактивации гистамина, которая происходит в тканях кишечника, печени, почках, в коже, клетках вилочковой железы (тимуса), эозинофилах и нейтрофилах.
Гистамин может связываться с некоторыми белковыми фракциями крови, что сдерживает избыточное взаимодействие свободного гистамина со специфическими рецепторами.
Небольшое количество гистамина выделяется в неизмененном виде с мочой.
Псевдоаллергические реакции
Псевдоаллергические реакции по внешним проявлениям ничем не отличаются от истинной аллергии, но они не имеют иммунологической природы, т.е. неспецифичны. При псевдоаллергических реакциях нет первичного вещества – антигена, с которым бы связывался белок-антитело в иммунологический комплекс. Аллергические пробы при псевдоаллергических реакциях ничего не выявят, ибо причина псевдоаллергической реакции не в проникновении в организм чужеродного вещества, а в интолерантности самого организма к гистамину. Интолерантность возникает при нарушении равновесия между гистамином, поступившем в организм с пищей и высвободившимся из клеток, и дезактивацией его ферментами. Псевдоаллергические реакции по своим проявлениям не отличаются от аллергических. Это могут быть поражения кожи (крапивница), спазм дыхательных путей, заложенность носа, диарея, гипотония (снижение артериального давления), аритмия.
Часто псевдоаллергические реакции возникают при употреблении продуктов с высокой концентрацией гистамина. О продуктах, нашпигованных гистамином, читайте здесь: https://zaryad-zhizni.ru/v-kakih-produktah-soderzhitsya-gistamin/.
Источник
