Перечислите области применения важнейших альдегидов и кетонов на каких свойствах

Свойства альдегидов 
Метаналь
— газ; соединения с количеством атомов углерода в молекуле менее 12 —
жидкие, причем густота и вязкость жидкости растет с ростом числа атомов
углерода, а растворимость в воде падает. Более длинные альдегиды —
твердые, в воде нерастворимые. Вещества с количеством атомов углерода
меньше 6 имеют резкий и неприятный запах. Все остальные альдегиды,
напротив, пахнут приятно.
Альдегиды химически активнее кетонов.
Они окисляются до карбоновых кислот, образуют сложные эфиры. Являются
сильными восстановителями, легко восстанавливаются до одноатомных
спиртов. Вступают в реакции со спиртами. В результате реакции
поликонденсации с фенолами получаются фенолформальдегидные смолы.
Взаимодействуют с гидросульфитами, реактивами Гриньяра, водно-спиртовыми
растворами щелочей. Вещества ядовиты; способны накапливаться в
организме человека.
Свойства кетонов
Агрегатное
состояние кетонов изменяется аналогично альдегидам: сначала это
жидкости, а вещества с длинными молекулами — твердые, легкоплавкие.
Жидкости хорошо растворяются в воде. Пахнут неприятно. Особенностью
жидких кетонов является высокая летучесть, большая, чем у спиртов и
карбоновых кислот.
В результате реакций восстановления и
гидрирования кетоны превращаются во вторичные спирты. Окисляются до
карбоновых кислот, но с трудом. Взаимодействуют с аммиаком,
гидросульфитами, ортокремниевой H4SiO4 и синильной HCN кислотами,
гидразином, гидроксиламином и др.
Кетоны тоже ядовиты. Обладают
раздражающим действием, легко проникают через неповрежденную кожу. При
этом кетоны участвуют в метаболизме живых организмов, в реакциях
тканевого дыхания.
Различают альдегиды и кетоны с помощью
качественных реакций, которые, как правило, определяют альдегиды. Одна
из таких реакций — «серебряного зеркала». В результате взаимодействия
альдегида и аммиачного раствора окиси серебра на стенках сосуда
образуется блестящий слой чистого серебра.
Применение
•
Ароматические альдегиды и кетоны применяются в парфюмерии, пищепроме,
химпроме. Они входят в состав пищевых и парфюмерных ароматизаторов,
чистящих средств, различного парфюма и косметических товаров,
освежителей воздуха и пр.
• Альдегиды и кетоны применяются в
фармацевтике, медицине, пищепроме, косметической индустрии; для
проведения органических синтезов, производства спиртов, карбоновых
кислот и их производных; получения искусственных волокон, тканей,
полимеров, смол, лаков и красок, растворителей, душистых веществ.
•
Формальдегид используется для консервации анатомических материалов и
объектов; в фармацевтике; в производстве пластиков; для дубления кож.
•
Уксусный альдегид востребован в химпроме для получения уксусной кислоты
и ее производных, ацетата целлюлозы, синтетического каучука, этанола,
ацетатных волокон и тканей; лекарственных препаратов.
• Цитраль —
альдегид с выраженным запахом лимона, входит в состав эфирных масел
эвкалипта, лимона, сорго, кебаба. Используется в медицине для снижения
давления у детей и взрослых; входит в состав лекарств, улучшающих
зрение, антисептиков и антибактериальных препаратов, как сырье для
производства витамина А. Так же применяется в пищепроме как
ароматизатор; входит в состав различных отдушек. 
•
Ацетон — простейший кетон, востребован в лабораториях и различных
областях промышленности. Используется в органических синтезах; как
растворитель; для получения полиуретанов, поликарбонатов, эпоксидных
смол; для экстракции; в фармацевтике для производства лекарств и пр.
• Циклогексанон — один из важнейших кетонов. Применяется как растворитель, для получения синтетических волокон, чернил и красок.
• Ацетилацетон — популярный в аналитике реагент, востребован для разделения металлов, растворитель для экстракций.
Источник
Из карбонильных соединений наибольшее применение находят формальдегид, ацетальдегид и ацетон.
Формальдегид (метаналь, муравьиный альдегид) Н-СНО широко используется для получения фенолформальдегидных и мочевино-формальдегидных (карбамидных) смол, пластмасс, для синтеза лекарственных средств (уротропин), продуктов органического синтеза, как дезинфицирующее средство и консервант биологических и анатомических препаратов, в кожевенном производстве – для обработки кож.
40% водный раствор формальдегида называют формалином. Его использование основано на свойстве свертывать белок. Действуя на белок, формалин делает его плотным, нерастворимым в воде и, главное, предохраняет от гниения. Поэтому его применяют для консервирования анатомических препаратов. Формалин прекрасно сохраняет костный материал, необходимый для восстановления живых тканей, проведения пластических операций.
В кожевном производстве дубящее действие формалина также основано на способности свертывать белок, в результате чего кожа твердеет и не подвергается гниению.
Вследствие высокой токсичности, обусловленной способностью формальдегида свертывать белки, он может использоваться лишь в качестве средства для дезинфекции помещений, хирургических инструментов.
Формалин применяется в сельском хозяйстве для дезинфекции зерно- и овощехранилищ, парников и теплиц, для протравливания семян с целью уничтожения личинок вредителей.
Большое количество метаналя используют для получения фенолформальдегидной смолы при его взаимодействии с фенолом. Эта смола необходима для производства различных пластмасс. Пластмассы, изготовленные из фенолформальдегидной смолы в сочетании с рзличными наполнителями, называют фенопластами.
На основе фенолформальдегидных смол готовят клеи, лаки, эмали, краски, политуры. Из полиформальдегида изготавливают литые и пленочные изделия.
А знаете ли вы?
Древесно-стружечные плиты (ДСП) изготавливают из древесных опилок и фенолформальдегидных смол. Мебель, изготовленная из таких плит, выделяет формальдегид и поэтому представляет опасность для здоровья. Помещение, где находится такая мебель, следует часто проветривать.
При взаимодействии формальдегида с карбамидом СО(NH2)2 получают карбамидную смолу, а из нее – аминопласты. Из этих пластмасс изготавливают микропористые материалы для нужд электротехники (выключатели, розетки и др.).
Интересно знать!
Немецкий химик А. Байер в 1872 г. из фенола и формальдегида получил смолообразный продукт. Бельгийский ученый Л. Бакеланд разработал способ получения этого вещества в промышленности. Так, с 1912 г. производится фенолформальедгидная смола, названная бакелитом.
А.М. Бутлеров в 1860 г. впервые синтезировал из формальдегида и аммиака органическое вещество гексаметилентетрамин, или утротропин, которое используется в медицине.
Взаимодействием формальдегида с аммиаком получают уротропин – лекарственный препарат (используют в качестве мочегонного средства, при лечении почечных заболеваний).
 Иногда спрессованный в виде брикетов уротропин применяют в качестве горючего (сухой спирт).
Иногда спрессованный в виде брикетов уротропин применяют в качестве горючего (сухой спирт).
Уротропин применяют также в качестве ингибитора кислотной коррозии металлов и в производстве взрывчатых веществ.
Нитрование уротропина приводит к образованию сильного взрывчатого вещества «гексоген»:

Синтезы на основе формальдегида
Ацетальдегид (уксусный альдегид, этаналь) СН3-СНО находит широкое применение в промышленном органическом синтезе. Он служит сырьем для получения уксусной кислоты, уксусного ангидрида, этилацетата, хлораля, этилового и бутилового спиртов, синтетических смол и ряда других соединений.

 Ацетон (пропанон-2, диметилкетон) СН3СОСН3 применяется в лакокрасочной промышленности, в производстве ацетатного шелка, пироксилина (бездымного пороха), киноплёнки. Благодаря сравнительно малой токсичности используется в пищевой и фармацевтической промышленности. Он служит исходным веществом при производстве небьющегося органического стекла.
Ацетон (пропанон-2, диметилкетон) СН3СОСН3 применяется в лакокрасочной промышленности, в производстве ацетатного шелка, пироксилина (бездымного пороха), киноплёнки. Благодаря сравнительно малой токсичности используется в пищевой и фармацевтической промышленности. Он служит исходным веществом при производстве небьющегося органического стекла.
Высшие непредельные и ароматические альдегиды и кетоны входят в состав эфирных масел и содержатся во многих цветах, фруктах, плодах, душистых и пряных растениях. Из-за приятного запаха они широко применяются в парфюмерии.
Ароматический кетон бензофенон (дифенилкетон) (С6Н5)2С=О с запахом герани, используется в парфюмерных композициях и для ароматизации мыла. Бензофенон и его производные способны поглощать УФ-лучи, что определило их применение в кремах и лосьонах от загара. Кроме того, некоторые производные бензофенона обладают противомикробной активностью и применяются в качестве консервантов.
Алифатический пеларгоновый альдегид (нониловый альдегид) СН3(СН2)7СНО содержится в эфирных маслах цитрусовых растений, обладает запахом апельсина, его используют как пищевой ароматизатор.
Ванилин C8H8O3 как душистое вещество используют в пищевой и парфюмерной промышленности. Но в последнее время чаще используется синтетический ванилин — широко известная ароматизирующая добавка в кондитерские изделия. Ванилин является исходным веществом в синтезе противотуберкулезного препарата «Фтивазида».
Коричный альдегид С6Н5СН=СНСНО применяется в кулинарии в виде палочек или порошка.
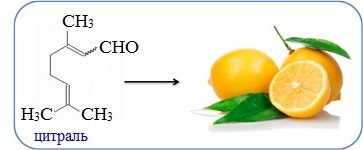
Цитраль C10H16O имеет интенсивный лимонный запах и является важнейшим компонентом композиций и отдушек средств бытовой химии, косметических и парфюмерных веществ.
Интересно знать!
Многие насекомые при нападении врагов используют средства химической защиты – выделяют соединения, которые обладают сильным, летучим запахом. Эти соединения оказывают раздражающее действие, а капли попавшие на покровы хищника могут вызвать раздражение и зуд.
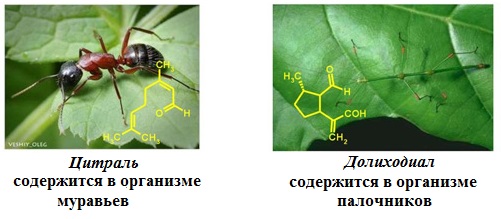
Гидрооксицитронеллаль (7-гидрокси-3,7-диметил-октаналъ) (СН3)2С(ОН)(СН2)3СН(СН)зСН2СНО – густая бесцветная жидкость со свежим запахом липы, с нотой ландыша. Его используют для приготовления многих композиций и отдушек.

Бензальдегид С6Н5СН=О обладает запахом горького миндаля. Бензальдегид содержится в эфирных маслах, а в виде гликозида амигдалина – в семенах горького миндаля, косточек вишни, абрикоса, персика.
Он применяется в качестве компонента парфюмерных композиций и пищевых эссенций как сырье для синтеза душистых веществ – коричного альдегида, коричной кислоты, бензилбензоата, трифенилметановых красителей.
Акролеин (пропеналь) СН2=СН-СНО является исходным сырьем для синтеза многих органических соединений. Его применяют для получения пластмасс, отличающихся большой твердостью, акрилонитрила, глицерина, аллилового спирта, акриловой кислоты, лекарственных средств.
Кротоновый альдегид CH3CH=CHCHO – сильный лакриматор, используется для получения бутанола, сорбиновой и масляной кислот. Содержится в соевом масле.
Фенилэтаналь (фенилуксусный альдегид) C6H5CH2CHO имеет запах гиацинта. Добавление незначительного количества его к парфюмерным композициям придает им приятный цветочный оттенок.
 Обепин (анисовый альдегид) C8H8O2 как душистое вещество с запахом, напоминающим запах цветов боярышника, используют при изготовлении композиций для духов и одеколонов, отдушек для косметических средств. В природе он найден в маслах аниса, фенхеля, акации, укропа, боярышника.
Обепин (анисовый альдегид) C8H8O2 как душистое вещество с запахом, напоминающим запах цветов боярышника, используют при изготовлении композиций для духов и одеколонов, отдушек для косметических средств. В природе он найден в маслах аниса, фенхеля, акации, укропа, боярышника.
Ацетофенон (метилфенилкетон) C6H5COCH3 используют как душистое вещество в парфюмерии, а также в синтезе некоторых лекарственных препаратов.
Диацетил (2,3-бутандион, диметилглиоксаль) С4H6O2 – имеет запах свежих сливок, используется как пищевая добавка для придания продуктам запаха масла или сыра.
Циклогексанон С6Н10О применяется в синтезе капролактама – мономера в производстве поликапроамида (капрон, дедерон, нейлон-6 и др.
Альдегиды и кетоны
Источник
Добрый день, дорогие подписчики и гости моего канала. Сегодня вас ждет еще одна статья из цикла «школьный курс химии». На написание этой статьи, меня вдохновили пособия для подготовки учеников старшей школы к ЕГЭ, в которых основные классы органических соединений описаны очень слабо и приведены далеко не все реакции встречающиеся на экзамене. В сегодняшней статье, я постараюсь, как можно более подробно разобрать два класса органических веществ – Альдегиды и Кетоны. И начнем мы как всегда с определений.
Альдегиды – это органические вещества, которые содержат карбонильную группу (=С=O), соединенную с атомом водорода и углеводородным радикалом.
Таким образом, общая формула альдегидов:
Кетоны — это органические вещества, в молекулах которых карбонильная группа (=С=O) связана с двумя углеводородными радикалами.
Общая формула кетонов:
Таким образом, карбонильная группа (=С=O) определяет принадлежность вещества к классу альдегидов или кетонов. Частный случай фунциональной карбонильной группы – это альдегидная группа (-COH) и она уже определяет принадлежность вещества лишь к классу альдегидов.
Гомологический ряд альдегидов следующий:
Гомологический ряд кетонов несколько сложнее, в виду изомерии, однако его можно представить так:
Как вы видете, всем известный растворитель краски ацетон, является простейшим кетоном.
Ацетон – это бесцветная летучая жидкость с характерным запахом. В последнее время он широко применяется в различных сферах производства, таких как:
– Синтез поликарбонатов и полиуретанов.
– Производство эпоксидных смол.
– Производство лаков.
– Производство взрывчатых веществ.
– Производство лекарственных препаратов.
– Используется при экстракции многих растительных веществ.
Так же, более подробно стоит поговорить и о некоторых простейших представителях класса альдегидов.
Формальдегид (от лат. formica — «муравей») — это бесцветный газ с резким запахом, хорошо растворимый в воде и других органических растворителях, очень ядовит. Его применяют для:
– Производства фенолформальдегидных пластмасс.
– Для производства многих лекарственных препаратов, например уротропина. Кстати, спресованый в виде брикетов уротропин применяют в качестве горючего (сухой спирт).
– Раствор формальдегида в воде называют формалином. Его используют для хранения биопрепаратов, протравливания семян перед посевом, дубления кож.
Ацетальдегид (Уксусный альдегид) – это летучая жидкость, хорошо растворимая в воде, с характерным запахом. Основные сферы применения уксусного альдегида:
– Производство уксусной кислоты.
– Получение ацетатного волокна.
– Получение альдегидных полимеров (различных пластмасс).
Получение альдегидов и кетонов:
Существует большое колличество способов получения альдегидов и кетонов перечислим некоторые из них.
1. Окисление спиртов на медном катализаторе:
C2H5OH + CuO → CH3CHO + Cu + H2O
Окисление вторичных спиртов по этому же методу, приводит к образованию кетонов:
2. Реакция Кучерова.
При гидратации ацетилена получается уксусный альдегид:
При гидратации любых других алкинов получаются кетоны:
3. При окисление вторичных спиртов перманганатом калия получаем кетоны:
5CH3CH(OH)CH3 + 2KMnO4 + 3H2SO4 = CH3-C(O)-CH3 + K2SO4 + 2MnSO4 + 8H2O
4. В промышленности формальдегид получают путем окисления метана при 500 градусах Цельсия, с участием различных катализаторов.
CH4 + O2 = H-COH + H2O
Химические свойства Альдегидов и Кетонов:
1. Взаимодействие с водородом (Гидрирование)
Слово Альдегиды, происходит от латинских слов «alcohol dehydrogenatus» – «алкоголь дегидрированый» или «спирт лишенный водорода», а дегидрированый продукт способен вернуть себе водород. Таким образом альдегиды востанавливаются до первичных спиртов, а кетоны до вторичных:
2. Гидратация.
Данная реакция характерна только для формальдегида и ацетальдегида.
Для кетонов данная реакция не характерна.
3. Присоединение синильной кислоты:
Кстати, необходимо знать, что синильная кислота или же цианистоводородная кислота – это бесцветная, очень летучая, легкоподвижная ядовитая жидкость, имеющая характерный запах горького миндаля.
4. Присоединение спиртов:
5. Взаимодействие с гидросульфитом натрия:
Данная реакция является качественной, так как образующаяся в результате нее соль выпадает в виде осадка.
6. Реакция «серебряного зеркала».
Это взаимодействие альдегида с аммиачным раствором оксида серебра или реактивом Толленса.
Данную реакцию можно записать так:
Однако, по факту кислота не может существовать с образовавшимся раствором аммиака, поэтому правильнее будет записать ее таким образом:
Данная реакция является качественной и для других веществ содержащих альдегидную группу, например для муравьинной кислоты, ее эфиров или для глюкозы.
Кетоны в реакцию серебряного зеркала не вступают.
7. Взаимодействие со свежеполученым осадком гидроксида меди II.
Эта реакция так же не характерна для кетонов.
Для альдегидов, эту реакцию можно записать так:
В результате реакции сначала произойдет образование желтого осадка, который затем постепенно начнет приобретать красно – оранжевый оттенок.
8. Взаимодействие с подкисленным раствором перманганата калия.
Надо отметить, что окисление формальдегида идет до углекислого газа:
HCOH + KMnO4 + H2SO4 = K2SO4 + MnSO4 + CO2 + H2O
Во всех остальных случаях образуется карбоновая кислота:
5CH3COH + 2KMnO4 + 3H2SO4 = 5CH3COOH + 2MnSO4 + K2SO4 + 3H2O
9. Реакция Тищенко.
Диспропорционирование альдегида – получение сложного эфира из альдегида – в присутствии алкоголята алюминия (1906 г.)
10. Реакция Фаворского.
Конденсация карбонильных соединений с алкинами с образованием ацетиленовых спиртов:
11. Реакция Бутлерова.
Получение углеводов из формальдегида в присутствие известкового раствора:
12. Галогенирование по альфа-атому углерода:
13. Полимеризация.
Полимериза́ция — это процесс образования высокомолекулярного вещества (полимера) путём многократного присоединения молекул низкомолекулярного вещества (мономера) к активным центрам в растущей молекуле.
Кетоны в эти реакции не вступают, а среди альдегидов имеет смысл лишь полимеризация формальдегида:
14. Поликонденсация.
Поликонденсация — процесс синтеза полимеров из органических соединений, обычно сопровождающийся выделением низкомолекулярных побочных продуктов (чаще всего воды).
Нам, особенно интересна поликонденсация формальдегида с фенолом, приводящая к образованию фенолформальдегидной смолы:
15. Реакция горения.
2 CH3COH + 5 O2 = 4 CO2 + 4 H2O
Вот пятнадцать химических реакций, которые могут встречаться на ЕГЭ по теме альдегидов. А я сейчас держу пособие для подготовки к ЕГЭ, где химических реакций перечислено только пять. К тому же забыли написать способы получения альдегидов. Так что качественно ищите материалы для подготовки к экзаменам.
Сдающим ЕГЭ, так же рекомендую к прочтению:
Карбоновые кислоты.
Фенолы.
То, что нужно знать о Спиртах.
Высоких балов тем, кто сдает ЕГЭ!
Источник
Среди кислородсодержащих органических соединений огромное значение имеют целых два класса веществ, которые всегда изучают вместе за схожесть в строении и проявляемых свойствах. Это альдегиды и кетоны. Именно эти молекулы лежат в основе многих химических синтезов, а их строение достаточно интересное, чтобы стать предметом изучения. Рассмотрим подробнее, что же представляют собой эти классы соединений.

Альдегиды и кетоны: общая характеристика
С точки зрения химии, к классу альдегидов следует относить органические молекулы, содержащие кислород в составе функциональной группы -СОН, называемой карбонильной. Общая формула в этом случае будет выглядеть так: R-COH. По своей природе это могут быть как предельные, так и непредельные соединения. Также среди них встречаются и ароматические представители, наравне с алифатическими. Количество атомов углерода в радикальной цепи варьируется в достаточно широких пределах, от одного (формальдегид или метаналь) до нескольких десятков.
Кетоны также содержат карбонильную группу -СО, однако соединена она не с катионом водорода, а с другим радикалом, отличным или идентичным тому, что входит в цепь. Общая формула выглядит так: R-CO-R,. Очевидно, что альдегиды и кетоны схожи по наличию функциональной группы такого состава.
Кетоны также могут быть предельными и непредельными, да и проявляемые свойства сходны с близкородственным классом. Можно привести несколько примеров, иллюстрирующих состав молекул и отражающих принятые обозначения формул рассматриваемых веществ.
- Альдегиды: метаналь – НСОН, бутаналь – СН3-СН2-СН2-СОН, фенилуксусный – С6Н5-СН2-СОН.
- Кетоны: ацетон или диметилкетон – СН3-СО-СН3, метилэтилкетон – СН3-СО-С2Н5 и другие.
Очевидно, что название данных соединений образуется двумя путями:
- по рациональной номенклатуре согласно входящим в состав радикалам и классового суффикса -аль (для альдегидов) и -он (для кетонов);
- тривиально, исторически сложившееся.
Если привести общую формулу для обоих классов веществ, то станет видно, что они являются изомерами друг другу: CnH2nO. Для них же самих характерны следующие виды изомерии:
- для кетонов – строение углеводородной цепи радикала и положение группы -СО;
- для альдегидов – только расположение атомов в цепи.

Чтобы различать между собой представителей обоих классов, используют качественные реакции, большинство из которых позволяют выявить именно альдегид. Так как химическая активность данных веществ несколько выше, благодаря наличию катиона водорода.
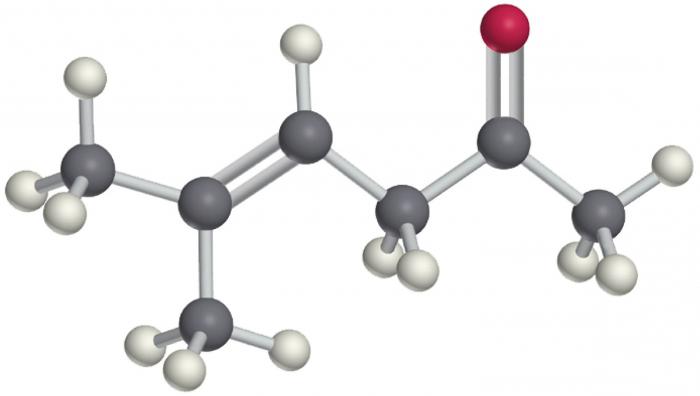
Строение молекулы
Рассмотрим, как же в пространстве выглядят альдегиды и кетоны. Строение их молекул можно отразить несколькими пунктами.
- Атом углерода, непосредственно входящий в функциональную группу, имеет sp2 – гибридизацию, что позволяет части молекулы иметь плоскую пространственную форму.
- При этом полярность связи С=О сильна. Как более электроотрицательный, кислород забирает себе основную часть плотности, концентрируя на себе частично отрицательный заряд.
- В альдегидах связь О-Н является также сильно поляризованной, что делает атом водорода подвижным.
В результате получается, что подобное строение молекул позволяет рассматриваемым соединениям и окисляться, и восстанавливаться. Формула альдегида и кетона с перераспределенной электронной плотностью позволяет предсказать продукты реакций, в которых участвуют данные вещества.
История открытия и изучения
Как и многие органические соединения, выделить и изучить альдегиды и кетоны людям удалось лишь в XIX веке, когда виталистические взгляды полностью рухнули и стало понятно, что эти соединения могут образовываться синтетическим, искусственным путем, без участия живых существ.
Однако еще в 1661 году Р. Бойль сумел получить ацетон (диметилкетон), когда подвергал нагреванию ацетат кальция. Но подробно изучить это вещество и назвать его, определить систематическое положение среди других, он не смог. Лишь в 1852 году Уильямсон сумел довести это дело до конца, тогда и началась история подробного развития и накопления знаний о карбонильных соединениях.

Физические свойства
Рассмотрим, каковы физические свойства альдегидов и кетонов. Начнем с первых.
- Первый представитель метаналь по агрегатному состоянию – газ, следующие одиннадцать – жидкости, свыше 12 атомов углерода входят в состав твердых альдегидов нормального строения.
- Температура кипения: зависит от числа атомов С, чем их больше, тем она выше. При этом чем более разветвлена цепочка, тем ниже опускается значение температуры.
- Для жидких альдегидов показатели вязкости, плотности, преломления зависят также от числа атомов. Чем их больше, тем они выше.
- Газообразный и жидкие альдегиды растворяются в воде очень хорошо, однако твердые практически не могут этого делать.
- Запах представителей очень приятный, часто это ароматы цветов, духов, фруктов. Лишь те альдегиды, в которых количество атомов углерода равно 1-5, являются сильно и неприятно пахнущими жидкостями.
Если обозначать свойства кетонов, то также можно выделить главные.
- Агрегатные состояния: низшие представители – жидкости, более массивные – твердые соединения.
- Запах резкий, неприятный у всех представителей.
- Растворимость в воде хорошая у низших, в органических растворителях отличная у всех.
- Летучие вещества, данный показатель превышает таковой у кислот, спиртов.
- Температура кипения и плавления зависит от строения молекулы, сильно варьируется от количества атомов углерода в цепи.
Это основные свойства рассматриваемых соединений, которые относятся к группе физических.
Химические свойства
Самое важное, это с чем реагируют альдегиды и кетоны, химические свойства данных соединений. Поэтому их мы рассмотрим обязательно. Сначала разберемся с альдегидами.
- Окисление до соответствующих карбоновых кислот. Общий вид уравнения реакции: R-COH + [O] = R-COOH. Ароматические представители еще легче вступают в подобные взаимодействия, также они способны формировать в результате сложные эфиры, имеющие важное промышленное значение. В качестве окислителей используют: кислород, реактив Толленса, гидроксид меди (II) и другие.
- Альдегиды проявляют себя как сильные восстановители, при этом превращаясь в предельные одноатомные спирты.
- Взаимодействие со спиртами с образованием продуктов ацеталей и полуацеталей.
- Особые реакции – поликонденсации. В результате образуются фенолформальдегидные смолы, имеющие значение для химической промышленности.
- Несколько специфических реакций со следующими реактивами:
- водно-спиртовая щелочь;
- реактив Гриньяра;
- гидросульфиты и прочие.
Качественной реакцией на данный класс веществ является реакция “серебряного зеркала”. В результате нее образуется металлическое восстановленное серебро и соответствующая карбоновая кислота. Для нее необходим аммиачный раствор оксида серебра или реактив Толлинса.
Химические свойства кетонов
Спирты, альдегиды, кетоны являются схожими по проявляемым свойствам соединениями, так как все они кислородсодержащие. Однако уже на стадии окисления становится ясно, что спирты – самые активные и легко поддающиеся воздействию соединения. Кетоны же окислить труднее всего.
- Окислительные свойства. В результате образуются вторичные спирты.
- Гидрирование также приводит к упомянутым выше продуктам.
- Кето-енольная таутомерия – особое специфическое свойство кетонов принимать бета-форму.
- Реакции альдольной конденсации с образование бета-кетоспиртов.
- Также кетоны способны взаимодействовать с:
- аммиаком;
- синильной кислотой;
- гидросульфитами;
- гидразином;
- ортокремниевой кислотой.
Очевидно, что реакции таких взаимодействий очень сложны, особенно те, которые являются специфическими. Это все основные особенности, которые проявляют альдегиды и кетоны. Химические свойства лежат в основе многих синтезов важных соединений. Поэтому знать природу молекул и их характер при взаимодействиях крайне необходимо в промышленных процессах.
Реакции присоединения альдегидов и кетонов
Мы уже рассмотрели данные реакции, однако не давали им такого названия. К присоединению можно отнести все взаимодействия, в результате которых активность проявила карбонильная группа. А точнее, подвижный атом водорода. Именно поэтому в данном вопросе преимущество отдается именно альдегидам, вследствие их лучшей реакционноспособности.
С какими веществами возможны реакции альдегидов и кетонов по нуклеофильному замещению? Это:
- Синильная кислота, образуются циангидрины – исходное сырье при синтезе аминокислот.
- Аммиак, амины.
- Спирты.
- Воду.
- Гидросульфат натрия.
- Реактив Гриньяра.
- Тиолы и другие.
Эти реакции имеют важное промышленное значение, поскольку продукты используются в разных областях жизнедеятельности людей.

Способы получения
Существует несколько основных методов, которыми синтезируют альдегиды и кетоны. Получение в лаборатории и промышленности можно выразить в следующих способах.
- Самым распространенным методом, в том числе и в лабораториях, является окисление соответствующих спиртов: первичных до альдегидов, вторичных до представителей кетонов. В качестве окислительного агента могут выступать: хроматы, ионы меди, перманганат калия. Общий вид реакции: R-OH + Cu (KMnO4) = R-COH.
- В промышленности часто используют способ, основанный на окислении алкенов – оксосинтез. Основной агент синтез-газ, смесь СО2 + Н2. Результатом становится альдегид с большим на один углерод числом атомов в цепи. R=R-R + СО2 + Н2 = R-R-R-COH.
- Окисление алкенов озоном – озонолиз. Результат также предполагает альдегид, но кроме этого еще и кетон в смеси. Если продукты мысленно соединить, убрав кислород, станет ясно, какой исходный алкен был взят.
- Реакция Кучерова – гидратация алкинов. Обязательный агент – соли ртути. Один из промышленных способов синтеза альдегидов и кетонов. R≡R-R + Hg2+ + H2O = R-R-COH.
- Гидролиз дигалогенпроизводных углеводородов.
- Восстановление: карбоновых кислот, амидов, нитрилов, хлорангидридов, сложных эфиров. В результате образуется как альдегид, так и кетон.
- Пиролиз смесей карбоновых кислот над катализаторами в виде оксидов металлов. Смесь должна быть парообразной. Суть заключается в отщеплении между молекулами диоксида углерода и воды. В результате образуется альдегид или кетон.
Ароматические альдегиды и кетоны получают иными способами, так как данные соединения имеют ароматический радикал (фенил, например).
- По Фриделю-Крафтсу: в исходных реагентах ароматический углеводород и дигалогензамещенный кетон. Катализатор – ALCL3. В результате образуется ароматический альдегид или кетон. Другое название процесса – ацилирование.
- Окисление толуола действием разных агентов.
- Восстановлением ароматических карбоновых кислот.
Естественно, что в промышленности стараются использовать те методы, в которых исходное сырье как можно более дешевое, а катализаторы менее токсичные. Для синтеза альдегидов – это окисление алкенов кислородом.

Применение в промышленности и значение
Применение альдегидов и кетонов осуществляется в таких отраслях промышленности, как:
- фармацевтика;
- химический синтез;
- медицина;
- парфюмерная область;
- пищевая промышленность;
- лакокрасочное производство;
- синтез пластмасс, тканей и прочее.
Можно обозначить еще не одну область, ведь ежегодно только формальдегида синтезируется приблизительно 6 млн т в год! Его 40% раствор именуется формалином и используется для хранения анатомических объектов. Он же идет на изготовление лекарственных препаратов, антисептиков и полимеров.
Уксусный альдегид, или этаналь, также массово производимый продукт. Количество ежегодного потребления в мире составляет около 4 млн т. Он – основа многих химических синтезов, при которых образуются важные продукты. Например:
- уксусная кислота и ее ангидрид;
- ацетат целлюлозы;
- лекарства;
- бутадиен – основа каучука;
- этиловый спирт;
- ацетатное волокно.
Ароматические альдегиды и кетоны – это составная часть многих ароматизаторов, как пищевых, так и парфюмерных. Большинство из них имеют очень приятные цветочные, цитрусовые, травяные ароматы. Это позволяет изготовлять на их основе:
- освежители воздуха различного рода;
- туалетные и парфюмерные воды;
- различные чистящие и моющие средства.
Некоторые из них являются ароматическими добавками к пище, разрешенными к употреблению. Их природное содержание в эфирных маслах, фруктах и смолах доказывают возможность подобного использования.
Отдельные представители
Такой альдегид, как цитраль, представляет собой жидкость с большой вязкостью и сильным ароматом лимона. В природе содержится как раз в эфирных маслах последнего. Также в составе эвкалипта, сорго, кебаба.
Хорошо известны области его применения:
- педиатрия – понижение внутричерепного давления;
- нормализация артериального давления у взрослых;
- компонент лекарства для органов зрения;
- составная часть многих душистых веществ;
- противовоспалительное средство и антисептик;
- сырье для синтеза ретинола;
- ароматизатор в пищевых целях.
Источник
