При какой температуре железо теряет магнитные свойства при температуре
Еще со времен
Гильберта было известно, что железо и
сталь теряют свои магнитные свойства,
будучи нагреты до светло-красного
каления. Они при этом перестают
намагничиваться и не притягиваются
магнитом, но при охлаждении восстанавливают
свои обычные качества. То же происходит
при несколько более высокой температуре
с кобальтом и при более низкой — с
никкелем. Вообще говоря, переход от
магнитного состояния к немагнитному
происходит очень быстро, как только
температура тела достигает определенного
предела.
152
В
виде примера приведем данные, которые
былиполучены:
Гопкинсоном во время одного опыта с
куском кованого железа. Когда этот
материал был подвергнут действию слабого
магнитного поля (H=0,3
эрстеда), его магнитная проницаемость
непрерывно возрастала с повышением
температуры сначала медленно, затем
все быстрее и быстрее и так далее, до
предельной температуры, которая в
описываемом случае оказалась равной
775° С. При этой температуре магнитная
проницаемость во много раз больше, чем
в случае холодного железа. При дальнейшем
нагревании последовала чрезвычайно
быстрая потеря магнитных свойств: когда
температура поднялась всего только на
11°, т. е. до 786°С, железо сделалось
практически немагнитным. Его магнитная
проницаемость стала равной 1,1, между
тем как при 775°С проницаемость имела
значение около 11000. На рисунке 89)
представлена графически зависимость
от температуры в данном случае, т. е. при
H=0,3
эрстеда.
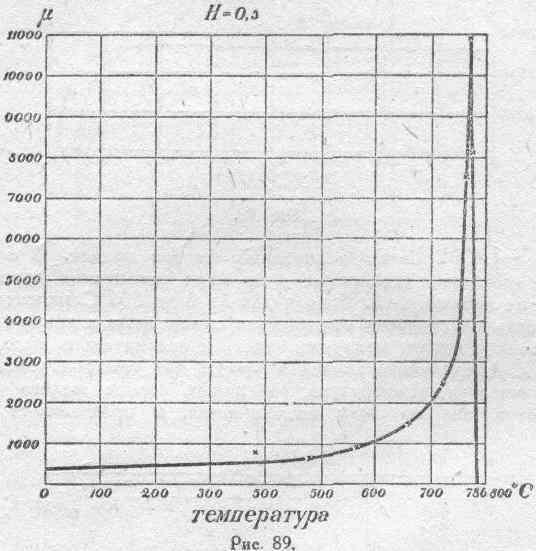
Здесь весьма
отчетливо видно, насколько внезапно
магнитная проницаемость данного образца
железа падает при приближении температуры
его к 786°С. Когда материал был подвергнут
действию сравнительно более сильного
поля, переход от магнитного состояния
к немагнитному совершался более плавно,
но потеря
153
магнитных свойств
столь же полная, и происходит это при
той же температуре, что и раньше. Гопкинсон
назвал ее критической температурой.
На рисунках 90 и 91 представлена зависимость
от температуры
при
H=4
эрстедам,
H=45
эрстедам,
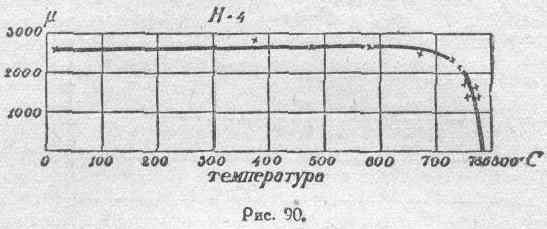

для того же сорта
железа, к которому относится и рисунок
89. В случае H=4
эрстедам, по мере повышения температуры
еще наблюдается некоторый подъем ,
и это
продолжается приблизительно до 650°.
Затем довольно
быстро падает. В случае же Н=45
эрстедам, повышения
по мере повышения температуры совсем
не наблюдается. В пределах от 0 до 500°С
магнитная проницаемость практически
сохраняется неизменною, а при дальнейшем
нагревании начинает медленно падать и
сравнительно медленно же падает до
предельного значения =1,1
при температуре в 786° С. Критическая
температура различных сортов железа и
стали колеблется, как показали
исследования, в пределах от 690° до 870°С.
У кобальта критическая температура
равна приблизительно 1000°, у никкеля
—около 310°С.
Из приведенных на
рисунках 89, 90 и 91 кривых ясно, что в
пределах нормальных рабочих температур,
встречающихся в обычной электротехнической
практике, изменение магнитных свойств
железа и стали в зависимости от нагревания
настолько ничтожно, что при всякого
рода расчетах им можно пренебречь.
На рисунке 92
приведены еще характерные кривые,
представляющие результаты наблюдений
Гопкинсона над ходом намагничения
железа при разных температурах.
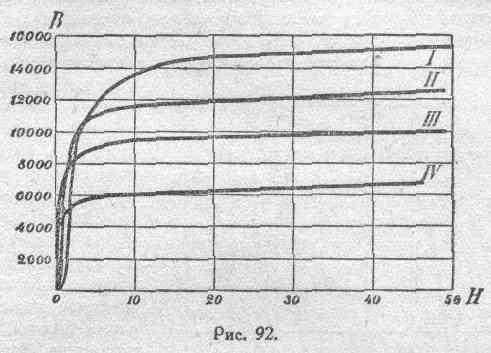
Здесь
кривая I
дает зависимость В
от
Н
при
температуре в 10°. Кривая 11 дает ту же
зависимость при температуре в 670°. Кривая
III
построена для
154
температуры
около 742°, и, наконец, кривая IV
— для температуры около 771°. На рисунке
93 представлены начальные части этих
кривых.
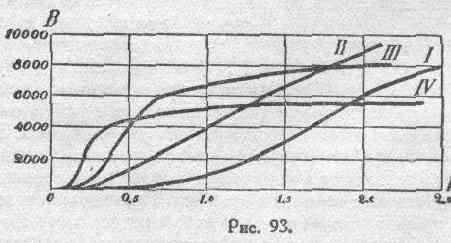
Здесь
масштаб Н
взят
нарочно большим, чтобы наглядно показать
относительное расположение кривых и
их пересечение. Обозначения кривых те
же, что и на рисунке 92.
Из
всех приведенных кривых отчетливо
видно, что чем слабее магнитное поле,
воздействующее на железо, тем большее
значение имеет повышение температуры
в смысле достижения высших степеней
намагничения. В этом отношении мы имеем
полную аналогию с влиянием сотрясений
на магнитные свойства ферромагнитных
материалов (см. § 39). В данном случае
гипотеза элементарных магнитов дает
возможность высказать предположение,
что с повышением температуры устойчивость
отдельных групп магнитиков должна
уменьшаться, так как при этом возрастает
общая подвижность всех молекул тела.
Надо полагать, что при приближении
к критической температуре эта подвижность
настолько уже велика, что достаточно
небольших добавочных воздействий со
стороны слабой намагничивающей силы
для того, чтобы нарушить исходные
группировки молекулярных магнитиков
и ориентировать ихв
направлении поля.
155
Есть
много данных в пользу того предположения,
что при переходе через критическую
температуру железо я
другие
магнитные материалы вообще претерпевают
какое-то резкое изменение в своих
свойствах. Так, при переходе через
критическую температуру резко меняются
термо-электрические свойства, а также
электрическое сопротивление материала.
Далее, железо и сталь, предварительно
нагретые выше критической температуры,
при остывании темнеют до достижения
этой температуры и затем внезапно
вспыхивают, проходя через нее. Это
последнее явление, открытое Барретом.
было им названо рекалесценцией.
Выяснилось,
что температура рекалесценции как раз
и есть температура критическая в
магнитном отношении. Современная
металлургия в полной мере выяснила
сущность того, что происходит с
железом и другими подобными материалами
при переходе через критическую
температуру. Именно, при этом происходит
очень быстрое изменение молекулярного
строения вещества, связанное с превращением
одной модификации его (магнитной)
в другую (немагнитную).
Кроме
тех изменений магнитных качеств железа,
которые обнаруживаются немедленно
при повышении температуры его, на
практике приходится встречаться еще с
одним явлением, которое также повидимому
обусловливается нагреванием. Речь идет
о так называемом старении
железа. Этот
процесс протекает очень медленно
при сравнительно низких температурах
и выражается между прочим в изменении
потерь на гистерезис, которые обычно
возрастают с течением времени. Такое
возрастание потерь на гисте-
156
резис
в прежнее время нередко наблюдалось
при работе трансформаторов переменного
тока, для изготовления которых применялось
простое железо. Есть основание полагать,
что в данном случае мы имеем дело с
медленным изменением молекулярного
строения железа. Опыт показывает,
что процесс старения ускоряется при
нагревании. В частности при температурах
порядка 150°—200° процесс этот протекает
в несколько дней, в то время как при
температурах порядка 50° он протекает
годы, прежде чем железо придет в некоторое
установившееся состояние. В связи с
тем, что явление впервые было наблюдено
в
трансформаторах,
сначала высказывалось предположение,
что возрастание потерь нагистерезис
представляет собою результат некоторой
усталости материала, происходящей
вследствие непрерывного перемагничивания,
подобно усталости упругого тела,
подверженного повторным механическим
напряжениям. Юинг, однако, показал, что
переменное намагничение само по себе
не производит никакого действия. Мордей
выяснил совершенно определенно, что
возрастание потерь на гистерезис
происходит исключительно благодаря
длительному нагреванию материала.
Это было затем подтверждено исследованием
Роджета. Для иллюстрации сказанного
выше о старении железа приведены на
рисунке 94 кривые гистерезиса, полученные
Роджетомдля
некоторого сорта железа при
Bmax=4000
гауссов.
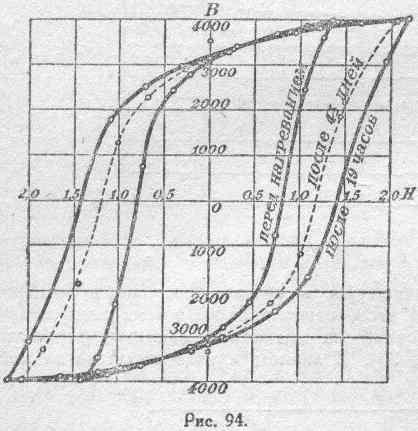
Здесь изображены
три цикла. Первый характеризует железо
в начальной стадии, т. е. до нагревания.
Второй — через 19 часов нагревания при
200°. Третий цикл характеризует материал
после нагревания при той же температуре
в течение 4 дней. За это время был пройден
максимум потерь на гистерезис.
В настоящее время
в области электрического машиностроения
и аппаратостроения вопрос о старении
железа потерял свою остроту, благодаря
тому, что удалось получить сплавы железа,
обладающие весьма устойчивыми магнитными
качествами (например, кремнистое железо).
Источник
Строение стали
Внимательно всмотревшись в излом металла, ясно можно увидеть, что он представляет собой нагромождение (совокупность) отдельных кристаллов (зерен), крепко сцепленных между собой. Мельчайшей частицей металла, как и всякого другого вещества, является атом. В элементарных ячейках, из которых состоят кристаллы железа, атомы расположены в определенном порядке. Это расположение изменяется в зависимости от температуры нагрева. При любой температуре ниже 910° атомы в ячейках кристаллов располагаются в виде куба, образуя так называемую кристаллическую решетку альфа-железа. В этом кубе восемь атомов расположены в углах решетки и один в центре.
При нагреве свыше 910° происходит перегруппировка атомов и кристаллическая решетка представляет собою форму куба с четырнадцатью атомами; условно ее называют решеткой гамма-железа. При температуре 1390° решетка гамма-железа перестраивается в решетку с девятью атомами, носящую название дельта-железо. Эта решетка отличается от решетки альфа-железа несколько большим расстоянием между центрами атомов и сохраняется до момента расплавления железа, т. е. до 1535° (Рис. 1).
Перестройка кристаллической решетки при медленном охлаждении происходит в обратном порядке: дельта-железо при 1390° превращается в гамма-железо, а гамма-железо при 898° превращается в альфа-железо.
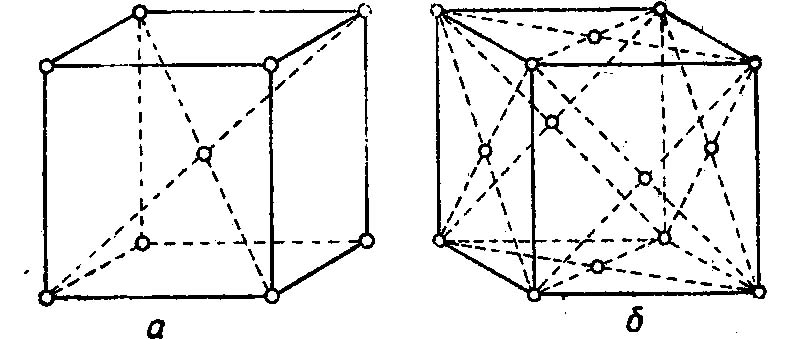
Рис. 1. Строение кристаллической решетки: а — альфа и дельта железа; б — гамма железа.
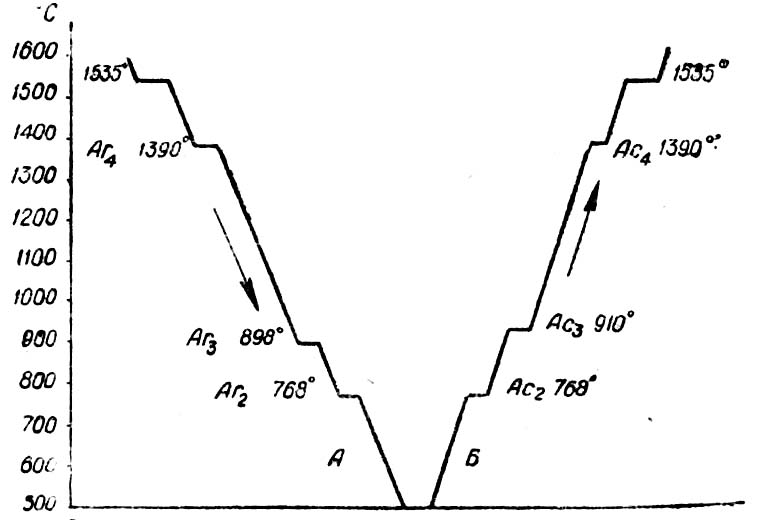
Критические точки превращения
На рис.2 показаны кривые охлаждения и нагревания чистого железа. Как видно из этих кривых, в процессе перестройки одной решетки в другую, а также при расплавлении и затвердевании железа происходят температурные остановки, являющиеся результатом выделения дополнительного количества тепла при охлаждении и поглощении дополнительного количества тепла при нагревании.

Рис. 2. Кривые охлаждения и нагрева чистого железа.
Температурные остановки, при которых происходят перестройки решеток, называются критическими температурами или критическими точками и обозначаются Аrпри охлаждении и Ас при нагревании. В точках Аr2и Ас2,не происходит перестройка атомной решетки, а изменяются магнитные свойства железа. При температуре выше 768° железо теряет способность притягиваться магнитом. При очень малой скорости нагревания и охлаждения критические точки А с3и Аr3не совпадают друг с другом на 12°. При увеличении скорости охлаждения несовпадение критических точек увеличивается, так как температура значительно снижается и железо переохлаждается. Это явление, носит название гистерезис.
При нагревании и охлаждении стали происходит также перестройка атомной решетки, но температуры критических точек не постоянны. Они зависят от содержания углерода и легирующих примесей в стали, а также от скорости нагревания и охлаждения.
На рис. 3 представлена диаграмма состояния углеродистой стали при медленном охлаждении и нагревании.
.jpg)
Рис.3. Диаграмма состояния углеродистых сталей.
Структура стали
Структурой стали называется внутреннее ее строение. Углерод в стали находится в виде химического соединения с железом, и это соединение называется — цементит. Кроме цементита, в стали имеется феррит, представляющий собой почти чистое железо. В зависимости от содержания углерода большая или меньшая часть феррита находится в механической смеси с цементитом, образуя новую структуру — перлит. Если небольшой кусок металла прошлифовать, отполировать и протравить в специальном реактиве, то под микроскопом можно различить структуры. Ниже приводится описание структур железоуглеродистых сплавов.
Аустенит представляет собою твердый раствор углерода и других элементов в гамма-железе. Наибольшее содержание углерода, которое может раствориться в ау-стените — это 2%. Аустенит образуется при затвердевании жидкой стали и при нагреве твердой стали выше критических температур.
В обычных сталях аустенит устойчив только лишь при температуре выше критических точек. При охлаждении, даже самом быстром, с этих температур аустенит превращается в другие структуры. При комнатной температуре аустенит полностью сохраняется в ряде марок нержавеющих сталей, в высокомарганцовистой стали и в незначительном количестве остается при закалке некоторых марок инструментальной и конструкционной сталей.
Аустенит мягок, пластичен, тягуч, мало упруг. Твердость его по Бринелю находится в пределах 170—220.
Аустенит немагнитен, обладает невысокой электропроводностью.
Феррит представляет собой твердый раствор углерода и других элементов в альфа-железе. Наибольшее содержание углерода, которое может раствориться в феррите, это 0,04%. Феррит устойчив при температурах ниже критической точки AC1. Он выделяется из аустенита при медленном охлаждении последнего ниже A6i. Феррит мягок, сильно тягуч. Твердость HB= 60—100. Феррит магнитен до 768°. Свыше этой температуры он теряет магнитные свойства.
Цементит представляет собой химическое соединение железа с углеродом Fe3C—карбид железа. Цементит содержит углерода 6,67%. Выделяется из жидкого и твердого раствора при медленном охлаждении. Цементит весьма тверд и хрупок. Твердость его НB= 800—820. Он магнитен до 210°. Выше этой температуры цементит теряет магнитные свойства.
Перлит представляет собой механическую смесь феррита и цементита. Он образуется из аустенита при медленном его охлаждении. Температура превращения аустенита в перлит 723°С. При весьма медленном переходе через эту температуру цементит образуется в виде зерен (глобулей), и тогда перлит называется зернистым. При более быстром охлаждении цементит приобретает форму пластинок, и такой перлит называется пластинчатым. При весьма быстром охлаждении в результате значительного переохлаждения аустенита вместо перлита получаются другие структуры, о которых речь будет ниже.
Перлит магнитен, прочен и пластичен. Твердость его находится в пределах от 160 до 230 кг/мм2 по Бринелю. При обработке резанием наиболее чистую поверхность дает структура зернистого перлита.
Мартенсит образуется в результате весьма быстрого охлаждения (закалки) аустенита. При быстром охлаждении успевает произойти перестройка кристаллической решетки гамма-железа в решетку альфа-железа, выделение же углерода в карбид железа не успевает произойти, и он весь остается растворенным в решетке альфа-железа. Так как нормально альфа-железо может растворить в себе не более 0,04% углерода, то такой раствор называют пересыщенным. Он отличается весьма большой твердостью (свыше Rc= 60) и хрупкостью. Следует указать, что решетка альфа-железа, получающаяся в результате закалки, имеет искаженную форму. Так, размеры ее граней не одинаковы — в одном направлении они удлинены за счет других (см. рис. 4). Такая решетка называется тетрагональной. Чем больше в стали углерода, тем больше тетрагональность решетки и тем более велики внутренние напряжения. При нагревании до температур 100—200° тетрагональность мартенсита уменьшается, форма кристаллической его решетки приближается к форме правильного куба, и вместе с этим уменьшаются внутренние напряжения. Мартенсит магнитен.
.jpg)
Рис. 4. Строение кристаллической решетки стали, закаленной на мартенсит.
Троостит представляет собой высокодисперсную (мелкораздробленную) смесь феррита и карбидов. Он образуется при охлаждении аустенита с замедленной против закалки скоростью или в результате нагрева (отпуска) мартенсита в пределах 250—400°.
При нагреве закаленной стали происходит постепенное выделение углерода из кристаллической решетки с образованием карбидов. Троостит менее прочен, более пластичен, чем мартенсит. Твердость его НB330—400. При охлаждении аустенита в горячих средах в интервале 250—400° (изотермическое превращение аустенита) происходит образование игольчатого троостита, несколько более прочного, чем обычный троостит.
Сорбит представляет собой дисперсную смесь феррита и карбидов. Он образуется при охлаждении аустенита с небольшой скоростью или при нагреве (отпуске) мартенсита до 400—650°. Карбиды сорбита более крупные, чем троостита. Сорбит пластичен, вязок и магнитен. Твердость НВ 270—320.
Ледебурит представляет собой эвтектическую смесь аустенита и цементита. Он содержит углерода 4 3% Образуется ледебурит при затвердевании жидкого сплава с содержанием углерода свыше 2%. Ледебурит хрупок.
На рис. 5. представлены фотоснимки структур стали с различным содержанием углерода.
Структура стали с содержанием углерода 0,83% состоит из сплошного перлита и называется эвтектоидной; при меньшем содержании углерода структура стали состоит из перлита и феррита и носит название доэвтектоидной, а при большем содержании углерода — из перлита и цементита и называется заэвтектоидной. Температура 723°, при которой перлит переходит в аустенит, также называется критической и обозначается Ас.
Для того чтобы доэвтектоидную и эвтектоидную сталь полностью отжечь, нормализовать или закалить, их нужно нагреть до такой температуры, при которой они перешли бы в аустенитное состояние.
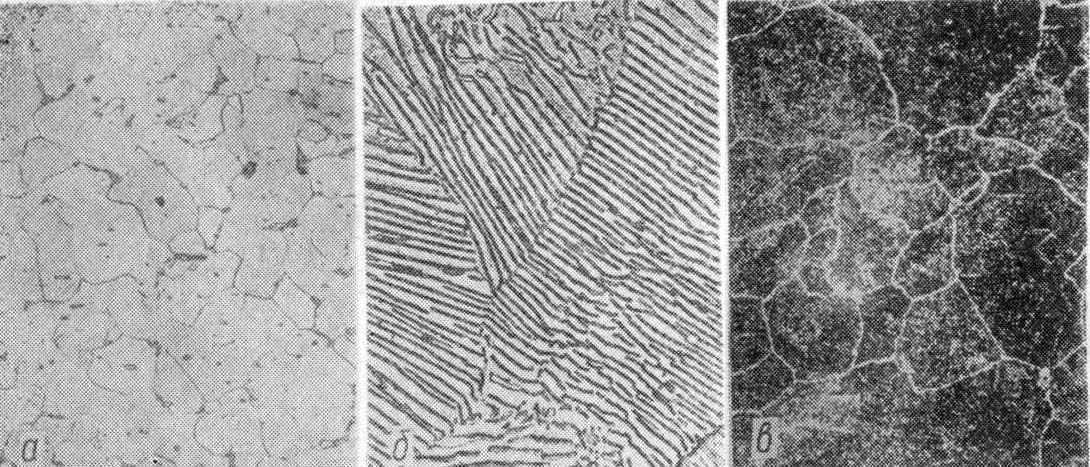
Рис. 5. Микроструктура отожженной углеродистой стали:
а – с содержанием углерода -0,1%
б – с содержанием углерода -0,85%
в – с содержанием углерода -1,1%
Превращения, происходящие в стали при нагревании
По диаграмме на рис. 3 можно проследить за изменениями структуры трех разных марок стали при нагревании:
- Сталь с содержанием углерода 0,83%. Структура стали представляет собой перлит. При температуре 723° в точке Aс1 перлит переходит в аустенит.
- Сталь с содержанием углерода 0,4%. Структура стали представляет собой перлит и феррит. При температуре 723° в точке К1 перлит переходит в аустенит, и по мере повышения температуры происходит растворение свободного феррита в аустените. При пересечении линии GS в точке К2 закончится растворение феррита и структура будет полностью состоять из аустенита. Для этой стали точка К1на диаграмме будет нижней критической точкой Ас1,а К2— верхней критической точкой Ас1,.
- Сталь с содержанием углерода 1,2%. Структура стали представляет собой перлит и цементит. При температуре 723° в точке Pi перлит переходит в аустенит, и при дальнейшем повышении температуры происходит постепенное растворение цементита в аустените. При пересечении линии SEв точке Р2 это растворение закончится. Для этой стали точка Р1 явится нижней критической точкой Ас1, а точка Ρ2 — верхней критической точкой, которая для заэвтектоидных сталей обозначается Асm.
Линия на диаграмме, обозначенная буквами GS, соответствует окончанию растворения феррита в аустените в доэвтектоидных сталях, а линия SE соответствует окончанию растворения цементита в аустените в заэвтектоидных сталях.
Следует указать, что заэвтектоидные стали при операциях термической обработки не нагревают выше линии Аcт(такая высокая температура нагрева приведет к перегреву и ухудшению свойств стали), а ограничиваются нагревом выше первой критической точки ACl, что полностью обеспечивает получение необходимых свойств.
Превращения, происходящие в стали при медленном охлаждении
В сталях, нагретых до аустенитного состояния, при весьма медленном охлаждении произойдут обратные превращения, а именно:
а) в стали с содержанием углерода 0,83% аустенит превратится в перлит;
б) в стали с содержанием углерода 0,4% сначала из аустенита начнет выделяться феррит, а затем в районе температуры 700° оставшийся аустенит превратится в перлит и
в) в стали с содержанием углерода 1,2% сначала из аустенита выделится цементит, а затем в районе температуры 700° оставшийся аустенит превратится в перлит.
Даже при весьма медленном охлаждении температура распада аустенита не совпадает с теми температурами, при которых аустенит образовался при нагревании. Чем скорость охлаждения больше, тем больше становится гистерезис, т. е. разница между критическими температурами (точками) при нагревании и охлаждении.
Превращения, происходящие в стали при быстром охлаждении
Как указывалось выше, при быстром охлаждении не успевает произойти превращение аустенита в перлит с выделением избыточного феррита или цементита, а в зависимости от скорости охлаждения аустенит превращается в новые структуры – мартенсит, троостит или сорбит. Сталь с этими структурами отличается от сталей со структурами перлита и феррита повышенной твердостью, прочностью и уменьшенной пластичностью. Если углеродистую сталь, нагретую выше критических температур, охладить очень быстро, то аустенит превратится в мартенсит и это превращение начнется лишь при температуре около 200°. При несколько меньшей скорости охлаждения образуется структура троостит, а при еще меньшей — сорбит.
В производственных условиях при охлаждении углеродистой инструментальной стали в воде образуется мартенсит, при охлаждении в масле — троостит и при охлаждении в струе воздуха -сорбит. На рис. 6 показаны микроструктуры закаленной стали.

Рис. 6. Микроструктура закаленной стали:
а — игольчатый мартенсит;
б — сорбит.
В легированных сталях, благодаря присутствию специальных элементов, для образования мартенсита не требуется столь большой скорости охлаждения, как для углеродистых сталей, и мартенсит образуется при охлаждении в масле, а для быстрорежущих сталей — и при охлаждении на воздухе.
Троостит и сорбит можно получить не только в результате ускоренного охлаждения, нои путем нагрева закаленной стали, имеющей структуру мартенсита, до температуры ниже Aс1, т. е. путем отпуска стали. В этом случае троостит получается при нагреве стали до 400°, а сорбит—при нагреве до 650°. При нагреве до промежуточных температур получаются смешанные структуры: при нагреве от 250—400° — мартенсит и троостит и при нагреве от 400—650° — троостит и сорбит. В производственных условиях троостит и сорбит получают путем отпуска закаленной стали.
Превращения, происходящие в стали при охлаждении в среде, имеющей температуру выше 200° (изотермическое превращение)
Если деталь, нагретую выше критической точки, поместить в среду, имеющую температуру от 700 до примерно 200°, и выдержать в ней до выравнивания температуры по всему сечению, то аустенит превратится в ту структуру, которая соответствует превращению при данной температуре.
О поведении стали при изотермической обработке, выборе температуры и времени выдержки судят по кривым изотермического превращения, построенным для разных марок стали.
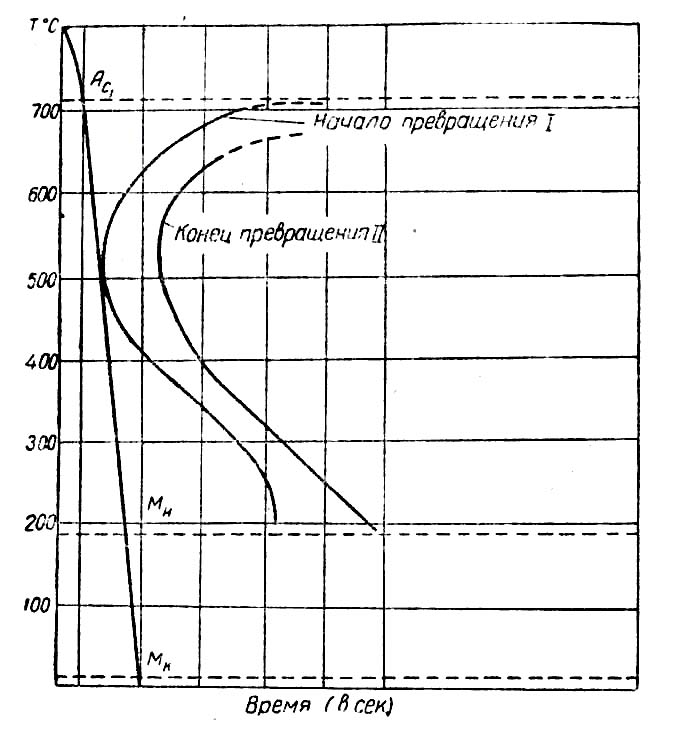
Рис. 7. Диаграмма изотермического превращения аустенита углеродистой стали.
На рис. 7 дан вид диаграммы изотермического превращения в стали. На горизонтальной оси отложено время начала и конца превращения, а на вертикальной— температура, при которой оно происходит. Линия А с соответствует переходу аустенита в перлит, а линия Мн — образованию мартенсита из аустенита. На кривой I начинаются, а на кривой II заканчиваются структурные превращения.
Если углеродистую инструментальную сталь, нагретую до 800°, поместить в масло, расплавленную соль или щелочь при температуре 250°, в ней образуется игольчатый троостит с высокой твердостью Rc=45—55. Если эту же сталь охладить в среде, имеющей температуру свыше 600°, в ней образуется перлит и такая сталь легко обрабатывается на станках. При охлаждении стали в среде с промежуточными температурами образуются структуры троостита и сорбита с соответствующей твердостью.
Изотермический отжиг нашел большое применение при термической обработке инструментальных сталей как процесс, резко уменьшающий время по сравнению с другими видами отжига.
Изотермическая закалка в инструментальном деле применяется редко из-за недостаточной для инструмента твердости, достигаемой при этом процессе.
Источник:
Остапенко Н.Н.,Крапивницкий Н.Н. Технология металлов. М. Высшая школа,1970г.
Каменичный И.С. Практика термической обработки инструмента. Киев, 1959 г.
Источник
