С наличием каких катионов связано такое свойство клетки как раздражимость
Обмен веществ в клетках. Раздражимость клеток
Обмен веществ — поступление в клетку веществ, их усвоение и выведение продуктов жизнедеятельности. Вещества из внешней среды поступают через цитоплазматическую мембрану н по каналам эндоплазматическои сети или непосредственно по гиалоплазме транспортируются к клеточным органоидам и ядру. Их дальнейшие превращения происходят под воздействием многочисленных ферментов, которые синтезируются в клетке на рибосомах эндоплазматическои сети.
Энергия, необходимая для процессов обмена, вырабатывается, накапливается и распределяется митохондриями. Продукты жизнедеятельности клетки по каналам эндоплазматическои сети поступают к цитоплазматической мембране, через которую и выводятся, либо образуют в цитоплазме клеточные включения. Белковые секреты обычно транспортируются к пластинчатому комплексу, в котором накапливаются и обособляются в виде секреторных гранул.
Разнообразные ферменты, способные расщеплять (гидролизировать) макромолекулярные комплексы клетки, содержатся в лизосомах. При разрыве лизосомноп мембраны (например, в результате повреждения клетки) ферменты высвобождаются и происходит переваривание ими клеточного содержимого. Этим можно объяснить лизис мертвых или умирающих клеток.
Раздражимость — свойство клеток отвечать на воздействие окружающей среды. Формы раздражимости различны: возбудимость нервных и мышечных клеток, секретообразованпе, выделение секрета и др. Более простой реакцией на внешние воздействия является внутреннее перемещение частей клетки, в результате чего осуществляется и функция движения клетки вцелом. Движение клетки может быть также результатом сокращения миофибрилл, биения ресничек или жгутиков в ответ на раздражители.
Жизненный цикл клетки начинается с момента ее образования (в результате деления материнской клетки), включает процессы роста и дифференциации и заканчивается у одних клеток делением, у других старением и смертью. В быстро делящихся клетках период между двумя делениями (интерфаза) короткий. У клеток, утративших способность к делению, интерфаза является основным периодом жизненного цикла, длительность ее может совпадать со сроком жизни организма (например, у невроцитов).

Различают непрямое деление клеток — митоз или кариокинез и прямое деление — амитоз. Специализированной формой митоза является эндомитоз. У половых клеток имеет место особый вид деления — мейоз.
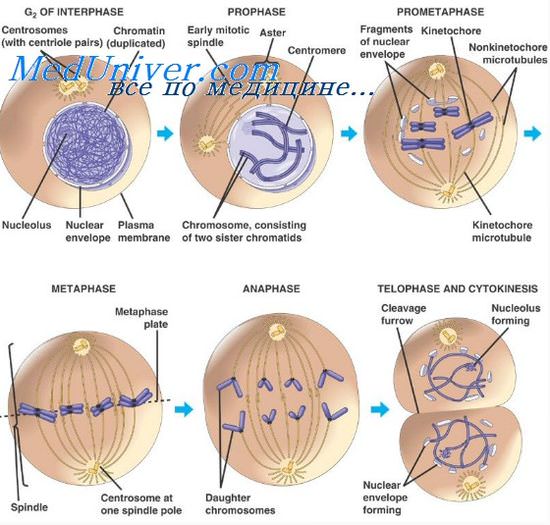
Митоз — наиболее распространенный способ деления, в результате которого каждая из двух дочерних клеток получает такой же набор хромосом, какой имела материнская клетка (2n). Во время этого процесса происходит полная перестройка ядра, протекающая в закономерной последовательности и состоящая из ряда постепенно сменяющихся стадий: профаза, метафаза, анафаза и телофаза.
В ранней профазе происходит заметное увеличение ядра и появление хромосом в виде спирализованных тонких нитей, сплетенных наподобие клубка, равномерно заполняющего ядро. По мере развития профазы хромосомы прогрессивно спирализуются, что обусловливает их укорочение и уплотнение; при этом связь между хроматидами ослабевает; к концу профазы они располагаются параллельно друг другу, оставаясь соединенными только в области центромеров (перетяжек). Окончание профазы связано с разрушением оболочки ядра, исчезновением ядрышка и появлением митотического веретена с двумя полюсами, формирующегося из центросомы.
В метафазе максимально укороченные хромосомы, направляемые своими центромерами, постепенно передвигаются к экватору веретена, где они располагаются в одной плоскости точно посередине между полюсами. Хромосомы связаны с нитями веретена при помощи иентромер. В этот период число, размеры и форму хромосом легко определить, рассматривая их со стороны полюсов.
Переход из метафазы в анафазу выражен четко. Одновременно во всех хромосомах удваиваются центромеры. Они двигаются к противоположным полюсам, увлекая за собой разъединившиеся сестринские хроматиды, которые с этого момента называются сестринскими хромосомами.
– Также рекомендуем “Телофаза и интерфаза митоза. Первое деление мейоза клеток”
Оглавление темы “Деление клеток. Половой хроматин”:
1. Обмен веществ в клетках. Раздражимость клеток
2. Телофаза и интерфаза митоза. Первое деление мейоза клеток
3. Второе деление мейоза. Амитоз и эндомитоз
4. Дифференциация клеток. Регенерация клеток
5. Способы регенерации клеток. Старение и гибель клетки
6. Удаление мертвых клеток из организма. Хромосомный пол
7. Половой хроматин. Тельца Барра
8. Х-хроматин в клетках различных тканей. Наличие Х-хроматина в клетках
9. Х-хроматин в лейкоцитах. Половые различия лейкоцитов
10. Половые виды лимфоцитов. Y-хроматин клеток организма
Источник
Ключевую роль в жизнедеятельности организмов играет совсем незначительное их количество. Это главным образом ионы металлов.
Катионы К +, Na +, Са2 + обеспечивают универсальное свойство живой материи – раздражимость, поддерживают осмотическое давление в клетке, у животных они участвуют в передаче нервных импульсов. Кроме того, К + и Na + участвуют в специальном механизме транспортировки различных соединений в клетку и их выводе за ее пределы. Преимущественно ионы Na + находятся за пределами клетки, а К + – внутри клетки. Ионы Са2 + обусловливают мышечные сокращения.

Какую функцию в клетках выполняют катионы и анионы
Катион Mg2 + входит в состав молекулы хлорофилла, содержится в костях и зубах, активизирует химические реакции, протекающие в клетках всех без исключения существ, a Fe2 + входит в состав гемоглобина, миоглобина, дыхательных пигментов.
Особа функция катиона NH4, участвующий в поддержании устойчивого pH в клетке. Он является важным компонентом синтеза белков, но его избыток, вызванный нарушением обмена веществ, может приводить к значительным функциональным расстройствам.
Важную роль в организмах разных видов живых существ играют анионы ортофосфорной кислоты Н2РС > 4 и НРО -, которые обусловливают буферность (от англ. Баф – смягчать толчки) клетки – способность поддерживать внутриклеточную среду на уровне установившегося значения pH 6,9, которое свойственно содержанию большинства клеток человека. Тогда как анионы угольной кислоты НСО3 поддерживают постоянное pH на уровне 7,4 за пределами клетки. Анионы HSO4 взаимодействуют с малорастворимыми соединениями и таким образом лишают организм различных шлаков. Анион СИ – является компонентом желудочного сока животных, а анион И – входит в состав гормона тироксина. (Вспомните, какой железой вырабатывается этот гормон.)
Где встречаются нерастворимые минеральные соединения
Особое значение приобретают нерастворимые в воде минеральные соли – неотъемлемый компонент всех опорных структур животных. При этом ключевым веществом является кальций ортофосфат Са3 (Р04) 2 – составляющая межклеточного «цемента», что обеспечивает соединение клеток в ткани. Кроме того, он непременно содержится в скелете, в частности в костях позвоночных животных или в раковине моллюсков.
Явление ионной асимметрии живого
В современной биологии считается вполне доказанным, что всем живым организмам присуще явление ионной асимметрии. Оно заключается в неравномерном распределении ионов одного и того же заряда как внутри, так и за пределами клетки. Типичным примером является разница в концентрации ионов Na + и К + в клетке и за ее пределами.
Несмотря на незначительное содержание, минеральные вещества и ионы являются важными составляющими каждого организма. Именно эти соединения, содержащиеся в клетках и за их пределами в виде ионов, ответственные за важнейшие функции – раздражительность и скорость обмена веществ – входят в состав многих важных веществ. У животных они ответственны за проведение нервного импульса и сокращение мышечных клеток, объединение клеток в ткани и межклеточное взаимодействие.
Нерастворимые соли участвуют в образовании скелета, ответственные за соединение клеток.
Оценка статьи:
Загрузка…
Теги: Биология, буферность, важнейшие функции, жизнь, клетка, природа, тироксин, функционирование организма
Источник
Минеральные вещества в клетке находятся в виде солей в твёрдом состоянии, либо диссоциированы на ионы.
Неорганические ионы представлены катионами и анионами минеральных солей.
Пример:
катионы: K+, Na+, Ca2+, Mg2+, NH4+.
Анионы: Cl−, H2PO4−, HPO42−, HCO3−, NO3−, SO42−, PO43−, CO32−.
Вместе с растворимыми органическими соединениями неорганические ионы обеспечивают стабильные показатели осмотического давления.
Концентрация катионов и анионов в клетке и в окружающей её среде — различна. Внутри клетки преобладают катионы K+ и крупные отрицательные органические ионы, в околоклеточных жидкостях всегда больше ионов Na+ и Cl−. В результате образуется разность потенциалов между содержимым клетки и окружающей её средой, обеспечивающая такие важные процессы, как раздражимость и передача возбуждения по нерву или мышце.
Являясь компонентами буферных систем организма, ионы определяют их свойства — способность поддерживать рН на постоянном уровне (близко к нейтральной реакции), несмотря на то, что в процессе обмена веществ непрерывно образуются кислые и щелочные продукты.
Пример:
анионы фосфорной кислоты (HPO42− и H2PO4−) создают фосфатную буферную систему млекопитающих, поддерживающую рН внутриклеточной жидкости в пределах (6,9)–(7,4).
Угольная кислота и её анионы (H2CO3 и CO32−) создают бикарбонатную буферную систему и поддерживают рН внеклеточной среды (плазмы крови) на уровне (7,4).
Соединения азота, фосфора, кальция и другие неорганические вещества используются для синтеза органических молекул (аминокислот, белков, нуклеиновых кислот и др.).
Пример:
ионы некоторых металлов (Mg, Ca, Fe, Zn, Cu, Mn, Mo, Br, Co) являются компонентами многих ферментов, гормонов и витаминов или активируют их.
Калий — обеспечивает функционирование клеточных мембран, поддерживает кислотно-щелочное равновесие, влияет на активность и концентрацию магния.
Ионы Na+ и K+ способствуют проведению нервных импульсов и возбудимости клетки. Эти ионы входят также в состав натрий-калиевого насоса (активный транспорт) и создают трансмембранный потенциал клеток (обеспечивают избирательную проницаемость клеточной мембраны, что достигается за счёт разности концентраций ионов Na+ и K+: внутри клетки больше K+, снаружи больше Na+).
Ключевая роль в регуляции мышечного сокращения принадлежит ионам кальция (Ca2+). Миофибриллы обладают способностью взаимодействовать с АТФ и сокращаться лишь при наличии в среде определённых концентраций ионов кальция. Ионы кальция также необходимы для процесса свёртывания крови.
Железо входит в состав гемоглобина крови.
Азот входит в состав белков. Все важнейшие части клеток (цитоплазма, ядро, оболочка и др.) построены из белковых молекул.
Фосфор входит в состав нуклеиновых кислот; обеспечивает нормальный рост костной и зубной тканей.
При недостатке минеральных веществ нарушаются важнейшие процессы жизнедеятельности клетки.
Источники:
Каменский А. А., Криксунов Е. А., Пасечник В. В. Биология. 9 класс // ДРОФА.
Каменский А. А., Криксунов Е.А., Пасечник В.В. Биология. Общая биология (базовый уровень) 10–11 класс // ДРОФА.
Лернер Г. И. Биология: Полный справочник для подготовки к ЕГЭ: АСТ, Астрель.
Источник
Лекция 2. Химический состав клеток. Вода, соли.
Цитология. Изучением клетки занимается цитология (от греч. цитос – клетка и логос – наука). Изучается строение клеток, строение и функции клеточных органоидов, процессы жизнедеятельности, протекающие в клетке. Каждая клетка проявляет все свойства живого – обмен веществ, раздражимость, развитие и размножение, является элементарной (наименьшей) единицей строения. Изучение клетки логично начать с изучения химического состава клетки.
Химический состав клеток.
Все клетки, независимо от уровня организации, сходны по химическому составу. В живых организмах обнаружено 86 химических элементов периодической системы Д.И.Менделеева. Для 25 элементов известны функции, которые они выполняют в клетке. Эти элементы называются биогенными. По количественному содержанию в живом веществе элементы делятся на три категории:
Макроэлементы, элементы, концентрация которых превышает 0,001%. Они составляют основную массу живого вещества клетки (около 99%). Макроэлементы делят на элементы 1 и 2 группы. Элементы 1-ой группы – C, N, H, O (на их долю приходится 98% от всех элементов). Элементы 2-ой группы – K, Na, Ca, Mg, S, P, Cl, Fe (1,9%).
Микроэлементы (Zn, Mn, Cu, Co, Mo, и многие другие), доля которых составляет от 0,001% до 0,000001%. Микроэлементы входят в состав биологически активных веществ – ферментов, витаминов и гормонов.
Ультрамикроэлементы (Hg, Au, U, Ra и др.), концентрация которых не превышает 0,000001%. Роль большинства элементов этой группы до сих пор не выяснена.
Макро- и микроэлементы присутствуют в живой материи в виде разнообразных химических соединений, которые подразделяются на неорганические и органические вещества.
К неорганическим веществам относятся: вода и минеральные вещества. К органическим веществам относятся: белки, жиры, углеводы, нуклеиновые кислоты, АТФ и другие низкомолекулярные органические вещества. Процентное соотношение указано в таблице 1.
Неорганические вещества клетки. Вода.
Вода – самое распространенное в живых организмах неорганическое соединение. Ее содержание колеблется в широких пределах: в клетках эмали зубов вода составляет по массе около 10%, а в клетках развивающегося зародыша – более 90%.
Без воды жизнь невозможна. Она не только обязательный компонент живых клеток, но и среда обитания организмов. Биологическое значение воды основано на ее химических и физических свойствах. Химические и физические свойства воды необычны. Они объясняются, прежде всего, малыми размерами молекул воды, их полярностью и способностью соединяться друг с другом водородными связями.
В молекуле воды один атом кислорода ковалентно связан с двумя атомами водорода. Молекула полярна: кислородный атом несет частичный отрицательный заряд, а два водородных – частично положительные заряды. Это делает молекулу воды диполем. Поэтому при взаимодействии молекул воды друг с другом между ними устанавливаются водородные связи. Они слабее ковалентной, но, поскольку каждая молекула воды способна образовывать 4 водородные связи, они существенно влияют на физические свойства воды. Большая теплоемкость, теплота плавления и теплота парообразования объясняются тем, что большая часть поглощаемого водой тепла расходуется на разрыв водородных связей между ее молекулами. Вода обладает высокой теплопроводностью, благодаря чему в различных участках клетки поддерживается одинаковая температура. Вода практически не сжимается, прозрачна в видимом участке спектра. Наконец, вода – единственное вещество, плотность которого в жидком состоянии больше, чем в твердом.
Вода – хороший растворитель ионных (полярных) соединений, а также некоторых не ионных, в молекуле которых присутствуют заряженные (полярные) группы. Если энергия притяжения молекул воды к молекулам какого-либо вещества больше, чем энергия притяжения между молекулами вещества, то молекулы гидратируются и вещество растворяется. По отношению к воде различают гидрофильные вещества – вещества, хорошо растворимые в воде и гидрофобные вещества – вещества, практически нерастворимые в воде. Есть органические молекулы, у которых один участок – гидрофилен, другой – гидрофобен. Такие молекулы называют амфипатическими, к ним относятся, например, фосфолипиды, образующие основу биологических мембран.
Вода является непосредственным участником многих химических реакций (гиролитическое расщепление белков, углеводов, жиров и др.), необходима как метаболит для реакций фотосинтеза.
Большинство биохимических реакций может идти только в водном растворе; многие вещества поступают в клетку и выводятся из нее в водном растворе. Благодаря большой теплоте испарения воды, происходит охлаждение организма.
Максимальная плотность воды при +4°С, при понижении температуры вода поднимается вверх, а так как плотность льда меньше плотности воды, то лед образуется на поверхности, поэтому при замерзании водоемов подо льдом остается жизненное пространство для водных организмов.
Благодаря силам когезии (электростатическому взаимодействию молекул воды, водородным связям) и адгезии (взаимодействию с окружающими ее стенками) вода обладает свойством подниматься по капиллярам – один из факторов, обеспечивающих движение воды в сосудах растений.
Несжимаемость воды определяет напряженное состояние клеточных стенок (тургор), а также выполняет опорную функцию (гидростатический скелет, например, у круглых червей).
Итак, значение воды для организма заключается в следующем:
- Является средой обитания для многих организмов;
- Является основой внутренней и внутриклеточной среды;
- Обеспечивает транспорт веществ;
- Обеспечивает поддержание пространственной структуры растворенных в ней молекул (гидратирует полярные молекулы, окружает неполярные молекулы, способствуя их слипанию);
- Служит растворителем и средой для диффузии;
- Участвует в реакциях фотосинтеза и гидролиза;
- При испарении участвует в терморегуляции организма;
- Обеспечивает равномерное распределение тепла в организме;
- Максимальная плотность воды при +4°С, поэтому лед образуется на поверхности воды.
Минеральные вещества.
Минеральные вещества клетки в основном представлены солями, которые диссоциируют на анионы и катионы, некоторые используются в неионизированной форме (Fe, Mg, Cu, Co, Ni и др.)
Для процессов жизнедеятельности клетки наиболее важны катионы Na+, Ca2+, Mg2+, анионы HPO42-, Cl-, HCO3-. Концентрации ионов в клетке и среде ее обитания, как правило, различны. В нервных и мышечных клетках концентрация К+ внутри клетки в 30-40 раз больше, чем вне клетки; концентрация Na+ вне клетки в 10-12 раз больше, нежели в клетке. Ионов Сl- вне клетки в 30—50 раз больше, чем внутри клетки. Существует ряд механизмов, позволяющих клетке поддерживать определенное соотношение ионов в протопласте и внешней среде.
Табл. 1. Важнейшие химические элементы
Химический элемент | Вещества, в которых химический элемент содержится | Процессы, в которых химический элемент участвует |
Углерод, водород, кислород, азот | Белки, нуклеиновые кислоты, липиды, углеводы и др. органические вещества | Синтез органических веществ и весь комплекс функций, осуществляемых этими органическими веществами |
Калий, натрий | Na+ и K+ | Обеспечивают функции мембран, в частности, поддерживают электрический потенциал клеточной мембраны, работу Na+/Ka+-насоса, проведение нервных импульсов, анионный, катионный и осмотический балансы |
Кальций | Са+2 Фосфат кальция, карбонат кальция Пектат кальция | Участвует в процессе свертывания крови, сокращения мышц, входит в состав костной ткани, зубной эмали, раковин моллюсков Формирование срединной пластинки и клеточной стенки у растений |
Магний | Хлорофилл | Фотосинтез |
Сера | Белки | Формирование пространственной структуры белка за счет образования дисульфидных мостиков |
Фосфор | Нуклеиновые кислоты, АТФ | Синтез нуклеиновых кислот, фосфорилирование белков (их активирование) |
Хлор | Cl- HCl | Поддерживает электрический потенциал клеточной мембраны, работу Na+/Ka+-насоса, проведение нервных импульсов, анионный, катионный и осмотический балансы Активизирует пищеварительные ферменты желудочного сока |
Железо | Гемоглобин Цитохромы | Транспорт кислорода Перенос электронов при фотосинтезе и дыхании |
Марганец | Декарбоксилазы, дегидрогеназы | Окисление жирных кислот, участие в процессах дыхания и фотосинтеза |
Медь | Гемоцианин Тирозиназа | Транспорт кислорода у некоторых беспозвоночных Образование меланина |
Кобальт | Витамин В12 | Формирование эритроцитов |
Цинк | Входит в состав более 100 ферментов: Алькогольдегидрогеназа, карбоангидраза | Анаэробное дыхание у растений Транспорт СО2 у позвоночных |
Фтор | Фторид кальция | Костная ткань, зубная эмаль |
Иод | Тироксин | Регуляция основного обмена |
Молибден | Нитрогеназа | Фиксация азота |
Различные ионы принимают участие во многих процессах жизнедеятельности клетки: катионы К+, Na+, Ca2+ обеспечивают раздражимость живых организмов; катионы Mg2+, Mn2+, Zn2+, Ca2+ и др. необходимы для нормального функционирования многих ферментов; образование углеводов в процессе фотосинтеза невозможно без Mg2+ (составная часть хлорофилла).
От концентрации солей внутри клетки зависят ее буферные свойства. Буферностью называют способность клетки поддерживать слабощелочную реакцию своего содержимого на постоянном уровне (рН около 7,4). Внутри клетки буферность обеспечивается главным образом анионами H2PO4- и НРО42-. Во внеклеточной жидкости и в крови роль буфера играют Н2СО3 и НСО3-.
Фосфатная буферная система:
Низкий pH Высокий pH
НРО42- + Н+ H2PO4-
Гидрофосфат – ион Дигидрофосфат – ион
Бикарбонатная буферная система:
Низкий pH Высокий pH
НСО3- + Н+ H2СO3
Гидрокарбонат – ион Угольная кислота
Некоторые неорганические вещества содержатся в клетке не только в растворенном, но и в твердом состоянии. Например, Са и Р содержатся в костной ткани, в раковинах моллюсков в виде двойных углекислых и фосфорнокислых солей.
Ключевые термины и понятия
1. Общая биология. 2. Тропизмы, таксисы, рефлексы. 2. Биогенные элементы. 3. Макроэлементы. 4. Элементы 1 и 2 групп. 5. Микро- и ультрамикроэлементы. 6. Гидрофильные и гидрофобные вещества. 7. Амфипатические вещества. 8. Гидролиз. 9. Гидратация. 10. Буферность.
Основные вопросы для повторения
- Перечислите уровни организации жизни на Земле.
- Перечислите основные свойства живых организмов.
- Классификация организмов, относящихся к империи Клеточные.
- Строение молекулы воды и ее свойства.
- Значение воды.
- Процентное соотношение органических веществ в клетке.
- Важнейшие катионы клетки и их концентрация в нервных и мышечных клетках.
- Реакция фосфатной буферной системы при понижении рН.
- Реакция карбонатной буферной системы при повышении рН.
Рис. . Вода. Значение воды.
Источник
