Свойства какого вещества описаны в тексте

- Главная
- Вопросы & Ответы
- Вопрос 3468623
Суррикат Мими
более месяца назад
Просмотров : 27
Ответов : 1
Лучший ответ:
Таня Масян
1 в первом ответ это озон а второе – кислород. Только дурак это не может знать
более месяца назад
Ваш ответ:
Комментарий должен быть минимум 20 символов
Чтобы получить баллы за ответ войди на сайт

Лучшее из галереи за : неделю месяц все время































Другие вопросы:
Васян Коваль
Умоляяяяююю, пожалуйста!!!!!!! Сколько сможете, пожалуйста
более месяца назад
Смотреть ответ
Просмотров : 13
Ответов : 1
Онтонио Веселко
Найдите координаты москвы широту и долготу на политической карте
более месяца назад
Смотреть ответ
Просмотров : 13
Ответов : 1
Мари Умняшка
Докажите тождество (4x-7)*0,4-0,5*(2x-3)-(-1,9-1,2x)=1
более месяца назад
Смотреть ответ
Просмотров : 26
Ответов : 1
Главный Попко
Помогите пожалуйста решить уравнение через дискриминант
более месяца назад
Смотреть ответ
Просмотров : 12
Ответов : 1
Пармезан Черница
Определите, в каком предложении причастие является сказуемым. 1. Заветный парк леди Сюзанны показался рыцарям местом весьма запущенным. 2. Беседка для тайных свиданий и качели для счастливой молодёжи не были покрашены. 3. На старой липе висел скворечник, отделанный рубинами и сапфирами. 4. Из него…
более месяца назад
Смотреть ответ
Просмотров : 24
Ответов : 1
Источник
Административный тест по химии в 9 классе за I-ое полугодие (I вариант)
А1. Как изменяются окислительные свойства в ряду элементов:
F→ Сl→ Br→ I?
ослабевают
не изменяются
усиливаются
сначала усиливаются, а потом ослабеваю
А2. Укажите электронную формулу атома серы
1S22S22P63S23P4
1S22S22P63S23P0
1S22S22P63S23P6
1S22S22P63S03P0
A3. Свойства какого вещества описаны в тексте: «… — газ с характерным запахом грозы, светло-фиолетового цвета, разрушает органические вещества. Окисляет металлы, в том числе золото и платину, производит белящее и дезинфицирующее действие»
пары йода
кислород
озон
азот
А4. В лаборатории имеются растворы реактивов: фенолфталеин, нитрат бария, гидроксид натрия, нитрат серебра, метилоранж, гидроксид кальция, сульфат калия, лакмус. Для установления качественного состава соляной кислоты необходимо воспользоваться реактивами:
лакмус и сульфат калия
фенолфталеин и гидроксид кальция
метилоранж и нитрат серебра
гидроксид натрия и нитрат бария
А5. Укажите вид химической связи в молекуле хлороводорода?
1) ионная
2) ковалентная полярная
3) ковалентная неполярная
4) металлическая
В1. Установите соответствие:
Химическая формула | |
А) Плавиковая кислота Б) Сульфит натрия В) Оксид серы( IѴ) Г) Гипс Д) Бромид натрия | 1) SO2 2)Na2SO4 3)CaSO4•2H2O 4) Na2SO3 5) CuSO4•5H2O 6)NaBr 7)NaBr2 8)HF |
В2. Для водорода верны следующие утверждения:
1) молекула образуется по типу неполярной ковалентной химической связи
2) атомы водорода в молекуле соединены двойной связью
3) является газом (н.у.), легче воздуха
4) восстанавливает медь из оксида
5) с металлами проявляет степень окисления -1
С.1.Дана схема превращений: Na→NaOH→Na2SO4→BaSO4
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. В первом превращении укажите окислитель и восстановитель. Для третьего превращения составьте полное и сокращённое ионное уравнение.
С2. Вычислите относительную плотность хлора по водороду и воздуху
Каждый ответ части А – 2 балла
части Б — 4 балла
части С — 6 баллов Итого30 баллов
36-61% -оценка»3»
62-85%- оценка «4»
86-100% — оценка «5»
Административный тест по химии в 9 классе за I-ое полугодие (II вариант)
А1. Как изменяются восстановительные свойства в ряду элементов:
O→ S→ Se→T?
1) ослабевают
2) не изменяются
3) усиливаются
4) сначала усиливаются, а потом ослабевают
А2. Укажите электронную формулу атома хлора
1S22S22P5
1S22S22P63S23P5
1S22S22P63S23P6
1S22S22P63S23P7
А3. Свойства какого вещества описаны в тексте: «… — газ, не имеющий цвета, запаха, мало растворим в воде, при t= — 183° превращается в жидкость бледно-синего цвета, сильный окислитель, самый распространённый элемент в природе.
водород
кислород
3) озон
4) азот
А4. В лаборатории имеются растворы реактивов: фенолфталеин, хлорид бария, гидроксид натрия, нитрат серебра, метилоранж, гидроксид кальция, нитрат калия, лакмус. Для установления качественного состава серной кислоты необходимо воспользоваться реактивами:
лакмус и нитрат калия
фенолфталеин и гидроксид кальция
3) метилоранж и хлорид бария
4) гидроксид натрия и нитрат серебра
А5. Какой вид химической связи в молекуле хлорида алюминия?
1) ионная
2) ковалентная полярная
3) ковалентная неполярная
4) металлическая
В1. Установите соответствие:
Химическая формула | |
А) Соляная кислота Б) Сульфид калия В) Оксид железа (III) Г) Глауберова соль Д) Фторид кальция | 1)K2S 2)Na2SO4•10 H2O 3)CaSO4•2H2O 4)СаF2 5) K2SO3 6)Fe2O3 7)HСl 8)СаF |
В 2. Для серной кислоты верны следующие утверждения:
1) в молекуле степень окисления серы равна -2
2) нельзя воду приливать к концентрированной кислоте
3) тяжёлая бесцветная маслянистая жидкость, поглощает влагу
4) концентрированная кислота обугливает сахар, бумагу, дерево
5) разбавленная кислота взаимодействует с медью
С1. Дана схема превращений: Zn→ZnCl2→Zn(OH)2→ZnO
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. В первом превращении укажите окислитель и восстановитель. Для второго превращения составьте полное и сокращённое ионное уравнение.
С.2 Вычислите массовую долю серы в сульфате магния
Каждый ответ части А – 2 балла
части Б — 4 балла
части С — 6 баллов Итого30 баллов
36-61% -оценка»3»
62-85%- оценка «4»
86-100% — оценка «5»
Источник
Выберите два высказывания, в которых говорится о кремнии как о простом веществе.
- Массовая доля кремния в земной коре превышает 25%.
- Кремний обладает полупроводниковыми свойствами.
- Кремний не растворяется в воде.
- Кремний входит в состав слюды и полевого шпата.
- При переломах костей содержание кремния в месте перелома возрастает почти в 50 раз.
Запишите в поле для ответа номера выбранных высказываний.
Это задание решали 13 тыс. раз. С ним справились 34% пользователей.
Выберите два высказывания, в которых говорится о калии как о химическом
элементе.
- Воспламенившийся калий тушат содой или поваренной солью.
- Калий используют как катализатор при производстве некоторых видов синтетического каучука.
- При недостатке калия семена теряют всхожесть.
- Инертный газ – единственная безопасная для калия среда.
- Калий содержится в крови и цитоплазме клеток.
Запишите номера выбранных ответов.
Это задание решали 8 тыс. раз. С ним справились 32% пользователей.
Выберите два высказывания, в которых говорится о фосфоре как о простом веществе.
- На долю фосфора приходится 0,08% массы земной коры.
- Красный фосфор не растворяется в сероуглероде.
- Фосфор входит в состав нуклеиновых кислот.
- Фосфорит – основа для получения фосфора при восстановлении углём.
- Многоликость фосфора – это его способность находиться в нескольких аллотропных модификациях.
В ответе укажите номера выбранных вариантов без пробелов и запятых.
Это задание решали 6 тыс. раз. С ним справились 30% пользователей.
Выберите два высказывания, в которых говорится о натрии как о химическом элементе.
- Натрий хорошо проводит тепло.
- Известны шесть радиоактивных изотопов натрия.
- Натрий входит в состав галита.
- С помощью амальгамы натрия можно определить содержание влаги в пробе органического вещества.
- При окислении натрия в сухом воздухе образуется перекись.
В ответе укажите номера выбранных вариантов без пробелов и запятых.
Это задание решали 5 тыс. раз. С ним справились 36% пользователей.
Выберите два высказывания, в которых говорится о ртути как о химическом элементе.
- Ртуть входит в состав оксида ртути.
- В воздухе были обнаружены пары ртути.
- Из разбитого градусника вылилась ртуть.
- Киноварь – рудный минерал, содержащий ртуть.
- Как проводник ртуть используется в переключателях света.
Запишите в поле для ответа цифры, соответствующие выбранным вариантам.
Это задание решали 5 тыс. раз. С ним справились 56% пользователей.
Выберите два высказывания, в которых говорится о кислороде как
о химическом элементе.
- Кислород плохо растворяется в воде.
- Кислород не имеет запаха.
- Кислород входит в состав воды.
- Кислород входит в состав воздуха.
- Кислород образует несколько аллотропных модификаций.
Запишите в поле ответа номера выбранных высказываний.
Это задание решали 5 тыс. раз. С ним справились 29% пользователей.
Выберите два высказывания, в которых говорится о железе как о химическом элементе.
- Железо реагирует с хлором.
- Железо быстро ржавеет во влажном воздухе.
- Пирит является сырьём для получения железа.
- Гемоглобин, содержащий железо, переносит кислород.
- В состав ржавчины входит железо.
Запишите в поле ответа номера выбранных высказываний без пробелов.
Это задание решали 24 тыс. раз. С ним справились 26% пользователей.
Источник
«Вещества и их свойства. Чистые вещества и смеси»
Ключевые слова конспекта: предмет химии, вещества и их свойства, чистые вещества и смеси, способо разделения смесей.
Химия – это наука о веществах, их свойствах, превращениях веществ и явлениях, сопровождающих эти превращения. Химия является одной из наук, изучающих природу. Вместе с биологией и физикой химия принадлежит к числу естественных наук.
Вещество — это то, из чего состоит физическое тело. Вещество характеризуется определенными физическими свойствами.
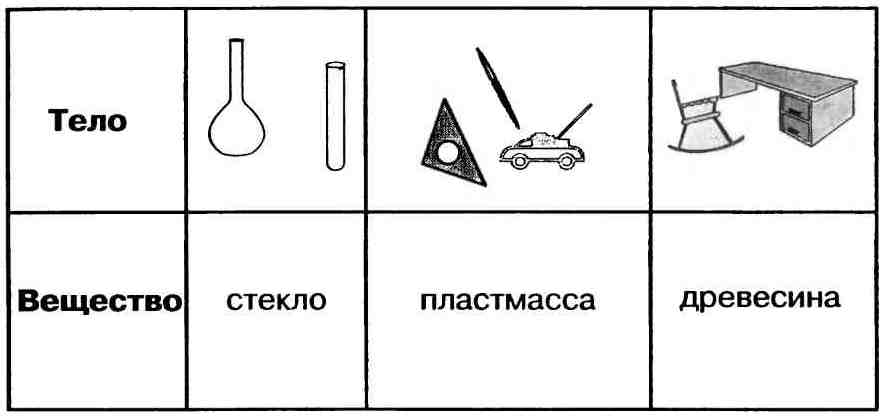
Свойства веществ — это признаки, по которым вещества отличаются друг от друга или сходны между собой, например:
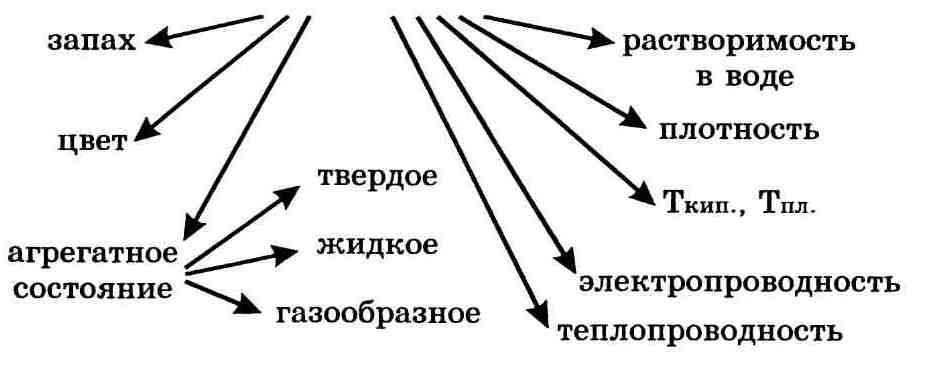
Важнейшие физические свойства вещества следующие: агрегатное состояние, цвет, запах, плотность, растворимость в воде, тепло-и электропроводность, температуры плавления и кипения.
Например, всем известное вещество алюминий можно охарактеризовать так: Алюминий — металл серебристо-белого цвета, сравнительно лёгкий (р = 2,7 г/см3), плавится при температуре 600°С. Алюминий очень пластичен. По электрической проводимости уступает лишь золоту, серебру и меди. Из-за лёгкости алюминий в виде сплавов широко используют в самолёто- и ракетостроении. Его также используют для изготовления электрических проводов и предметов быта.
Чистые вещества и смеси
Чистыми называются вещества, состоящие из одинаковых молекул. Смесь состоит из молекул разных веществ.
Каждое вещество имеет прежде всего свои, характерные именно для него свойства. Они в наибольшей степени проявляются, только если вещество является практически чистым, т. е. содержит мало примесей.
В природе чистых веществ не бывает, они встречаются преимущественно в виде смесей. Во многих случаях смеси нелегко отличить от чистых веществ. Например, сахар, растворяясь в воде, образует однородную по внешнему виду смесь. Даже с помощью микроскопа нельзя обнаружить частицы веществ, входящих в эту смесь. Такие смеси называют гомогенными (однородными).
Молоко на первый взгляд тоже кажется однородным веществом. Однако, если рассмотреть каплю молока под микроскопом, можно увидеть, что в ней плавает множество мельчайших капелек жира. Если дать молоку постоять, то эти капельки соберутся в верхнем слое, образуя сливки. Подобные неоднородные смеси называют гетерогенными смесями.
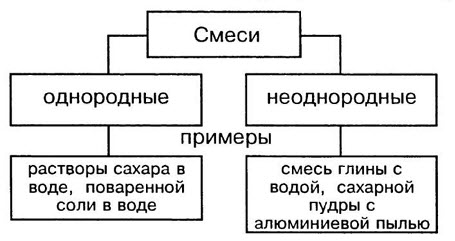
Однородные смеси — это смеси, в которых даже с помощью микроскопа нельзя обнаружить частицы веществ, входящих в смесь. Неоднородные смеси — это смеси, в которых невооруженным глазом или с помощью микроскопа можно заметить частицы веществ,составляющие смесь.
Способ разделения смесей
В смеси сохраняются свойства составляющих их веществ компонентов. На основании этих свойств выбирают рациональный способ разделения смесей.
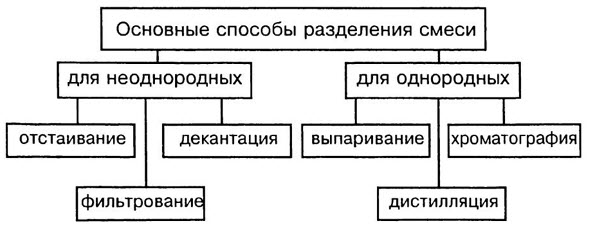
Способы разделения смесей основаны на различии свойств веществ-компонентов, их составляющих: плотности, растворимости в воде и других жидкостях-растворителях, способности плавиться и испаряться.
Способы разделения смесей: неоднородные смеси — отстаивание и фильтрование, действие магнитом; однородные смеси — перегонка, выпаривание, кристаллизация и хроматография.
Отстаивание. Прием разделения смеси твердого и жидкого вещества путем осаждения твердого на дно под действием сил тяжести.
- а) При выдерживании воды, содержащей частички глины, в емкостях глина медленно осаждается на дно, отстаивается. Применяется при очистке питьевой воды.
- б) Чтобы разделить смесь поваренной соли и речного песка, надо поместить ее в колбу и добавить воды. Соль растворится, а песок опустится на дно. Затем осторожно слить раствор, чтобы песок остался в колбе. Соль из раствора получают выпариванием воды.
- в) Для разделения смеси малорастворимых друг в друге жидкостей с различной плотностью используют делительную воронку. Это цилиндрический сосуд с краником внизу. Помещенная в эту воронку смесь бензина с водой или растительного масла с водой быстро расслаивается, причем водный слой оказывается внизу. Открывая кран, сливаем воду, а когда вода заканчивается, закрываем кран. В воронке — бензин или масло.
Фильтрование. Чтобы избавиться от нерастворимых в воде примесей, воду пропускают через фильтр. Материал фильтра — бумага, ткань, пористая керамика. Примеси остаются на фильтре, а вода очищается.
Действие магнитом. Выделение из неоднородной смеси веществ, способных к намагничиванию. К магниту притягиваются железные опилки.
Перегонка. Прием разделения однородных жидких смесей путем испарения летучих жидкостей, различающихся температурами кипения, с последующей конденсацией паров. Так из нефти, представляющей собой смесь жидких, газообразных и твердых углеводородов, получают попутные газы, бензин, керосин, дизельное топливо и другие продукты.
Выпаривание. Способ извлечения растворенного в жидком растворителе твердого или жидкого вещества. Например, упаривая воду из сладкого сиропа, получают сахар.
Кристаллизация. Избирательное извлечение одного из нескольких твердых веществ, содержащихся в растворе. Частичное упаривание воды с последующим охлаждением раствора приводит к осаждению кристаллов главного компонента. Так из морской воды выделяют поваренную соль NaCl, а другие соли, присутствующие в меньшем количестве, остаются в растворе.
Хроматография. Метод разделения смесей, основанный на различиях относительной растворимости веществ в используемом растворителе (жидкая фаза) и прочности связывания этих веществ поверхностью сорбента (твердая фаза).
Бумажная хроматография. Нанесем каплю раствора смеси двух веществ на расстоянии 2 см от края длинной полоски фильтровальной бумаги. Подвесим полоску в стеклянном цилиндре, на дне которого находится растворитель. Нижнюю часть полоски погрузим в растворитель, при этом пятно со смесью находится чуть выше. Верхняя часть полоски удерживается проволокой у отверстия цилиндра. Сверху цилиндр закроем стеклом, чтобы не испарялся растворитель. Боковые стороны полоски не касаются стенок цилиндра. Растворитель смачивает полоску, и жидкий фронт движется вверх за счет капиллярных сил. Вместе с растворителем по бумаге движутся и растворенные вещества. Если они цветные, то за движением можно наблюдать визуально. Вещество, которое лучше растворимо и менее прочно удерживается сорбентом (бумагой), поднимется выше. Когда фронт поднимется достаточно высоко и пятна разделятся, полоску вынимают и разрезают.
Колоночная хроматография — процесс, родственный рассмотренному. В качестве твердой фазы служит силикагель, помещенный в колонку. Только в этом случае смесь наносят равномерно вверху колонки, а потом добавляют растворитель. Разделенные вещества собирают внизу в разные стаканчики.
Конспект урока «Вещества и их свойства. Чистые вещества и смеси».
Следующая тема: «Физические и химические явления».
Источник
