Укажите какой оксид обладает более основными свойствами

Оксиды – сложные вещества, состоящие из двух элементов, одним из которых является кислород. Оксиды могут быть солеобразующими и несолеобразующими: одним из видов солеобразующих оксидов являются основные оксиды. Чем они отличаются от других видов, и каковы их химические свойства?

Классификация оксидов
Солеобразующие оксиды подразделяются на основные, кислотные и амфотерные оксиды. Если основным оксидам соответствуют основания, то кислотным – кислоты, а амфотерным оксидам соответствуют амфотерные образования. Амфотерными оксидами называют такие соединения, которые в зависимости от условий могут проявлять либо основные, либо кислотные свойства.
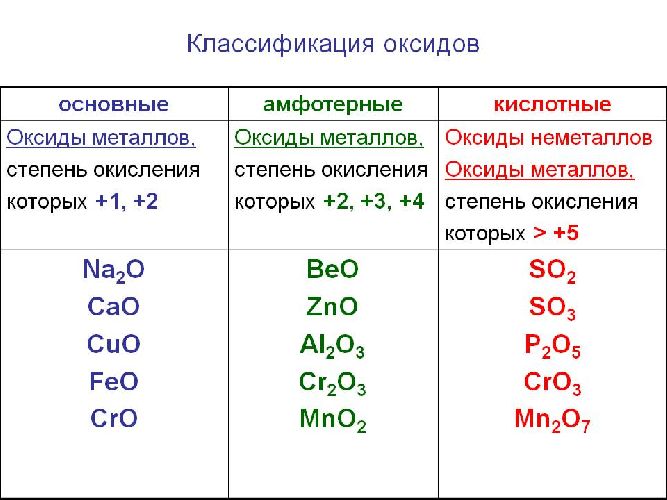
Рис. 1. Классификация оксидов.
Физические свойства оксидов очень разнообразны. Они могут быть как газами (CO2), так и твердыми (Fe2O3) или жидкими веществами (H2O).
При этом большинство основных оксидов является твердыми веществами различных цветов.
оксиды, в которых элементы проявляют свою высшую активность называются высшими оксидами. Порядок возрастания кислотных свойств высших оксидов соответствующих элементов в периодах слева направо объясняется постепенным возрастанием положительного заряда ионов этих элементов.
Химические свойства основных оксидов
Основными оксидами называются оксиды, которым соответствуют основания. Например, основным оксидам K2O, СaO соответствуют основания KOH, Ca(OH)2 .

Рис. 2. Основные оксиды и соответствующие им основания.
Основные оксиды образуются типичными металлами, а также металлами переменной валентности в низшей степени окисления (например, CaO, FeO), реагируют с кислотами и кислотными оксидами, образуя при этом соли:
CaO (основной оксид)+CO2 (кислотный оксид)=СaCO3 (соль)
FeO (основной оксид)+H2 SO4 (кислота)=FeSO4 (соль)+2H2O (вода)
Основные оксиды также взаимодействуют с амфотерными оксидами, в результате чего происходит образование соли, например:
CaO+ZnO=CaZnO2
С водой реагируют только оксиды щелочных и щелочно-земельных металлов:
BaO (основной оксид)+H2O (вода)=Ba(OH)2 (основание щелочнозем. металла)
Многие основные оксиды имеют характер восстанавливаться до веществ, состоящих из атомов одного химического элемента:
3CuO+2NH3 =3Cu+3H2 O+N2
При нагревании разлагаются только оксиды ртути и благородных металлов:
2AU2O=4Au+O2
2HgO=2Hg+O2

Рис. 3. Оксид ртути.
Список основных оксидов:
| Название оксида | Химическая формула | Свойства |
| Оксид кальция | CaO | негашенная известь, белое кристаллическое вещество |
| Оксид магния | MgO | белое вещество, малорастворимое в воде |
| Оксид бария | BaO | бесцветные кристаллы с кубической решеткой |
| Оксид меди II | CuO | вещество черного цвета практически нерастворимое в воде |
| Оксид ртути II | HgO | твердое вещество красного или желто-оранжевого цвета |
| Оксид калия | K2O | бесцветное или бледно-желтое вещество |
| Оксид натрия | Na2O | вещество, состоящее из бесцветных кристаллов |
| Оксид лития | Li2 O | вещество, состоящее из бесцветных кристаллов, которые имеют строение кубической решетки |
В главных подгруппах периодической системы при переходе от одного элемента к другому сверху вниз наблюдается усиление основных свойств оксидов
Что мы узнали?
При образовании основных оксидов одним из обязательных элементов является кислород.Основные оксиды обладают рядом физических и химических свойств, таких как взаимодействие с водой, кислотами и другими оксидами.
Тест по теме
Оценка доклада
Средняя оценка: 4.6. Всего получено оценок: 1017.
Источник
Оксидами называются сложные вещества, в состав молекул которых входят атомы кислорода в степни окисления – 2 и какого-нибудь другого элемента.
 Оксиды могут быть получены при непосредственном взаимодействии кислорода с другим элементом, так и косвенным путём (например, при разложении солей, оснований, кислот). В обычных условиях оксиды бывают в твёрдом, жидком и газообразном состоянии, этот тип соединений весьма распространён в природе. Оксиды содержатся в Земной коре. Ржавчина, песок, вода, углекислый газ – это оксиды.
Оксиды могут быть получены при непосредственном взаимодействии кислорода с другим элементом, так и косвенным путём (например, при разложении солей, оснований, кислот). В обычных условиях оксиды бывают в твёрдом, жидком и газообразном состоянии, этот тип соединений весьма распространён в природе. Оксиды содержатся в Земной коре. Ржавчина, песок, вода, углекислый газ – это оксиды.
Они бывают солеобразующими и несолеобразующие.
Солеобразующие оксиды – это такие оксиды, которые в результате химических реакций образуют соли. Это оксиды металлов и неметаллов, которые при взаимодействии с водой образуют соответствующие кислоты, а при взаимодействии с основаниями – соответствующие кислые и нормальные соли. Например, оксид меди (CuO) является оксидом солеобразующим, потому что, например, при взаимодействии её с соляной кислотой (HCl) образуется соль:
CuO + 2HCl → CuCl2 + H2O.
В результате химических реакций можно получать и другие соли:
CuO + SO3 → CuSO4.
Несолеобразующими оксидами называются такие оксиды, которые не образуют солей. Примером могут служить СО, N2O, NO.
Солеобразующие оксиды в свою очередь бывают 3-х типов: основными (от слова «основание»), кислотными и амфотерными.
Основными оксидами называются такие оксиды металлов, которым соответствуют гидроксиды, относящиеся к классу оснований. К основным оксидам относятся, например, Na2O, K2O, MgO, CaO и т.д.
 Химические свойства основных оксидов
Химические свойства основных оксидов
1. Растворимые в воде основные оксиды вступают в реакцию с водой, образуя основания:
Na2O + H2O → 2NaOH.
2. Взаимодействуют с кислотными оксидами, образуя соответствующие соли
Na2O + SO3 → Na2SO4.
3. Реагируют с кислотами, образуя соль и воду:
CuO + H2SO4 → CuSO4 + H2O.
4. Реагируют с амфотерными оксидами:
Li2O + Al2O3 → 2LiAlO2.
Если в составе оксидов в качестве второго элемента будет неметалл или металл, проявляющий высшую валентность (обычно проявляют от IV до VII), то такие оксиды будут кислотными. Кислотными оксидами (ангидридами кислот) называются такие оксиды, которым соответствуют гидроксиды, относящие к классу кислот. Это, например, CO2, SO3, P2O5, N2O3, Cl2O5, Mn2O7 и т.д. Кислотные оксиды растворяются в воде и щелочах, образуя при этом соль и воду.
Химические свойства кислотных оксидов
1. Взаимодействуют с водой, образуя кислоту:
SO3 + H2O → H2SO4.
Но не все кислотные оксиды непосредственно реагируют с водой (SiO2 и др.).
2. Реагируют с основанными оксидами с образованием соли:
CO2 + CaO → CaCO3
3. Взаимодействуют со щелочами, образуя соль и воду:
CO2 + Ba(OH)2 → BaCO3 + H2O.
В состав амфотерного оксида входит элемент, который обладает амфотерными свойствами. Под амфотерностью понимают способность соединений проявлять в зависимости от условий кислотные и основные свойства. Например, оксид цинка ZnO может быть как основанием, так и кислотой (Zn(OH)2 и H2ZnO2). Амфотерность выражается в том, что в зависимости от условий амфотерные оксиды проявляют либо осно́вные, либо кислотные свойства.
Химические свойства амфотерных оксидов
1. Взаимодействуют с кислотами, образуя соль и воду:
ZnO + 2HCl → ZnCl2 + H2O.
2. Реагируют с твёрдыми щелочами (при сплавлении), образуя в результате реакции соль – цинкат натрия и воду:
ZnO + 2NaOH → Na2 ZnO2 + H2O.
При взаимодействии оксида цинка с раствором щелочи (того же NaOH) протекает другая реакция:
ZnO + 2 NaOH + H2O => Na2[Zn(OH)4].
Координационное число – характеристика, которая определяет число ближайших частиц: атомов или инов в молекуле или кристалле. Для каждого амфотерного металла характерно свое координационное число. Для Be и Zn – это 4; Для и Al – это 4 или 6; Для и Cr – это 6 или (очень редко) 4;
Амфотерные оксиды обычно не растворяются в воде и не реагируют с ней.
Остались вопросы? Хотите знать больше об оксидах?
Чтобы получить помощь репетитора – зарегистрируйтесь.
Первый урок – бесплатно!
Зарегистрироваться
© blog.tutoronline.ru,
при полном или частичном копировании материала ссылка на первоисточник обязательна.
Источник
Сегодня мы начинаем
знакомство с важнейшими классами неорганических соединений. Неорганические
вещества по составу делятся, как вы уже знаете, на простые и сложные.

ОКСИД | КИСЛОТА | ОСНОВАНИЕ | СОЛЬ |
ЭхОу | НnA А | Ме(ОН)b ОН | MenAb |
Сложные неорганические
вещества подразделяют на четыре класса: оксиды, кислоты, основания, соли. Мы
начинаем с класса оксидов.
ОКСИДЫ
Оксиды
– это сложные вещества, состоящие из двух химических элементов, один из которых
кислород, с валентность равной 2. Лишь один химический элемент – фтор,
соединяясь с кислородом, образует не оксид, а фторид кислорода OF2.
Называются они просто – “оксид + название элемента” (см. таблицу). Если
валентность химического элемента переменная, то указывается римской цифрой,
заключённой в круглые скобки, после названия химического элемента.
Формула | Название | Формула | Название |
CO | оксид | Fe2O3 | оксид |
NO | оксид | CrO3 | оксид |
Al2O3 | оксид | ZnO | оксид |
N2O5 | оксид | Mn2O7 | оксид |
Классификация
оксидов
Все
оксиды можно разделить на две группы: солеобразующие (основные, кислотные, амфотерные)
и несолеобразующие или безразличные.

Оксиды металлов МехОу | Оксиды | |||
Основные | Кислотные | Амфотерные | Кислотные | Безразличные |
I, II Ме | V-VII Me | ZnO,BeO,Al2O3, Fe2O3, Cr2O3 | >II неМе | I, II неМе CO, NO, N2O |
1). Основные оксиды – это оксиды, которым
соответствуют основания. К основным оксидам относятся оксиды металлов
1 и 2 групп, а также металлов побочных подгрупп с валентностью I и II
(кроме ZnO
–
оксид цинка и BeO – оксид берилия):

2). Кислотные оксиды – это оксиды, которым
соответствуют кислоты. К кислотным оксидам относятся оксиды неметаллов (кроме
несолеобразующих – безразличных), а также оксиды металлов побочных подгрупп с
валентностью от V
до VII (Например, CrO3-оксид
хрома (VI), Mn 2O7 – оксид марганца (VII)):

3). Амфотерные
оксиды – это оксиды, которым соответствуют основания и кислоты. К ним
относятся оксиды металлов главных и побочных подгрупп с валентностью III, иногда IV,
а также цинк и бериллий (Например, BeO, ZnO, Al2O3, Cr2O3).
4). Несолеобразующие оксиды – это оксиды
безразличные к кислотам и основаниям. К ним относятся оксиды неметаллов с валентностью I и II
(Например,N2O, NO, CO).
Вывод: характер свойств оксидов в первую очередь
зависит от валентности элемента.
Например,
оксиды хрома:
CrO
(II
– основный);
Cr
2O3 (III – амфотерный);
CrO3
(VII
– кислотный).
Классификация оксидов
(по растворимости в воде)
Кислотные оксиды | Основные оксиды | Амфотерные оксиды |
Растворимы в воде. Исключение –SiO2 (не | В воде растворяются только оксиды щелочных и (это металлы I «А» и II «А» групп, исключение Be ,Mg) | С водой не взаимодействуют. В воде не растворимы |
Выполните задания:
1. Выпишите отдельно химические формулы солеобразующих кислотных и основных оксидов.
NaOH, AlCl3, K2O, H2SO4, SO3, P2O5, HNO3, CaO, CO.
2. Даны вещества: CaO, NaOH, CO2, H2SO3, CaCl2, FeCl3, Zn(OH)2, N2O5, Al2O3, Ca(OH)2, N2O, FeO, SO3, Na2SO4, ZnO, CaCO3, Mn2O7, CuO, KOH, CO, Fe(OH)3
Выпишите оксиды и классифицируйте их.
Получение
оксидов
Тренажёр “Взаимодействие кислорода с простыми веществами”
1. | а) Тренажёр “Взаимодействие | 2Mg |
б) | 2H2S+3O2=2H2O+2SO2 | |
2.Разложение (используйте таблицу кислот, см. приложения) | а) СОЛЬt= | СaCO3=CaO+CO2 |
б) Нерастворимых Ме(ОН)bt= MexOy+ H2O | Cu (OH)2 t=CuO+H2O | |
в) НnA = КИСЛОТНЫЙ | H2SO3=H2O+SO2 |
Физические
свойства оксидов
При комнатной температуре большинство оксидов –
твердые вещества (СаО, Fe2O3 и др.), некоторые – жидкости
(Н2О, Сl2О7 и др.) и газы (NO, SO2
и др.).



Химические
свойства оксидов
ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВНЫХ ОКСИДОВ 1. CaO + SO2 = CaSO3 2. 3K2O + 2H3PO4 = 2K3PO4 + 3H2O 3. Основной оксид + Вода = Щёлочь Na2O + H2O = 2NaOH |
ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТНЫХ ОКСИДОВ 1. СO2 + H2O = H2CO3, SiO2 – не реагирует 2. P2O5 + 6KOH = 2K3PO4 + 3H2O 3. CaO + SO2 = CaSO3 4. CaCO3 + |
ХИМИЧЕСКИЕ СВОЙСТВА АМФОТЕРНЫХ ОКСИДОВ Взаимодействуют ZnO + 2 HCl = ZnCl2 + H2O ZnO + 2 NaOH + H2O = Na2[Zn(OH)4] ZnO + 2 NaOH = Na2ZnO2 + H2O |
Применение
оксидов
Некоторые
оксиды не растворяются в воде, но многие вступают с водой в реакции соединения:
SO3 + H2O
= H2SO4
CaO + H2O = Ca(OH)2
В
результате часто получаются очень нужные и полезные соединения. Например, H2SO4
– серная кислота, Са(ОН)2 – гашеная известь и т.д.
Если
оксиды нерастворимы в воде, то люди умело используют и это их свойство.
Например, оксид цинка ZnO – вещество белого цвета, поэтому используется для
приготовления белой масляной краски (цинковые белила). Поскольку ZnO
практически не растворим в воде, то цинковыми белилами можно красить любые
поверхности, в том числе и те, которые подвергаются воздействию атмосферных
осадков. Нерастворимость и неядовитость позволяют использовать этот оксид при
изготовлении косметических кремов, пудры. Фармацевты делают из него вяжущий и
подсушивающий порошок для наружного применения.
Такими
же ценными свойствами обладает оксид титана (IV) – TiO2. Он тоже
имеет красивый белый цвет и применяется для изготовления титановых белил. TiO2
не растворяется не только в воде, но и в кислотах, поэтому покрытия из этого
оксида особенно устойчивы. Этот оксид добавляют в пластмассу для придания ей
белого цвета. Он входит в состав эмалей для металлической и керамической
посуды.
Оксид
хрома (III) – Cr2O3 – очень прочные кристаллы
темно-зеленого цвета, не растворимые в воде. Cr2O3
используют как пигмент (краску) при изготовлении декоративного зеленого стекла
и керамики. Известная многим паста ГОИ (сокращение от наименования
“Государственный оптический институт”) применяется для шлифовки и полировки
оптики, металлических
изделий, в ювелирном
деле.

Благодаря
нерастворимости и прочности оксида хрома (III) его используют и в
полиграфических красках (например, для окраски денежных купюр). Вообще, оксиды
многих металлов применяются в качестве пигментов для самых разнообразных
красок, хотя это – далеко не единственное их применение.
Задания для закрепления
1. Закончите УХР, укажите тип реакции, назовите
продукты реакции
Na2O + H2O
=
N2O5
+ H2O =
CaO + HNO3
=
NaOH + P2O5
=
K2O + CO2
=
Cu(OH)2 = ?
+ ?
2. Осуществите превращения по схеме:
1) K→K2O→KOH→K2SO4
2) S→SO2→H2SO3→Na2SO3
3) P→P2O5→H3PO4→K3PO4
Источник
Оксиды — это сложные вещества, состоящие из атомов двух элементов, один из которых — кислород со степенью окисления -2. При этом кислород связан только с менее электроотрицательным элементом.
В зависимости от второго элемента оксиды проявляют разные химические свойства. В школьном курсе оксиды традиционно делят на солеобразующие и несолеобразующие. Некоторые оксиды относят к солеобразным (двойным).
Двойные оксиды — это некоторые оксиды , образованные элементом с разными степенями окисления.
Солеобразующие оксиды делят на основные, амфотерные и кислотные.
Основные оксиды — это оксиды, обладающие характерными основными свойствами. К ним относят оксиды, образованные атомами металлов со степень окисления +1 и +2.
Кислотные оксиды — это оксиды, характеризующиеся кислотными свойствами. К ним относят оксиды, образованные атомами металлов со степенью окисления +5, +6 и +7, а также атомами неметаллов.
Амфотерные оксиды — это оксиды, характеризующиеся и основными, и кислотными свойствами. Это оксиды металлов со степенью окисления +3 и +4, а также четыре оксида со степенью окисления +2: ZnO, PbO, SnO и BeO.
Несолеобразующие оксиды не проявляют характерных основных или кислотных свойств, им не соответствуют гидроксиды. К несолеобразующим относят четыре оксида: CO, NO, N2O и SiO.
Классификация оксидов

Тренировочные тесты по теме Классификация оксидов.
Получение оксидов
Общие способы получения оксидов:
1. Взаимодействие простых веществ с кислородом:
1.1. Окисление металлов: большинство металлов окисляются кислородом до оксидов с устойчивыми степенями окисления.
Например, алюминий взаимодействует с кислородом с образованием оксида:
4Al + 3O2 → 2Al2O3
Не взаимодействуют с кислородом золото, платина, палладий.
Натрий при окислении кислородом воздуха образует преимущественно пероксид Na2O2,
2Na + O2 → 2Na2O2
Калий, цезий, рубидий образуют преимущественно пероксиды состава MeO2:
K + O2 → KO2
Примечания: металлы с переменной степенью окисления окисляются кислородом воздуха, как правило, до промежуточной степени окисления (+3):
4Fe + 3O2 → 2Fe2O3
4Cr + 3O2 → 2Cr2O3
Железо также горит с образованием железной окалины — оксида железа (II, III):
3Fe + 2O2 → Fe3O4
1.2. Окисление простых веществ-неметаллов.
Как правило, при окислении неметаллов образуется оксид неметалла с высшей степенью окисления, если кислород в избытке, или оксид неметалла с промежуточной степенью окисления, если кислород в недостатке.
Например, фосфор окисляется избытком кислорода до оксида фосфора (V), а под действием недостатка кислорода до оксида фосфора (III):
4P + 5O2(изб.) → 2P2O5
4P + 3O2(нед.) → 2P2O3
Но есть некоторые исключения.
Например, сера сгорает только до оксида серы (IV):
S + O2 → SO2
Оксид серы (VI) можно получить только окислением оксида серы (IV) в жестких условиях в присутствии катализатора:
2SO2 + O2 = 2SO3
Азот окисляется кислородом только при очень высокой температуре (около 2000оС), либо под действием электрического разряда, и только до оксида азота (II):
N2 + O2 = 2NO
Не окисляется кислородом фтор F2 (сам фтор окисляет кислород). Не взаимодействуют с кислородом прочие галогены (хлор Cl2, бром и др.), инертные газы (гелий He, неон, аргон, криптон).
2. Окисление сложных веществ (бинарных соединений): сульфидов, гидридов, фосфидов и т.д.
При окислении кислородом сложных веществ, состоящих, как правило, из двух элементов, образуется смесь оксидов этих элементов в устойчивых степенях окисления.
Например, при сжигании пирита FeS2 образуются оксид железа (III) и оксид серы (IV):
4FeS2 + 11O2 → 2Fe2O3 + 8SO2
Сероводород горит с образованием оксида серы (IV) при избытке кислорода и с образованием серы при недостатке кислорода:
2H2S + 3O2(изб.) → 2H2O + 2SO2
2H2S + O2(нед.) → 2H2O + 2S
А вот аммиак горит с образованием простого вещества N2, т.к. азот реагирует с кислородом только в жестких условиях:
4NH3 + 3O2 →2N2 + 6H2O
А вот в присутствии катализатора аммиак окисляется кислородом до оксида азота (II):
4NH3 + 5O2 → 4NO + 6H2O
3. Разложение гидроксидов. Оксиды можно получить также из гидроксидов — кислот или оснований. Некоторые гидроксиды неустойчивы, и самопроизвольную распадаются на оксид и воду; для разложения некоторых других (как правило, нерастворимых в воде) гидроксидов необходимо их нагревать (прокаливать).
гидроксид → оксид + вода
Самопроизвольно разлагаются в водном растворе угольная кислота, сернистая кислота, гидроксид аммония, гидроксиды серебра (I), меди (I):
H2CO3 → H2O + CO2
H2SO3 → H2O + SO2
NH4OH → NH3 + H2O
2AgOH → Ag2O + H2O
2CuOH → Cu2O + H2O
При нагревании разлагаются на оксиды большинство нерастворимых гидроксидов — кремниевая кислота, гидроксиды тяжелых металлов — гидроксид железа (III) и др.:
H2SiO3 → H2O + SiO2
2Fe(OH)3 → Fe2O3 + 3H2O
4. Еще один способ получения оксидов — разложение сложных соединений — солей.
Например, нерастворимые карбонаты и карбонат лития при нагревании разлагаются на оксиды:
Li2CO3 → CO2 + Li2O
CaCO3 → CaO + CO2
Соли, образованные сильными кислотами-окислителями (нитраты, сульфаты, перхлораты и др.), при нагревании, как правило, разлагаются с с изменением степени окисления:
2Zn(NO3)2 → 2ZnO + 4NO2 + O2
Более подробно про разложение нитратов можно прочитать в статье Окислительно-восстановительные реакции.
Химические свойства оксидов
Значительная часть химических свойств оксидов описывается схемой взаимосвязи основных классов неорганических веществ.
Химические свойства основных оксидов
Подробно про химические свойства оксидов можно прочитать в соответствующих статьях:
Химические свойства основных оксидов.
Химические свойства кислотных оксидов.
Химические свойства амфотерных оксидов.
Источник
