В каких веществах содержится водород


- Обозначение – H (Hydrogen);
- Латинское название – Hydrogenium;
- Период – I;
- Группа – 1 (Ia);
- Атомная масса – 1,00794;
- Атомный номер – 1;
- Радиус атома = 53 пм;
- Ковалентный радиус = 32 пм;
- Распределение электронов – 1s1;
- t плавления = -259,14°C;
- t кипения = -252,87°C;
- Электроотрицательность (по Полингу/по Алпреду и Рохову) = 2,02/-;
- Степень окисления: +1; 0; -1;
- Плотность (н. у.) = 0,0000899 г/см3;
- Молярный объем = 14,1 см3/моль.
Бинарные соединения водорода с кислородом:
- Вода (H2O)
- Пероксид водорода (H2O2)
Водород (“рождающий воду”) был открыт английским ученым Г. Кавендишем в 1766 году. Это самый простой элемент в природе – атом водорода имеет ядро и один электрон, наверное, по этой причине водород является самым распространенным элементом во Вселенной (составляет более половины массы большинства звезд).
Про водород можно сказать, что “мал золотник, да дорог”. Несмотря на свою “простоту”, водород дает энергию всем живым существам на Земле – на Солнце идет непрерывная термоядерная реакция в ходе которой из четырех атомов водорода образуется один атом гелия, данный процесс сопровождается выделением колоссального количества энергии (подробнее см. Ядерный синтез).
В земной коре массовая доля водорода составляет всего 0,15%. Между тем, подавляющее число (95%) всех известных на Земле химических веществ содержат один или несколько атомов водорода.
Водород “открывает” Периодическую таблицу химических элементов Д. И. Менделеева, находясь в левом верхнем углу таблицы под почетным номером “1”.
Главная особенность водорода, отличающая его от остальных элементов Периодической системы, заключается в том, что он “сидит” сразу на двух стульях, – в I и VII группах (в главных подгруппах). Такое “двуличие” водорода объясняется тем, что он имеет много общего, как с щелочными металлами, так и с галогенами. Атом водорода, как и атомы щелочных металлов, может окисляться, превращаясь в катион H+. С другой стороны, как и галогены, атом водорода может присоединять 1 электрон, проявляя свойства восстановителя, превращаясь в гидрид-ион H-.
Водород в ряду электроотрицательности находится аккурат между типичными металлами и типичными неметаллами (электроотрицательность водорода равна 2,1).
Стабильные изотопы водорода:
- протий (1H) – легкий водород, составляет 99,985%;
- дейтерий (2H) – тяжелый водород, 0,015%;
- тритий (3H) – на Земле содержится около 2 кг.
Строение атома водорода проще не придумаешь – вокруг ядра, состоящего из одного протона (заряд +1), вращается по единственной s-орбитали один электрон (см. Электронная структура атомов).
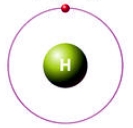
В соединениях с неметаллами (HCl, H2O, CH4…) водород отдает свой единственный электрон более электроотрицательным элементам, проявляя степень окисления +1 (чаще), образуя только ковалентные связи (см. Ковалентная связь).
В соединениях с металлами (NaH, CaH2…) водород, наоборот, принимает на свою единственную s-орбиталь еще один электрон, пытаясь, таким образом, завершить свой электронный слой, проявляя степень окисления -1 (реже), образуя чаще ионную связь (см. Ионная связь), т. к., разность в электроотрицательности атома водорода и атома металла может быть достаточно большой.
H2
В газообразном состоянии водород находится в виде двухатомных молекул, образуя неполярную ковалентную связь.
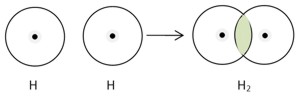
Молекулы водорода обладают:
- большой подвижностью;
- большой прочностью;
- малой поляризуемостью;
- малыми размерами и массой.
Свойства газа водорода:
- самый легкий в природе газ, без цвета и запаха;
- плохо растворяется в воде и органических растворителях;
- в незначительных кол-вах растворяется в жидких и твердых металлах (особенно в платине и палладии);
- трудно поддается сжижению (по причине своей малой поляризуемости);
- обладает самой высокой теплопроводностью из всех известных газов;
- при нагревании реагирует со многими неметаллами, проявляя свойства восстановителя;
- при комнатной температуре реагирует со фтором (происходит взрыв): H2 + F2 = 2HF;
- с металлами реагирует с образованием гидридов, проявляя окислительные свойства: H2 + Ca = CaH2;
В соединениях водород гораздо сильнее проявляет свои восстановительные свойства, чем окислительные. Водород является самым сильным восстановителем после угля, алюминия и кальция. Восстановительные свойства водорода широко используются в промышленности для получения металлов и неметаллов (простых веществ) из оксидов и галлидов.
Fe2O3 + 3H2 = 2Fe + 3H2O
Реакции водорода с простыми веществами
Водород принимает электрон, играя роль восстановителя, в реакциях:
- с кислородом (при поджигании или в присутствии катализатора), в соотношении 2:1 (водород:кислород) образуется взрывоопасный гремучий газ:
2H20+O2 = 2H2+1O+572 кДж
- с серой (при нагревании до 150°C-300°C):
H20+S ↔ H2+1S
- с хлором (при поджигании или облучении УФ-лучами):
H20+Cl2 = 2H+1Cl
- с фтором:
H20+F2 = 2H+1F
- с азотом (при нагревании в присутствии катализаторов или при высоком давлении):
3H20+N2 ↔ 2NH3+1
Водород отдает электрон, играя роль окислителя, в реакциях с щелочными и щелочноземельными металлами с образованием гидридов металлов – солеобразные ионные соединения, содержащие гидрид-ионы H- – это нестойкие кристаллические в-ва белого цвета.
Ca+H2 = CaH2-1
2Na+H20 = 2NaH-1
Для водорода нехарактерно проявлять степень окисления -1. Реагируя с водой, гидриды разлагаются, восстанавливая воду до водорода. Реакция гидрида кальция с водой имеет следующий вид:
CaH2-1+2H2+10 = 2H20+Ca(OH)2
Реакции водорода со сложными веществами
- при высокой температуре водород восстанавливает многие оксиды металлов:
ZnO+H2 = Zn+H2O
- метиловый спирт получают в результате реакции водорода с оксидом углерода (II):
2H2+CO → CH3OH
- в реакциях гидрогенизации водород реагирует с многими органическими веществами.
Более подробно уравнения химических реакций водорода и его соединений рассмотрены на странице “Водород и его соединения – уравнения химических реакций с участием водорода”.
Применение водорода
- в атомной энергетике используются изотопы водорода – дейтерий и тритий;
- в химической промышленности водород используют для синтеза многих органических веществ, аммиака, хлороводорода;
- в пищевой промышленности водород применяют в производстве твердых жиров посредство гидрогенизации растительных масел;
- для сварки и резки металлов используют высокую температуру горения водорода в кислороде (2600°C);
- при получении некоторых металлов водород используют в качестве восстановителя (см. выше);
- поскольку водород является легким газом, его используют в воздухоплавании в качестве наполнителя воздушных шаров, аэростатов, дирижаблей;
- как топливо водород используют в смеси с СО.
В последнее время ученые уделяют достаточно много внимания поиску альтернативных источников возобновляемой энергии. Одним из перспективных направлений является “водородная” энергетика, в которой в качестве топлива используется водород, продуктом сгорания которого является обыкновенная вода.
Способы получения водорода
Промышленные способы получения водорода:
- конверсией метана (каталитическим восстановлением водяного пара) парами воды при высокой температуре (800°C) на никелевом катализаторе: CH4 + 2H2O = 4H2 + CO2;
- конверсией оксида углерода с водяным паром (t=500°C) на катализаторе Fe2O3: CO + H2O = CO2 + H2↑;
- термическим разложением метана: CH4 = C + 2H2↑;
- газификацией твердых топлив (t=1000°C): C + H2O = CO + H2↑;
- электролизом воды (очень дорогой способ при котором получается очень чистый водород): 2H2O → 2H2↑ + O2.
Лабораторные способы получения водорода:
- действием на металлы (чаще цинк) соляной или разбавленной серной кислотой: Zn + 2HCl = ZCl2 + H2; Zn + H2SO4 = ZnSO4 + H2↑;
- взаимодействием паров воды с раскаленными железными стружками: 4H2O + 3Fe = Fe3O4 + 4H2↑.
Источник
Обобщающая схема «ВОДОРОД»
I.
Водород – химический элемент
а) Положение в ПСХЭ
- порядковый номер №1
- период 1
- группа I (главная подгруппа «А»)
- относительная масса Ar(Н)=1
- латинское название Hydrogenium (рождающий
воду)
б) Распространённость водорода в
природе
Водород – химический элемент. | В земной коре (литосфера и гидросфера) – 1% по массе (10 место |
АТМОСФЕРА – 0,0001% по числу атомов | |
Самый распространённый элемент во вселенной – 92% от числа всех атомов |
Водород – химический элемент | В соединениях | Н2О – вода (11% по массе) |
СН4 – газ метан (25% по массе) | ||
Органические вещества (нефть, горючие природные газы и В организмах животных и растений (то есть в составе белков, В теле человека в среднем содержится около 7 килограммов водорода. |
в) Валентность водорода в соединениях
I Н2 ↑,
ц, з, Mr(Н2)=2,
газ легче воздуха
H2O – вода;
Н2О2 –
перекись водорода
II. Водород – простое вещество (Н2)
Получение
1.Лаборатория А) Взаимодействие металлов с кислотами: Zn + 2HCl = ZnCl2 + H2↑ соль Б) Взаимодействие активных металлов с водой: 2Na + 2H2O = 2NaOH + H2↑ |
2. · эл. ток 2H2O = · t, Ni CH4 + 2H2O = |
Нахождение
водорода в природе.
Водород широко
распространен в природе, его содержание в земной коре (литосфера и гидросфера) составляет
по массе 1%, а по числу атомов 16%. Водород входит в состав самого
распространенного вещества на Земле – воды (11,19% Водорода по массе), в состав
соединений, слагающих угли, нефть, природные газы, глины, а также организмы
животных и растений (то есть в состав белков, нуклеиновых кислот, жиров,
углеводов и других). В свободном состоянии Водород встречается крайне редко, в
небольших количествах он содержится в вулканических и других природных газах.
Ничтожные количества свободного Водорода (0,0001% по числу атомов) присутствуют
в атмосфере. В околоземном пространстве Водород в виде потока протонов образует
внутренний (“протонный”) радиационный пояс Земли. В космосе Водород
является самым распространенным элементом. В виде плазмы он составляет около
половины массы Солнца и большинства звезд, основную часть газов межзвездной
среды и газовых туманностей. Водород присутствует в атмосфере ряда планет и в
кометах в виде свободного Н2, метана СН4, аммиака NH3,
воды Н2О, радикалов. В виде потока
протонов Водород входит в состав корпускулярного излучения Солнца и космических
лучей.
Существуют три изотопа водорода:
а) легкий водород – протий,
б) тяжелый водород – дейтерий (D),
в) сверхтяжелый водород – тритий (Т).
Тритий неустойчивый
(радиоактивный) изотоп, поэтому в природе он практически не встречается.
Дейтерий устойчив, но его очень мало: 0,015% (от массы всего земного водорода).
Валентность
водорода в соединениях
В соединениях водород
проявляет валентность I.
Физические
свойства водорода
Простое вещество
водород (Н2) – это газ, легче воздуха, без цвета, без запаха, без
вкуса, tкип = – 2530С, водород в воде нерастворим , горюч. Собирать водород можно путем вытеснения
воздуха из пробирки или воды. При этом пробирку нужно перевернуть вверх дном.
Получение
водорода
В лаборатории водород
получают в результате реакции
Видео – Эксперимент
“Получение водорода и проверка его на чистоту”
Zn + H2SO4
= ZnSO4 + H2
.
Вместо цинка можно
использовать железо, алюминий и некоторые другие металлы, а вместо серной
кислоты – некоторые другие разбавленные кислоты. Образующийся водород собирают
в пробирку методом вытеснения воды (см. рис. 10.2 б) или просто в
перевернутую колбу (рис. 10.2 а).
В промышленности в больших
количествах водород получают из природного газа (в основном это метан) при
взаимодействии его с парами воды при 800 °С в присутствии никелевого
катализатора:
CH4 + 2H2O = 4H2 +CO2
(t, Ni)
или обрабатывают при
высокой температуре парами воды уголь:
2H2O + С =
2H2 + CO2. (t)
Чистый водород получают
из воды, разлагая ее электрическим током (подвергая электролизу):
2H2O = 2H2+ O2(электролиз).
Дополнительно:
Видео – Эксперимент
“Мыльные пузыри с водородом”
ТРЕНАЖЁРЫ
Тренажёр №1- Нахождение
водорода в природе. Физические свойства
Тренажёр №2 –
Характеристика водорода по положению в Периодической системе элементов Д. И.
Менделеева
АЛГОРИТМ СОСТАВЛЕНИЯ УХР ПОЛУЧЕНИЯ ВОДОРОДА
Источник
Если кислород является самым распространенным химическим элементом на Земле, то водород – самый распространенный элемент во всей Вселенной. Наше Солнце (и другие звезды) примерно на половину состоит из водорода, а что касается межзвездного газа, то он на 90% состоит из атомов водорода. Немалое место этот химический элемент занимает и на Земле, ведь вместе с кислородом он входит в состав воды, а само его название «водород» происходит от двух древнегреческих слов: «вода» и «рожаю». Помимо воды водород присутствует в большинстве органических веществ и клеток, без него, как и без кислорода, была бы немыслима сама Жизнь.
История открытия водорода
Первым среди ученых водород заметил еще великий алхимик и лекарь средневековья Теофраст Парацельс. В своих алхимических опытах, в надежде отыскать «философский камень» смешивая металлы с кислотами Парацельс получил некий неизвестный до того горючий газ. Правда отделить этот газ от воздуха так и не удалось.
Только спустя полтора века после Парацельса французскому химику Лемери таки удалось отделить водород от воздуха и доказать его горючесть. Правда Лемери так и не понял, что полученный им газ является чистым водородом. Параллельно подобными химическими опытами занимался и русский ученый Ломоносов, но настоящий прорыв в исследовании водорода был сделан английским химиком Генри Кавендишом, которого по праву считают первооткрывателем водорода.
В 1766 году Кавендишу удалось получить чистый водород, который он называл «горючим воздухом». Еще через 20 лет талантливый французский химик Антуан Лавуазье смог синтезировать воду и выделить из нее этот самый «горючий воздух» – водород. И к слову именно Лавуазье предложил водороду его название – «Hydrogenium», он же «водород».

Антуан Лавуазье со своей женой, помогавшей ему проводить химические опыты, в том числе и по синтезу водорода.
Водород в таблице Менделеева
В основе расположения химических элементов в периодической системе Менделеева лежит их атомный вес, рассчитанный относительно атомного веса водорода. То есть иными словами водород и его атомный вес является краеугольным камнем таблицы Менделеева, той точкой опоры, на основе которой великий химик создал свою систему. Поэтому не удивительно, что в таблице Менделеева водород занимает почетное первое место.

Помимо этого водород имеет такие характеристики:
- Атомная масса водорода составляет 1,00795.
- У водорода в наличии три изотопа, каждый из которых обладает индивидуальными свойствами.
- Водород – легкий элемент имеющий малую плотность.
- Водород обладает восстановительными и окислительными свойствами.
- Вступая в химические реакции с металлами, водород принимает их электрон и стает окислителем. Подобные соединения называются гидратами.
Строение молекулы водорода
Водород это газ, молекула его состоит из двух атомов.
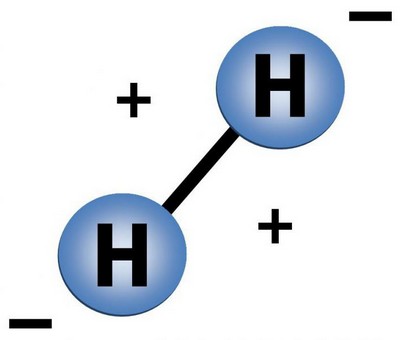
Так схематически выглядит молекула водорода.
Молекулярный водород, образованный из таких вот двухатомных молекул взрывается при поднесенной горящей спичке. Молекула водорода при взрыве распадается на атомы, которые превращаются в ядра гелия. Именно таким образом происходят ядерные реакции на Солнце и других звездах – за счет постоянного распадение молекул водорода наше светило горит и обогревает нас своим теплом.
Физические свойства водорода
У водорода в наличие следующие физические свойства:
- Температура кипения водорода составляет 252,76 °C;
- А при температуре 259,14 °C он уже начинает плавиться.
- В воде водород растворяется слабо.
- Чистый водород – весьма опасное взрывчатое и горючее вещество.
- Водород легче воздуха в 14,5 раз.
Химические свойства водорода
Поскольку водород может быть в разных ситуациях и окислителем и восстановителем его используют для осуществления реакций и синтезов.
Окислительные свойства водорода взаимодействуют с активными (обычно щелочными и щелочноземельными) металлами, результатом этих взаимодействий является образование гидридов – солеподобных соединений. Впрочем, гидриды образуются и при реакциях водорода с малоактивными металлами.
Восстановительные свойства водорода обладают способностью восстанавливать металлы до простых веществ из их оксидов, в промышленности это называется водородотермией.

Как получить водород?
Среди промышленных средств получения водорода можно выделить:
- газификацию угля,
- паровую конверсию метана,
- электролиз.
В лаборатории водород можно получить:
- при гидролизе гидридов металлов,
- при реакции с водой щелочных и щелочноземельных металлов,
- при взаимодействии разбавленных кислот с активными металлами.
Применение водорода
Так как водород в 14 раз легче воздуха, то в былые времена им начиняли воздушные шары и дирижабли. Но после серии катастроф произошедших с дирижаблями конструкторам пришлось искать водороду замену (напомним, чистый водород – взрывоопасное вещество, и малейшей искры было достаточно, чтобы случился взрыв).

Взрыв дирижабля Гинденбург в 1937 году, причиной взрыва как раз и стало воспламенение водорода (вследствие короткого замыкания), на котором летал этот огромный дирижабль.
Поэтому для подобных летательных аппаратов вместо водорода стали использовать гелий, который также легче воздуха, получение гелия более трудоемкое, зато он не такой взрывоопасный как водород.
Тем не менее, водород весьма хорошо зарекомендовал себя в качестве одного из компонентов ракетного топлива. А автомобили, работающие на водородном топливе более экологичнее своих дизельных и бензиновых собратьев.
Также с помощью водорода производится очистка различных видов топлива, в особенности на основе нефти и нефтепродуктов.
Водород, видео
И в завершение образовательное видео по теме нашей статьи.

Автор: Павел Чайка, главный редактор журнала Познавайка
При написании статьи старался сделать ее максимально интересной, полезной и качественной. Буду благодарен за любую обратную связь и конструктивную критику в виде комментариев к статье. Также Ваше пожелание/вопрос/предложение можете написать на мою почту pavelchaika1983@gmail.com или в Фейсбук, с уважением автор.
Источник
