В какой массе азота содержится 10 24 молекул и какой объем они занимают
Молекулы вступают в реакцию в определённых соотношениях, и это описывают химические реакции. Например, из этого уравнения
2Н2 + О2 = 2Н2О
видно, что в реакции приняли участие 2 молекулы водорода и 1 молекула кислорода, образовав при этом 2 молекулы воды. Но молекула так малы, что увидеть их невозможно, и уж тем более нельзя взять их в руки. Поэтому в учебнике химии и появляется понятие моль – количество вещества, в котором содержится число Авогадро частиц (6,02*10 в двадцать третьей степени). Рядом с этим понятием стоит другое – молярная масса, то есть масса 1 моля частиц. Молярная масса совпадает с атомной или молекулярной, рассчитывается по таблице Менделеева и выражается в граммах на моль (г/моль).
Фото: pixabay.com
Но мы прекрасно знаем, что не все вещества в обычных условиях находятся в твёрдом или жидком состоянии. Например, кислород, азот, хлор, неон – это газы. Резонно спросить: а как же их взвешивать? На этот случай химии для 8 класса припасено ещё одно понятие – молярный объём.
Что такое молярный объём
Тут следует запомнить, что в обычных условиях 1 моль любого газа занимает одинаковый объём. То есть молярный объём – это объём 1 моля любого газа. Сейчас советую на всякий случай вспомнить, что в 1 моле любого вещества (в том числе газа) содержится число Авогадро частиц. Старайтесь не забывать об этом факте.
Теперь надо обязательно упомянуть следующее. Все знают, что при изменении температуры и давления объём газов меняется. Так вот чтобы все расчёты вести правильно, то есть в одинаковых условиях, говорят о нормальных условиях: температуре 0 градусов Цельсия и давлении в 1 атмосферу (или 101,3 кПа). Это нужно просто запомнить:
нормальные условия в химии: температура – 0 градусов Цельсия, давление – 1 атм.
Экспериментально было доказано, что в нормальные условиях 1 моль любого газа занимает объем 22,4 литра.
То есть молярный объём любого газа в н.у. составляет 22,4 л/моль.
И это число тоже нужно запомнить! Оно даже важнее, чем сами нормальные условия, потому используется это число в решениях по химии намного чаще, чем н.у. (нормальные условия).
Как найти молярный объём
Очень просто. Если молярную массу для каждого вещества нужно рассчитывать по таблице Менделеева, то
молярный объём для всех газов одинаков.
Пример 1.
Молярная масса воды Н2О 18 г/моль (2*1+16, всё берем из периодической таблицы), молярная масса оксида кальция СаО 56 г/моль (40+16), молярная масса серной кислоты Н2SO4 98 г/моль (2*1+32+4*16).
Зато в нормальных условиях молярный объём кислорода О2 22,4 л/моль, молярный объём фтора P2 22,4 л/моль, молярный объём ксенона 22,4 г/моль. Приятно, не правда ли?
Другое дело, если речь идёт о химических реакциях. Но для начала просто потренируемся с цифрами.
Пример 2.
Определите объём, который занимают 10 моль кислорода в н.у.
Решение:
Молярный объём кислорода 22,4 л/моль, то есть 1 моль занимает 22,4 л. Следовательно, 10 моль будут занимать в 10 раз больше 22,4*10=224 литра. Это и есть ответ: 10 моль кислорода займут объём 224 литра.
Пример 3.
Известно, что неон в н.у. занял объём 5,6 литра. В каком количестве взят неон (в молях)?
Решение:
1 моль занимает объём 22,4 литра, а вот неизвестное число моль заняло объём 5,6 литра. Можно составить пропорцию:
1 моль – 22,4 литра
Х моль – 5,6 литра
Отсюда Х=1*5,6/22,4=0,25. Значит ответ такой: неон взяли в количестве 0,25 моль.
Пример 4.
Это уже расчёт по химической реакции, поэтому будьте внимательны. Итак, хлор прореагировал с водородом с образованием хлорида водорода:
Н2 + Cl2 = 2HCl
Для реакции взяли 11,2 литра водорода. Сколько понадобилось хлора (н.у.)?
Решение:
Посмотрим, сколько нам дано водорода по условию задачи. 1 моль водорода занимает объём 22,4 литра. Но у нас всего 11,2 литра водорода, то есть Х моль. Составим пропорцию:
1 моль – 22,4 литра
Х моль – 11,2 литра
Отсюда Х=1*11,2/22,4=0,5 моль водорода. Значит, по условию задачи у нас водорода 0,5 моль.
Из уравнения химической реакции Н2 + Cl2 = 2HCl видно, что нам нужно по 1 молю водорода и хлора (об этом говорят коэффициенты в уравнении). То есть, 1 моль водорода реагирует с 1 молем хлора. Но нам дали всего 0,5 моль водорода, сколько нам нужно хлора? Составим ещё одну пропорцию:
1 моль водорода реагирует с 1 молем хлора
0,5 моль водорода реагирует с Х молями хлора.
Отсюда получаем: Х=0,5*1/1=0,5 моль. Таким образом, нам нужно 0,5 моль хлора. А это количество занимает объём 22,4*0,5=11,2 литра.
Ответ: понадобилось 11,2 литра хлора.
В следующий раз мы научимся делать расчёты по реакциям, в которых участвуют и твёрдые вещества, и газы, то есть одновременно будем использовать молярную массу и молярный объём.
Пишите, пожалуйста, в комментариях, что осталось непонятным, и я обязательно дам дополнительные пояснения. Жалуйтесь на сложности в изучении школьного курса и говорите, что вас испугало в учебнике химии. И тогда следующая статья будет рассказывать именно об этой проблеме.
Источник
Решение задач на количественные характеристики вещества:
количества вещества, массу и объем
Количество вещества (ν) связано с числом структурных единиц (N) в образце вещества, его массой (m) и объемом (V) — для газообразных веществ при н. у. — следующими уравнениями:
 в которых
в которых
Vm = 22,4 л/моль (мл/ммоль, м3/кмоль) при н.у.,
NA = 6,02 • 1023 (постоянная Авогадро),
а молярная масса (М) численно равна относительной молекулярной массе вещества.
Цитаты из пособия «Задачи по химии 8-9 кл.» (авт. О.С. Габриелян и др.) использованы в учебных целях. Ссылка на покупку книги указана в конце конспекта.
ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ
№ 1.
Определите абсолютную массу (в г) одной молекулы воды.
 Ответ: m (молекулы Н2O) = 2,99 • 10–23 г.
Ответ: m (молекулы Н2O) = 2,99 • 10–23 г.
№ 2.
Определите массу порции оксида серы (VI), содержащей 7,224 • 1023 атомов кислорода.

Ответ: m(SO3) = 32 г.
№ 3.
Сколько атомов азота содержится в оксиде азота (I), объем которого (н. у.) равен 20,16 л?
 Ответ. N(N) = 10,836 • 1023.
Ответ. N(N) = 10,836 • 1023.
№ 4.
Определите объем (н. у.) оксида углерода (IV), в котором содержится столько же атомов кислорода, сколько их содержится в 48 г карбоната кальция.

Ответ. V(СO2) = 16,12 л.
№ 5.
Определите относительную плотность сероводорода по водороду и по воздуху.

Ответ: DH2(H2S) = 17; Dвозд(H2S) = 1,17.
№ 6.
Плотность газа по кислороду равна 0,875. Определите число молекул, содержащихся в 15,4 г этого газа.

Ответ. N(газа) = 3,311 • 1023.
ЗАДАЧИ с КРАТКИМ ОТВЕТОМ
№ 7. Сплав содержит 16 г меди и 11,2 г железа. Атомов какого метала будет больше в данном образце сплава?
№ 8. Смешали 16,8 г азота и 15,68 л (н. у.) водорода. Какое суммарное число молекул обоих газов будет содержаться в данной смеси?
№ 9. Чему равна масса порции хлорида бария, содержащая 1,3244 • 1024 ионов хлора?
№ 10. Какую массу должен иметь образец нитрата калия, чтобы в нем было столько же атомов кислорода, сколько их содержится в образце сульфата натрия массой 21,3 г?
№ 11. Сколько атомов хлора содержится в смеси, состоящей из 16,68 г хлорида фосфора (V) и 16,5 г хлорида фосфора (III)?
№ 12. Вычислите массу смеси, содержащей 672 мл (н. у.) оксида азота (I), 0,125 моль оксида азота (II) и 1,15 г оксида азота (IV). Сколько атомов азота будет содержаться в этой смеси?
№ 13. Молекула некоторого газа имеет массу 6,063* 10–23г. Определите плотность данного газа по гелию.
№ 14. Вычислите плотность газа по азоту, если 1 л (н. у.) этого газа имеет массу 1,7857 г.
№ 15. Плотность газа по воздуху равна 2,207. Найдите плотность этого газа по хлору и массу одной молекулы этого газа (в г).
№ 16. Масса порции оксида алюминия равна массе порции оксида кремния (IV). В какой порции будет содержаться больше атомов кислорода?
№ 17. Порции метана СН4 и аммиака NH3 содержат одинаковое число атомов водорода. Какая порция будет иметь большую массу?
№ 18. Десять молекул газа имеют массу 6,063 * 10–22г. Определите плотность данного газа по водороду.
№ 19. Определите массу и объем (н. у.) аммиака, содержащего столько же атомов водорода, сколько их содержится в 2,55 г сероводорода.
Решение задач на основные количественные характеристики вещества. Выберите дальнейшие действия:
- Перейти к следующей теме: Решение задач с долей вещества в смеси, в соединении.
- Вернуться к списку конспектов по Химии.
- Проверить знания по Химии.
- Купить книгу Задачи по химии и способы их решения. 8-9 кл. / О.С. Габриелян и др. — М.: Дрофа.
Источник
Решениие задач по химии на закон Авогадро
Задача 53.
Сопоставить числа молекул, содержащихся в 1г NH3 и в 1г N2. В каком случае и во сколько раз число молекул больше?
Решение:
В одном моле любого вещества содержится 6,02 . 1023 молекул этого вещества.
Рассчитаем содержание количества вещества в 1г NH3 и N2 по формуле:
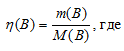
 (B) – количество вещества (В);
(B) – количество вещества (В);
m(B)- масса вещества (В);
M(B) – Молярная масса вещества (В).
М(NH3) = 17г/моль, M(N2) = 28г/моль.
Тогда
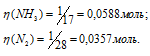
Число молекул NH3 больше числа молекул N2, так как  (NH3) >
(NH3) > (N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
(N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
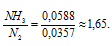
Ответ: в 1,65 раз число молекул NH3 больше числа молекул N2.
Задача 54.
Выразить в граммах массу одной молекулы диоксида серы.
Решение:
Находим молекулярную массу диоксида серы:
M(SO2) = 32 + (16 . 2) = 64г/моль.
Молекулярная масса численно составляет массу одного моля вещества, а значит, вес одного моля численно равен молекулярной массе и составляет 64г. Известно, что в одном моле любого вещества содержится 6,02 . 1023 молекул данного вещества. Исходя из этого, рассчитаем массу в граммах одной молекулы диоксида серы:
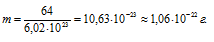
Ответ: масса одной молекулы диоксида серы равна.
Задача 55.
Одинаково ли число молекул в 0,001кг Н2 и в 0,001кг О2? В 1 моле Н2 и в 1 моле 02? В 1л Н2 и в 1л О2 при одинаковых условиях?
Решение:
Молекулярные массы водорода и кислорода равны соответственно 2г/моль и 32г/моль. Отсюда находим количество водорода и кислорода, зная их массы:
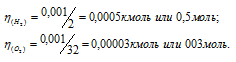
Один моль любого вещества содержит 6,02 .1023 молекул. Следовательно, в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул:

Так как имеется по одному молю водорода и кислорода, то количество молекул веществ будет одинаково:
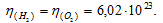
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1л водорода и в 1л кислорода:
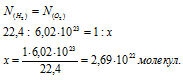
Ответ: а) в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул; б) в одном моле водорода и в одном моле кислорода содержится одинаковое число молекул: в) в одном литре водорода и в одном литре кислорода содержится одинаковое число молекул.
Задача 56.
Сколько молекул содержится в 1,00 мл водорода при нормальных условиях?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 .1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1мл водорода из пропорции:
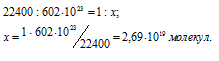
Ответ: 2,69 .1019 молекул.
Задача 57.
Какой объем при нормальных условиях занимают 27 .1021 молекул газа?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда находим какой объём при нормальных условиях занимают 27 .1021 молекул газа, составив пропорцию:
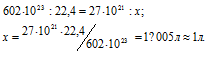
Ответ: V=1л.
Задача 58.
Каково соотношение объемов, занимаемых 1 молем О2 и 1 молем О3 (условия одинаковые)?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Следовательно соотношение объёмов, занимаемых одним молем О2 и одним молем О3 иметь вид:
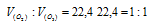
Ответ: 1:1
Задача 59.
Взяты равные массы кислорода, водорода и метана при одинаковых условиях. Найти отношение объемов взятых газов.
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Мольные массы кислорода, водорода и метана, соответственно равны 32 г/моль; 2г/моль; 16 г/моль.
Так как массы кислорода, водорода и метана одинаковы при одинаковых условиях, то отношение объёмов взятых газов находим из пропорции:
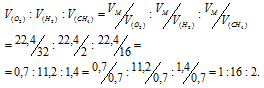
Ответ: 1:16:2.
Задача 60.
На вопрос, какой объем займет 1моль воды при нормальных условиях, получен ответ: 22,4л. Правильный ли это ответ?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Так как вода при нормальных условиях находится в жидкой, а не в газообразной фазе, то ответ, что 1моль воды займёт 22,4л не правильный. Учитывая, что молярная масса воды равна 18г/моль, а плотность равна единице, то правильный ответ будет равен:
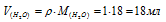
Ответ: 18мл.
Задача 61.
Сколько молекул диоксида углерода находится в 1л воздуха, если объемное содержание СО2 составляет 0,03% (условия нормальные)?
Решение:
При нормальных условиях углекислый газ, содержащийся в 1л воздуха, занимает объём 0,0003л. Зная, что мольный объём любого газа занимает 22,4л, рассчитаем число молей углекислого газа в 0,0003л из пропорции:
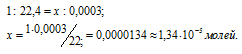
Учитывая, что в одном моле вещества содержится 6,02 . 1023 молекул, находим число молекул в 0,0003л газа:

Ответ: 8,07 .1018 молекул.
Источник
Сохраните:
Ответы и задания для 6,7,8,9,10,11 класса 43-го турнира Ломоносова по химии 2020-2021 учебный год, официальная дата проведения турнира в онлайне: 04.10.2020 (4 октября 2020 год).
P.S свои ответы пишите в комментариях ниже, тем самым поможете другим ребятам, а они вам.
Ссылка для скачивания заданий для 6-11 класса: скачать задания
43 турнир М.В. Ломоносова по химии задания и ответы 6-11 класс 2020:
1)Рассчитайте молекулярную массу вещества, имеющего формулу Ca(HCO3)2. Атомные массы считайте целыми числами.
Ответ: 162
2)Рассчитайте, сколько протонов содержится в ядрах всех атомов, входящих в состав молекулы серной кислоты (H2SO4).
Ответ: 50
3)Школьник нашел моток проволоки из белого металла. Он предположил, что это оловянная проволока, тем более ему как раз требовалось олово для пайки. Но как убедиться в этом? К счастью недавно он как раз изучал в школе закон Архимеда, поэтому сразу сообразил, что нужно делать. Он взвесил проволоку и получил величину 841,3 г. Затем он полностью погрузил проволоку в воду и снова взвесил ее, на этот раз весы показали 726,3 г. Школьник произвел необходимые расчеты и убедился, что проволока действительно изготовлена из олова.
Определите по этим данным плотность олова. Приведите свой расчет.
Ответ: 7,3 г/см
Если бы проволока такой же массы (841,3 г) была изготовлена из алюминия, плотность которого 2,7 г см3, то сколько бы она весила в воде?
Ответ: 530,3
4)Водород взаимодействует с парами йода образуя газообразный иодоводород HI. В реакцию в замкнутом сосуде ввели некоторые количества H2 и I2. Через некоторое время состав смеси (в % по молям) стал таким: 30% HI, 10% H2 и 60% I2.
Определите мольное соотношение водорода и йода в первоначальной смеси.
Для реакции взяли такую же смесь водорода и паров йода, как в вопросе 1. Через некоторое время в смеси обнаружено 0,4 моль HI. Определите количества (в моль) водорода и йода, которые в этот момент остаются в сосуде, если известно, что количество водорода уменьшилось в ходе реакции на 50%.
5)Вещества А, Б, В и Г вступают в следующие реакции (многоточие означает, что в реакции образуются и другие продукты): А+K2CO3 + H2O = 2Б Б+HCl =А+….. А+2Mg =В+….. В+O2 =А А+В= 2Г. Определите вещества А, Б, В и Г, если известно, что они все содержат один и тот же элемент, причем его содержание в веществе А составляет 27,27%.
Ответ: A – CO2, Б – KHCO3, В – C, Г – CO
6)В лаборатории имеется пять колб с водными растворами различных веществ. Они подписаны: №1 хлорид аммония, №2 — соляная кислота, №3 — гидроксид калия, №4 — хлорид алюминия, №5 — карбонат натрия. Однако все этикетки перепутаны таким образом, что ни один из растворов не подписан правильно.
При сливании раствора №1 с раствором №4 выделяется газ, который окрашивает влажную индикаторную бумажку в синий цвет. При сливании растворов №2 и №3 выпадает осадок. А при сливании раствора №2 с раствором №5 никаких изменений не происходит.
- Укажите правильные надписи для колб №№ 1–5. Приведите необходимые рассуждения.
- Напишите уравнения реакций, упомянутых в условии.
- Какие еще реакции можно провести между указанными веществами? Напишите их уравнения.
Ответ: №1 карбонат натрия, №2 гидроксид калия, №3 хлорид аллюминия, №4 хлорид аммония, №5 соляная кислота. 2_NH4Cl + Na2CO3 = H2O + CO2 + 2_NaCl + 2_NH3 AlCl3+ 3_KOH = Al(OH)3 + 3_KCl KOH+ HCl= H2O+ KCl
7)Смесь, состоящую из металла А и не которого оксида Б, прокалили и получили смесь продуктов В и Г. При растворении смеси В и Г в избытке соляной кислоты была получена соль Д и выделился горючий газ Е с плотностью по водороду 16. К раствору, содержащему соль Д массой 4,75 г, добавили избыток раствора гидроксида натрия, выпавший при этом осадок отделили, высушили и прокалили, при этом было получено 2,0 г продукта Ж.
- Определите вещества А–Ж.
- Приведите необходимые расчеты
Ответ: А – магний Б – оксид кремния (IV) В – силицид магния Г – оксид магния Д – хлорид магния Е – силан Ж – оксид магния.
Mg+SiO2=Mg2Si+MgOMgO+2HCl=MgCl2+H2OMg2Si+4HCl=SiH4+2MgCl2MgCl2+2NaOH=Mg(OH)2+2NaClMg(OH)2=MgO+H2O
8)Смесь пропана и пропена пропустили в темноте через сосуд, содержащий раствор брома в четыреххлористом углероде. После пропускания газовой смеси масса сосуда увеличилась на 1,26 г. Газ, который не поглотился раствором брома, собрали и сожгли в кислороде. Продукты сгорания последовательно пропустили через трубки, содержащие избыток безводного оксида фосфора(V) и избыток сухого гидроксида калия. Масса первой трубки увеличилась на 2,52 г, а масса второй — на 5,28 г.
- Определите количество пропана в исходной смеси (в моль).
- Определите количество пропена в исходной смеси (в моль).
- Приведите необходимые расчеты.
9)Органическое вещество Х имеет следующий элементный состав: 61,31% C; 5,11% H; 23,36% O; и 10,22% N и молекулярную массу менее 180. Вещество Х можно получить из бензола в четыре стадии. Ниже приведены реагенты и условия, которые требуются на каждой стадии, но в произвольном порядке, не соответствующем реальной последовательности реакций.
- HNO3, H2SO4
- Zn, HCl
- C2H4, H3PO4
- KMnO4, H2SO4 (водный раствор)
В реакции, приведенной под номером 1, образуется два изомерных продукта, в реальных синтезах требуется их разделение. В качестве решения вы можете выбрать любой из изомеров.
- Определите вещество Х
- Расставьте стадии его получения в правильном порядке
- Определите промежуточные вещества, которые получаются на каждой стадии (запишите их названия).
04.10.2020 XLIII Турнир Ломоносова задания и ответы по всем предметам:
04.10.2020 XLIII Турнир Ломоносова задания и ответы
Источник
На самом деле, понятия «атомистика» не существует, но в интернете стали так говорить, поэтому и я не буду исключением.
Задачи на «атомистику» — это задачи на соотношения частиц (атомов, молекул, ионов и т.д.) в гомогенных и гетерогенных системах (растворах, твердых и газообразных смесях). Это могут быть массовые соотношения (например, массовая доля элемента в смеси), мольные соотношения (например, соотношение числа атомов водорода и кислорода или мольная доля), объемные соотношения (объемная доля и др.).
Задачи разделены по уровню сложности: от простых до сложных. А также предлагаю вам порешать задачи на удобрения, в которых без «атомистики» не обойтись. Как показывает моя практика, если вы умеете решать задачи на удобрения, то вы полностью понимаете тему «атомистика».
И, конечно же, после каждой задачи вы найдёте подробные видео-объяснения, а ответы в конце страницы.
- Простые задачи
- Задачи средней сложности
- Сложные задачи
- Задачи на удобрения
- Задачи из реального ЕГЭ 2020 на атомистику
Простые задачи
Укажите число атомов водорода в одной формульной единице гидросульфита аммония NH4HSO3.
Рассчитайте химическое количество азота в порции простого вещества, содержащей 6,02∙1025 молекул.
Имеется сосуд, в котором содержится 8,428∙1022 молекул некоторого газа. Укажите объём сосуда (в литрах).
Рассчитайте химическое количество (моль) поваренной соли, в которой содержится такое же химическое количество натрия, как и в карбонате натрия химическим количеством 4 моль.
В каком объёме (л) бурого газа содержится столько же атомов, сколько и в аргоне объёмом 2 л (объёмы измерены при одинаковых условиях)?
Рассчитайте количество (моль) CO2, в котором содержится столько же атомов углерода, сколько их содержится в СО массой 1,4 г.
Рассчитайте количество (моль) атомов водорода в аммиаке, объёмом (н.у.) 32,48 л.
Укажите объём (л) порции метана СН4 (н.у.), в которой содержится 0,1 моль атомов углерода.
Рассчитайте объём оксида азота (IV) (л, н.у.), в котором содержится столько же атомов азота и кислорода в сумме, как и общее число атомов в азотной кислоте массой 56,7 г.
Рассчитайте массу (г) порции азотной кислоты, содержащей столько же атомов водорода, сколько в аммиаке объёмом 3,36 л (н.у.).
Укажите число атомов водорода в образце дигидата ацетата цинка ((CH3COO)2Zn∙2H2O) массой 131,4 г.
Вычислите число атомов в образце фтора (н.у.) объёмом 30,24 дм3.
Укажите количество (моль) оксида серы (VI), содержащего столько же атомов кислорода, как и в оксиде серы (IV) массой 76,8 г.
Вычислите число атомов азота в порции гидросульфата аммония массой 16,1.
Рассчитайте массу (г) соли Na2S, содержащей столько же атомов серы, сколько их содержится в сероводороде массой 48,96 г.
Укажите число моль воды в 1 моль кристаллогидрата сульфата натрия с Mr равной 322.
Каков объём кислорода (л, н.у.), содержащего столько же атомов кислорода, сколько их содержится в алебастре массой 87 г?
Рассчитайте количество (моль) ионов в навеске селенида калия массой 39,25.
В порции газа массой 26,4 г содержится 3,612∙1023 молекул. Укажите относительную плотность этого газа по водороду.
Вычислите количество (моль) всех анионов, содержащихся в Ca3(PO4)2 массой 372 г.
Какое число электронов содержится в образце массой 6,4 г, состоящем из нуклида меди-64?
Задачи средней сложности
Образец сплава железа-56 с медью-63 содержит электроны и нейтроны химическим количеством 2,77 моль и 3,21 моль соответственно. Рассчитайте массовую долю (%) меди в сплаве.
Какую массу (г) гидросульфата аммония надо добавить к гидросульфиту натрия массой 15,6 г для получения смеси, содержащей равное число атомов водорода и кислорода?
Какую массу (г) сульфата натрия следует добавить к сульфиду натрия массой 3,9 г, чтобы в полученной смеси массовая доля натрия стала равной 51,9%?
В порции кристаллогидрата сульфата железа (II) содержится 1,204∙1024 атомов железа и 1,3244∙1025 атомов кислорода. Укажите число атомов водорода в данной порции кристаллогидрата.
В смеси оксида железа (II) и оксида железа (III) на 4 атома железа приходится 5 атомов кислорода. Вычислите массовую долю (%) оксида железа (II) в такой смеси.
Газовая смесь содержит 6,02∙1022 молекул и имеет массу 2,3 г. Укажите относительную плотность этой газовой смеси по кислороду.
Для получения бронзы массой 567 г (массовая доля меди 79,01%) использовали минералы медный блеск Cu2S и касситерит SnO2. Укажите общую массу (г) израсходованных минералов, если считать, что минералы не содержали примесей.
Образец минерала браунита массой 100 состоит из вещества, формула которого 3Mn2O3∙MnCO3, и примесей, которые не содержат в своём составе металлы. Массовая доля этих примесей 1,5%. Вычислите массу (г) марганца в исходном образце минерала.
Одна таблетка биологически активных добавок (БАВ) к пище содержит медь массой 2 мг, где медь находится в форме ацетата меди (II). Укажите массу (г) ацетата меди (II), который поступает в организм за неделю при ежедневном приёме 1 таблетки БАВ.
Алюминиевая руда (боксит) состоит из оксида алюминия и других веществ, не содержащих алюминий. Массовая доля алюминия в боксите составляет 21,6%. Вычислите массу (г) оксида алюминия в образце боксита массой 100 г.
Сложные задачи
Для анализа смеси массой 3,125 г, состоящей из хлорида калия и бромида калия, её растворили в воде и к полученному раствору добавили раствор нитрата серебра (I) массой 42,5 г с массовой долей соли 20%. В результате чего образовался осадок массой 5,195 г. Рассчитайте массовую долю (%) ионов калия в исходной смеси.
