В каком количестве вещества бензола с6н6 содержится

Определение и формула
Заголовок
Простой углеводород. Относится к ароматическим углеводородам, классу органических веществ.
Вещество представляет собой прозрачную жидкость, не имеет цвета, обладает сладковатым характерным запахом. Бензол относят к ненасыщенным углеводородам. Знаменитая формула бензольного кольца была предложена нобелевским лауреатом в области химии – Лайнусом Полингом. Именно он предложил изображать бензол в виде шестигранника с окружностью внутри. Это изображение дает понимание об отсутствии двойных связей и наличии единого электронного облака, в которое охвачены все 6 атомов углерода.
Формула
C6H6
Получение бензола
Естественные источники получения
Естественный источник для получения бензола – это каменный уголь. Процесс коксования каменного угля был открыт Майклом Фарадеем в далеком 1825 году. Он изучал светильный газ, который использовали в фонарях уличного освещения, смог выделить и описать бензол. Сейчас этим способом из каменноугольной смолы бензол практически не получают. Существует множество других более продуктивных способов его получения.
Искусственные источники получения
- Искусственный каталитический риформинг бензина. Для получения используются бензиновые нефтяные фракции. В этом процессе образуется большое количество толуола. Спрос на рынке для толуола не очень большой, поэтому из него также далее получают бензол. Из тяжелых фракций нефти пиролизом через процесс деалкилирования смеси толуола, ксилола получают бензол.
- Получение методом Реппе. До 1948 года по методу Бертло получали бензол, пропуская ацетилен над активированным углем при температуре 400°C. Выход бензола был большой, но получалась многокомпонентная смесь веществ, с трудом поддающаяся очистке. В 1948 году Реппе заменил активированный уголь никелем. В результате на выходе получался бензол. Процесс называется тримеризацией ацетелена – три молекулы ацетилена превращаются в одну бензола:
3С2Н2 → С6H6.
Свойства бензола
Физические свойства
| Свойство | Описание |
|---|---|
| плотность | 0,879 г/см3 |
| молярная масса | 78,11 г/моль |
| цвет жидкости | прозрачный, бесцветный |
| температура кипения | 80,1°C |
| температура плавления | 5,5°C |
| растворимость в воде | не растворяется |
При горении выделяется большое количество копоти, так как углеводород ненасыщенный (ему не хватает 8 атомов водорода, чтобы отвечать стандартной формуле предельных углеводородов). При низких температурах бензол становится белой кристаллической массой.
Химические свойства
Бензол вступает в реакции замещения в присутствии катализаторов – обычно это соли Al(3+) или Fe(3+):
- Галогенирование – качественная реакция на бензол с Br2:
C6H6 + Br2 = C6H5Br + HBr.
- Нитрование – взаимодействие с азотной кислотой. В органической химии этот процесс сопровождается отщеплением OH-группы:
C6H6 + HO-NO2 → C6H5NO2 + H2O.
- Каталитическое алкилирование приводит к получению гомологов бензола – алкилбензолов:
С6H6 + С2H5Cl → C6H5C2H5 + HCl.
Гомологи бензола, содержащие радикал, реагирует не так как сам бензол. Реакции идут по-другому и часто на свету:
- галогенирование С6H5-CH3 + Br2 (на свету) = С6H5-CH2Br + HBr;
- нитрование – С6H5-CH3 + 3HNO3 → C6H2CH3(NO2)3.
Реакции окисления бензола идут очень сложно и не характерны для этого вещества. Окисление характерно для гомологов. Вот, например, реакция получения бензойной кислоты:
С6H5CH3 + [O] → C6H5COOH.
Процесс горения вещества происходит по стандартной схеме для всех органических веществ:
CnH2n-6 + (3n-3)2 O2 → nCO2 + (n-3)H2O.
Реакции гидрирования. Реакция проходит сложно, требуются катализаторы, давление, температура. В реакциях бензола с водородом получается циклогексан:
С6H6 + 3H2 → C6H12.
А в реакциях с алкилбензолом – метилциклогексан, где один атом водорода замещается на радикальную группу -CH3:
С6H5CH3 + 3H2 → C6H11-CH3.
Применение бензола
Бензол в чистом виде практически не используется. Его вырабатывают для производства других важных соединений, таких как, например, этилбензол, из которого получают стирол и полистирол.
Львиную долю бензола пускают на производства фенола, который необходим в производстве капрона, красителей, пестицидов, лекарств. Знаменитое лекарство аспирин невозможно получать без участия фенола.
Циклогексан из бензола необходим для производства пластмасс и искусственных волокон, нитробензол идет на выработку анилина, который используют для производства каучуков, красителей и гербицидов.
Тест по теме «Бензол»
Источник
Арены – ароматические углеводороды, содержащие одно или несколько бензольных колец.
Бензольное кольцо составляют 6 атомов углерода, между которыми чередуются двойные и одинарные связи.
Важно заметить, что двойные связи в молекуле бензола не фиксированы, а постоянно перемещаются по кругу.
Арены также называют ароматическими углеводородами. Первый член гомологического ряда – бензол – C6H6.
Общая формула их гомологического ряда – CnH2n-6.
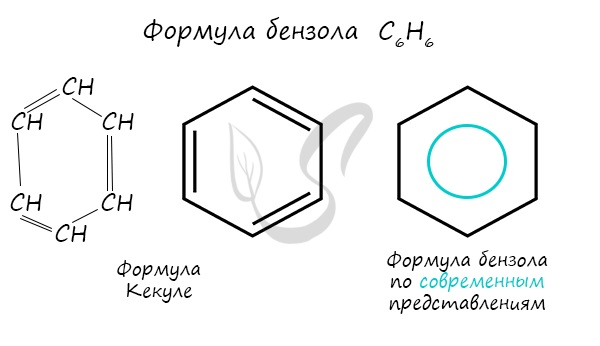
Долгое время структурная формула бензола оставалась тайной. Предложенная Кекуле формула с двумя тройными связями не могла
объяснить то, что бензол не вступает в реакции присоединения. Как уже было сказано выше, по современным представлениям,
двойные связи в молекуле постоянно перемещают, поэтому правильнее рисовать их в виде кольца.
За счет чередования двойных связей в молекуле бензола формируется сопряжение. Все атомы углерода находятся в состоянии sp2
гибридизации. Валентный угол – 120°.
Номенклатура и изомерия аренов
Названия аренов формируются путем добавления названий заместителей к главной цепи – бензольному кольцу: бензол, метилбензол (толуол),
этилбензол, пропилбензол и т.д. Заместители, как обычно, перечисляются в алфавитном порядке. Если в бензольном кольце несколько заместителей,
то выбирают кратчайший путь между ними.
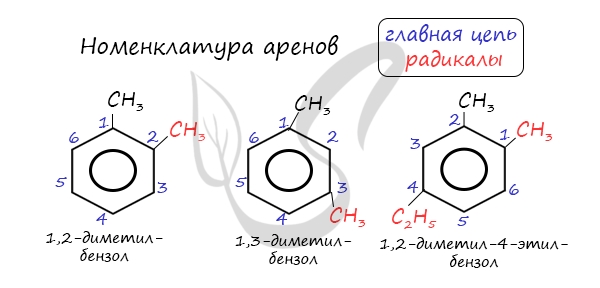
Для аренов характерна структурная изомерия, связанная с положением заместителей. Например, два заместителя в бензольном
кольце могут располагаться в разных положениях.
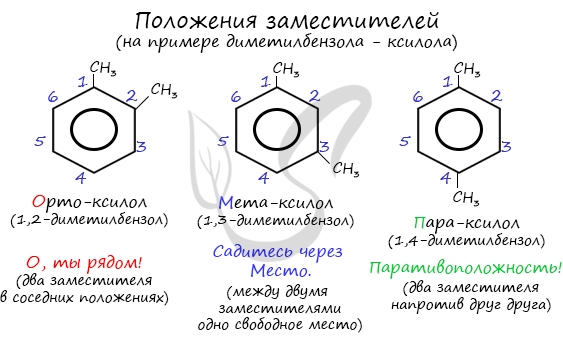
Название положения заместителей в бензольном кольце формируется на основе их расположения относительно друг друга. Оно обозначается
приставками орто-, мета- и пара. Ниже вы найдете мнемонические подсказки для их успешного запоминания 😉
Получение аренов
Арены получают несколькими способами:
- Реакция Зелинского (тримеризация ацетилена)
- Дегидроциклизация алканов
- Дегидрирование циклоалканов
- Синтез Дюма
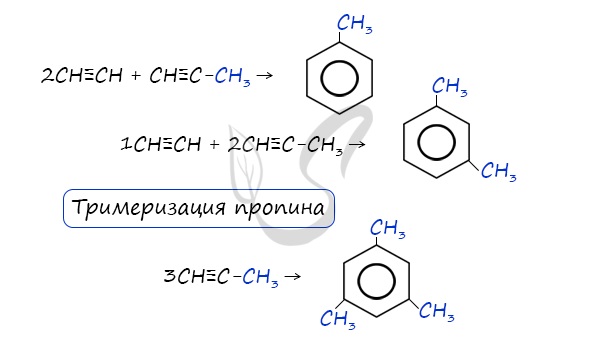
Данная реакция протекает при пропускании ацетилена над активированным углем при t = 400°C. В результате образуется ароматический
углеводород – бензол.

В случае, если к ацетилену добавить пропин, то становится возможным получение толуола. Увеличивая долю пропина, в конечном итоге
можно добиться образования 1,3,5-триметилбензола.
В ходе таких реакций, протекающих при повышенной температуре и в присутствии катализатора – Cr2O3, линейная
структура алкана замыкается в цикл, отщепляется водород.
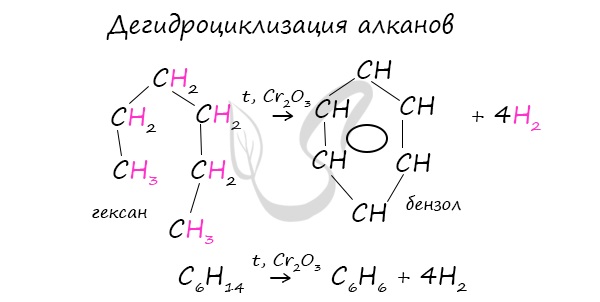
При дегидроциклизации гептана получается толуол.
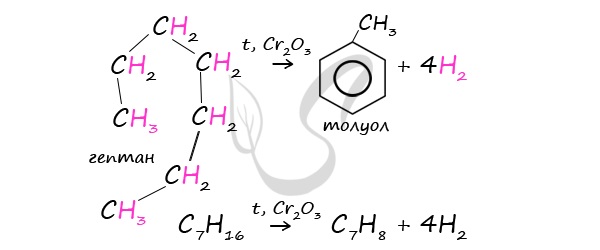
В результате дегидрирования уже “готовых” циклов – циклоалканов, отщепляются 3 моль водорода, и образуется соответствующий арен,
с теми же заместителями, которые были у циклоалкана.

Синтез Дюма заключается в сплавлении солей карбоновых кислот с щелочами. В результате такой реакции возможно образование различных органических веществ, в том числе аренов.
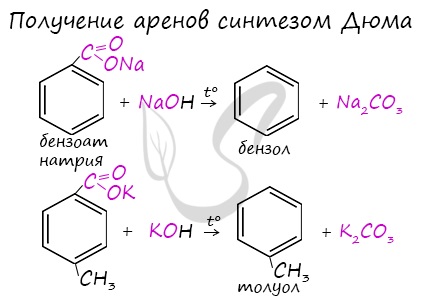
Химические свойства аренов
Арены – ароматические углеводороды, которые содержат бензольное кольцо с сопряженными двойными связями. Эта особенность
делает реакции присоединения тяжело протекающими (и тем не менее возможными!)
Запомните, что, в отличие от других непредельных соединений, бензол и его гомологи не обесцвечивают бромную воду и
раствор перманганата калия.
- Гидрирование
- Галогенирование
- Нитрование
- Алкилирование
- Окисление
- Полимеризация
При повышенной температуре и наличии катализатора, водород способен разорвать двойные связи в бензольном кольце
и превратить арен в циклоалкан.

Реакция бензола с хлором на свету приводит к образованию гексахлорциклогексана, если же использовать только катализатор,
то образуется хлорбензол.
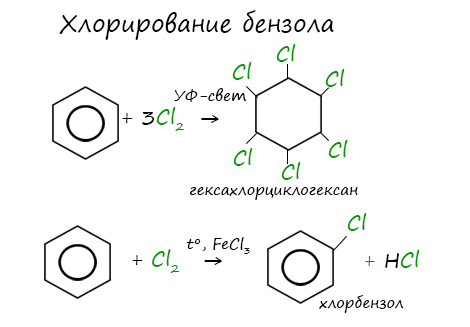
Реакции с толуолом протекают иначе: при УФ-свете хлор направляется в радикал метил и замещает атом водорода в нем, при действии катализатора хлор замещает один атом водорода в бензольном кольце (в орто- или пара-положении).
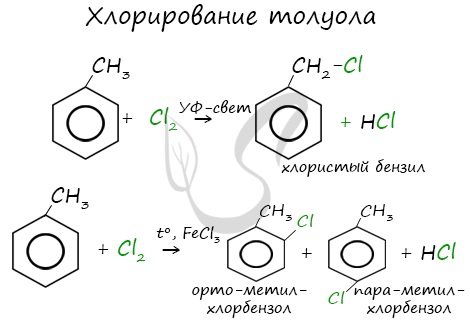
Почему хлор направляется именно в орто- и пара-положения относительно метильной группы? Здесь самое время
коснуться темы ориентантов I (орто-, пара-ориентантов) и II порядков (мета-ориентанты).
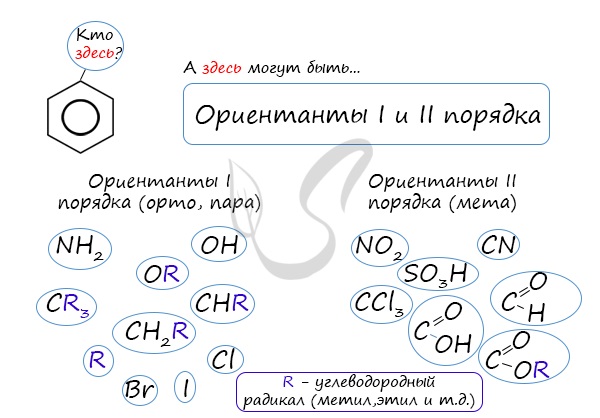
К ориентантам первого порядка относятся группы: NH2, OH, OR, CR3, CHR2,
CH 2R, галогены. К ориентантам второго: NO2, CN, SO3H, CCl3,
CHO, COOH, COOR.
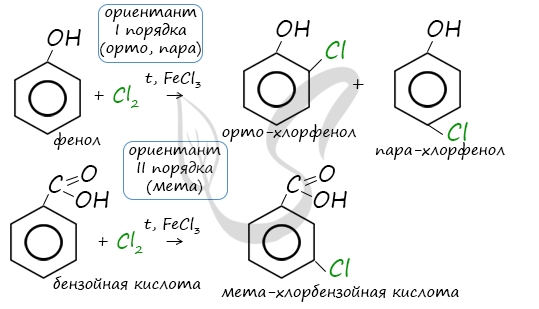
Например, ориентант I порядка, гидроксогруппа OH, обеспечивает протекание хлорирования в орто- и пара-положениях.
А карбоксильная группа COOH, ориентант II порядка, обуславливает хлорирование в мета-положениях.
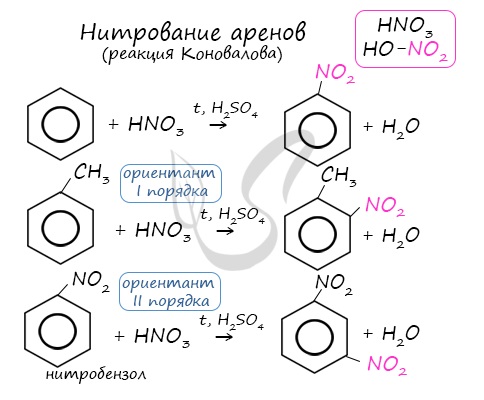
Арены вступают в реакции нитрования, протекающие при повышенной температуре и в присутствии серной кислоты,
обладающей водоотнимающими свойствами.
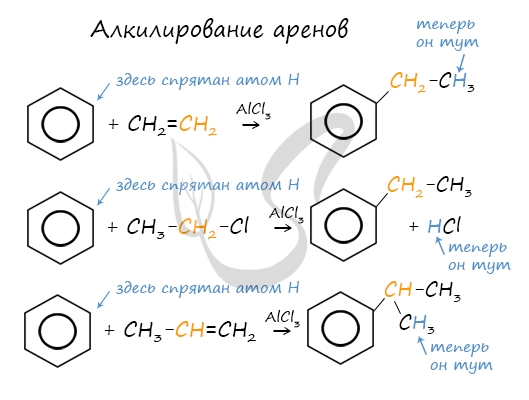
Алкилирование аренов осуществляется путем введения алкильного радикала в молекулу бензола. Алкильным радикалом чаще
всего выступает алкен или галогеналкан.
В случае если для алкилирования используется алкен, то с молекулой бензола соединяется наименее гидрированный атом
углерода алкена, прилежащий к двойной связи. Один атом водорода переходит из бензольного кольца к радикалу.
Арены, как и все органические вещества, сгорают с образованием углекислого газа и воды.
2C6H6 + 15O2 → 12CO2 + 6H2O
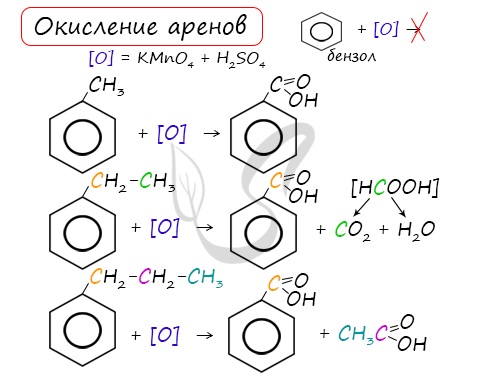
При неполном окислении гомологи бензола способны окисляться до бензойной кислоты (при подкислении раствора серной
кислотой). Сам бензол не вступает в реакцию окисления с KMnO4, не обесцвечивает его раствор.
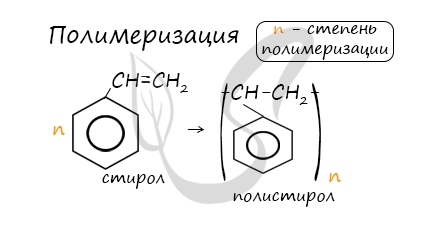
В реакцию полимеризации способен вступать стирол (винилбензол), в радикале которого содержится двойная связь.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
Ароматические углеводороды. Бензол и его гомологи
Ароматические углеводороды (арены) – вещества, в молекулах которых содержится одно или несколько бензольных колец – циклических групп атомов углерода с особым характером связей. Гомологический ряд CnH2n-6.
Понятие «бензольное кольцо» сразу требует расшифровки. Для этого необходимо хотя бы коротко рассмотреть строение молекулы бензола. Первая структура бензола была предложена в 1865 г. немецким ученым А. Кекуле:
К наиболее важным ароматическим углеводородам относятся бензол С6Н6 и его гомологи : толуол С6Н5СНз, ксилол С6Н4(СНз)2 и др.; нафталин C10H8, антрацен С14Н10 и их производные.
Атомы углерода в молекуле бензола образуют правильный плоский шестиугольник, хотя обычно его рисуют вытянутым.
Окончательно строение молекулы бензола подтверждено реакцией образования его из ацетилена. В структурной формуле изображается по три одинарных и три двойных чередующихся углерод-углеродных связей. Но такое изображение не передает истинного строения молекулы. В действительности углерод-углеродные связи в бензоле равноценны, и они обладают свойствами, не похожими на свойства ни одинарных, ни двойных связей. Эти особенности объясняются электронным строением молекулы бензола.
Электронное строение бензола
Каждый атом углерода в молекуле бензола находится в состоянии sp2-гибридизации. Он связан с двумя соседними атомами углерода и атомом водорода тремя σ-связями. В результате образуется плоский шестиугольник: все шесть атомов углерода и все σ-связи С-С и С-Н лежат в одной плоскости. Электронное облако четвертого электрона (р-электрона), не участвующего в гибридизации, имеет форму гантели и ориентировано перпендикулярно к плоскости бензольного кольца. Такие р-электронные облака соседних атомов углерода перекрываются над и под плоскостью кольца.

В результате шесть р-электронов образуют общее электронное облако и единую химическую связь для всех атомов углерода. Две области большой электронной плоскости расположены по обе стороны плоскости σ-связей.

p-Электронное облако обусловливает сокращение расстояния между атомами углерода. В молекуле бензола они одинаковы и равны 0,14 нм. В случае простой и двойной связи эти расстояния составили бы соответственно 0,154 и 0,134 нм. Значит, в молекуле бензола нет простых и двойных связей. Молекула бензола – устойчивый шестичленный цикл из одинаковых СН-групп, лежащих в одной плоскости. Все связи между атомами углерода в бензоле равноценны, чем и обусловлены характерные свойства бензольного ядра. Наиболее точно это отражает структурная формула бензола в виде правильного шестиугольника с окружностью внутри (I). (Окружность символизирует равноценность связей между атомами углерода.) Однако часто пользуются и формулой Кекуле с указанием двойных связей (II):
Бензольное ядро обладает определенной совокупностью свойств, которую принято называть ароматичностью.
Гомологический ряд, изомерия, номенклатура
Условно арены можно разделить на два ряда. К первому относят производные бензола (например, толуол или дифенил), ко второму — конденсированные (полиядерные) арены (простейший из них — нафталин):
Гомологический ряд бензола имеет общую формулу СnН2n-6. Гомологи можно рассматривать как производные бензола, в котором один или несколько атомов водорода замещены различными углеводородными радикалами. Например, С6Н5-СН3 – метилбензол или толуол, С6Н4(СН3)2 – диметилбензол или ксилол, С6Н5—С2Н5 – этилбензол и т.д.

Так как в бензоле все углеродные атомы равноценны, то у первого его гомолога – толуола – изомеры отсутствуют. У второго гомолога – диметилбензола – имеются три изомера, отличающиеся взаимным расположением метильных групп (заместителей). Это орто- (сокращенно о-), или 1,2-изомер, в нем заместители находятся у соседних атомов углерода. Если заместители разделены одним атомом углерода, то это мета- (сокращенно м-) или 1,3-изомер, а если они разделены двумя атомами углерода, то это пара- (сокращенно п-) или 1,4-изомер. В названиях заместители обозначаются буквами (о-, м-, п-) или цифрами.

Физические свойства
Первые члены гомологического ряда бензола – бесцветные жидкости со специфическим запахом. Плотность их меньше 1 (легче воды). В воде нерастворимы. Бензол и его гомологи сами являются хорошими растворителями для многих органических веществ. Арены горят коптящим пламенем ввиду высокого содержания углерода в их молекулах.
Химические свойства
Ароматичность определяет химические свойства бензола и его гомологов. Шестиэлектронная π-система является более устойчивой, чем обычные двухэлектронные π-связи. Поэтому реакции присоединения менее характерны для ароматических углеводородов, чем для непредельных углеводородов. Наиболее характерными для аренов являются реакции замещения. Таким образом, ароматические углеводороды по своим химическим свойствам занимают промежуточное положение между предельными и непредельными углеводородами.
I. Реакции замещения



Алкилирование бензола происходит также при его взаимодействии с алкенами:
Дегидрированием этилбензола получают стирол (винилбензол):
II. Реакции присоединения

III. Реакции окисления
2С6Н6 + 15O2 → 12СO2 + 6Н2O
Не происходит химической реакции (сходство с алканами).
Свойства гомологов бензола
В гомологах бензола различают ядро и боковую цепь (алкильные радикалы). По химическим свойствам алкильные радикалы подобны алканам; влияние бензольного ядра на них проявляется в том, что в реакциях замещения всегда участвуют атомы водорода у атома углерода, непосредственно связанного с бензольным ядром, а также в более легкой окисляемости С-Н связей.

Влияние электронодонорного алкильного радикала (например, -СН3) на бензольное ядро проявляется в повышении эффективных отрицательных зарядов на атомах углерода в орто- и пара-положениях; в результате облегчается замещение связанных с ними атомов водорода. Поэтому гомологи бензола могут образовывать тризамещенные продукты (а бензол обычно образует монозамещенные производные).
I. Реакции с участием боковой цепи



II. Реакции с участием бензольного ядра

При избытке галогена:



Способы получения бензола
См. «Циклоалканы»
См. «Алканы»
См. «Алкины»
Способы получения гомологов бензола



Кроме одноядерных ароматических углеводородов, к которым относятся бензол и его гомологи, существуют также многоядерные арены; например:


Источник
