В молекулах какого соединения содержится ковалентная неполярная связь

Молекулы образуются из атомов, но почему атомы соединяются в молекулы? Дело в том, что их удерживают вместе химические связи.
Химическая связь – это взаимодействие атомов, посредством которого они и удерживаются в молекуле или кристалле.
«Ответственность» за образование химической связи несут неспаренные электроны, находящиеся на внешнем электронном уровне. При этом электроны атомов, которые образуют молекулу, образуют электронную пару (или несколько). Ниже мы рассмотрим, как образуется ковалентная связь и, в частности, ковалентная неполярная связь.
Что такое ковалентная связь
Выше мы узнали, что связь – это фактически пара электронов, которая образуется из электронов, находящихся на внешних слоях атомов. Эта электронная пара находится между связанными атомами. Такой вид связи называют ковалентной. Самый простой пример, объясняющий процесс образования ковалентной химической связи, – это образование молекулы водорода Н2. У каждого атома водорода имеется лишь один электрон (водород – это первый элемент периодической таблицы). Когда два атома водорода сближаются, эти электроны образуют пару, и находится она между двумя атомами. Выглядит процесс так:
Н∙ + ∙Н → Н : Н
Для удобства электронную пару обозначают чёрточкой, то есть структурно молекула водорода можно изобразить так: Н—Н. Обратите внимание на следующий факт: в данной молекуле имеются
два одинаковых атома, поэтому электронная пара расположена ровно посередине между атомами, она никуда не смещается. И эта связь носит название «ковалентная неполярная».
Ковалентная неполярная связь
Ковалентная неполярная связь образуется посредством электронной пары, которая находится посередине между атомами в молекуле и не смещена ни к одному из атомов. Вполне можно сказать, что
ковалентная неполярная связь всегда будет образовывать лишь при условии, что молекула образована двумя одинаковыми атомами
(потому что только в таком случае пара электронов будет располагаться посередине). Таким образом, в молекулах газов всегда имеется ковалентная неполярная связь (Н2, Сl2, F2, О2 и пр).
Напомню, что химическая связь может быть образована одной парой электронов (как в молекуле водорода) или несколькими. Рассмотрим для примера молекулу кислорода О2. Если обратиться к таблице Менделеева, то можно понять, что у кислорода имеется на внешнем слое шесть электронов, из которых два неспаренные. Схематично процесс образования молекулы выглядит так:
Как видно, в этом случае получается две электронные пары. Они расположены ровно посередине между атомами кислорода, то есть образуется ковалентная неполярная связь, к тому же двойная. Молекула кислорода выглядит так: О=О.
Если же мы рассмотрим образование молекулы азота (у атома азота на внешнем электронном слое пять электронов, из которых неспаренных три), то снова увидим образование ковалентной неполярной связи, но на этот раз тройной (за счёт трёх электронных пар). Схематично молекула азота можно изобразить так: N≡N.
Таким образом, ковалентная неполярная связь образуется парой электронов, которая расположена между атомами и не смещена ни к одному из них. Именно так построены двухатомные молекулы газов. А как образуются молекулы других веществ, например, воды или углекислого газа, которые состоят из разных атомов? Это мы обсудим здесь.
Пишите, пожалуйста, в комментариях, что осталось непонятным, и я обязательно дам дополнительные пояснения. Жалуйтесь на сложности в изучении школьного курса и говорите, что вас испугало в учебнике химии. И тогда следующая статья будет рассказывать именно об этой проблеме.
Источник
Сущность и виды химической связи
КОВАЛЕНТНАЯ СВЯЗЬ – это связь, возникающая между атомами за счет
образования общих электронных пар (Например,
H2, HCl, H2O, O2).
По степени смещенности общих электронных пар к одному из связанных ими
атомов ковалентная связь может быть полярной и неполярной.
А) КОВАЛЕНТНАЯ НЕПОЛЯРНАЯ СВЯЗЬ (КНС) –образуют
атомы одного и того же химического элемента – неметалла (Например, H2, O2, О3).
Механизм образования связи.
Каждый атом неметалла отдает
в общее пользование другому атому наружные не спаренные электроны. Образуются
общие электронные пары. Электронная пара принадлежит в равной мере обоим
атомам.
Рассмотрим механизм образования
молекулы хлора:
Cl2 – кнс.
Электронная схема образования молекулы Cl2:

Структурная формула молекулы Cl2:
σ
Cl– Cl, σ (p– p) – одинарная связь
Демонстрация образования молекулы водорода
Рассмотрим механизм образования
молекулы кислорода:
О2 – кнс.
Электронная схема образования молекулы О2:
Структурная формула молекулы О2:
σ
О = О
π
В молекуле кратная, двойная связь:
Одна σ (p– p)
и одна
π (р – р)
Б) КОВАЛЕНТНАЯ ПОЛЯРНАЯ СВЯЗЬ (КПС) – образуют атомы разных
неметаллов, отличающихся по значениям электроотрицательности (Например,
HCl, H2O).
Встречаются
исключения, когда ковалентную связь образуют атом неметалла и металла!
Например, AlCl3, разница в
электроотрицательности ∆ Э.О.<1.7, т.е. ∆ Э.О.= 3,16 (Cl) – 1,61(Al) = 1,55
Электроотрицательность (ЭО) – это
свойство атомов одного элемента притягивать к себе электроны от атомов других
элементов.
Самый электроотрицательный элемент – фтор F
Электроотрицательность можно
выразить количественно и выстроить элементы в ряд по ее возрастанию. Наиболее
часто используют ряд электроотрицательности элементов, предложенный
американским химиком Л. Полингом.
Таблица. Электроотрицательности (ЭО) некоторых
элементов (приведены в порядке
возрастания ЭО).
Элемент | K | Na | Ca | Al | H | Br | N | Cl | O | F |
ЭО | 0.82 | 0.93 | 1 | 1.61 | 2.2 | 2.96 | 3.04 | 3.16 | 3.44 | 4.0 |
Механизм
образования связи.
Каждый атом
неметалла отдает в общее пользование другому атому свои наружные не спаренные
электроны. Образуются общие электронные пары. Общая электронная пара смещена к
более электроотрицательному элементу.
Рассмотрим механизм образования
молекулы хлороводорода:
НCl – кпс.
Электронная схема образования молекулы НCl:

Структурная формула молекулы НCl:
σ
Н →Cl,
σ (s– p)
–
одинарная связь σ, смещение электронной плотности в сторону более
электроотрицательного атома хлора (→)
Свойства
ковалентной связи
1) Длина –
межъядерное расстояние
2) Энергия –
энергия, выделяющаяся при образовании или поглощающаяся при разрыве химической
связи.
С увеличением кратности связи
энергия увеличивается, длина связи уменьшается и химическая активность падает:
F – F | O = O | N ≡ N | C ≡ O Одна из трёх связей О→С по донорно-акцепторному механизму |
155 кДж/моль | 498 кДж/моль | 946 кДж/моль | 1065 кДж/моль |
3) Насыщаемость –
определяется способностью атомов образовывать ограниченное число связей:
Например, водород всегда
одновалентен;
азот может быть трехвалентен в
молекуле аммиака NH3 и четырёхвалентен в ионе
аммония NH4+ (валентные возможности
расширяются за счёт участия неподелённой электронной пары атома азота в
образовании ковалентной связи по донорно-акцепторному механизму).
4) Направленность* –
обуславливает форму молекулы в пространстве.
* – подробнее будет изучено в старших классах. Ковалентная связь образуется в
направлении максимального перекрывания электронных орбиталей взаимодействующих
атомов при образовании σ – связей. (см. “гибридизация”)
Закрепление
№1. Выпишите отдельно формулы веществ с ковалентной полярной и неполярной связями:
H2S, KCl, O2, Na2S, Na2O, N2, NH3, CH4, BaF2, LiCl, O3, CO2, SO3, CCl4, F2.
№2. Напишите
механизм образования молекул с ковалентным типом связи, определите тип
перекрывания электронных облаков (π или σ), а так же механизм
образования (обменный или донорно-акцепторный): H2S, KCl, O2, Na2S, Na2O, N2, NH3, CH4, BaF2, LiCl, CCl4, F2
Источник
Ковалентная связь – определение, характеристика. Что такое ковалентная связь?
Сам термин «ковалентная связь» происходит от двух латинских слов: «со» – совместно и «vales» – имеющий силу, так как это связь происходящая за счет пары электронов, принадлежащей одновременно обоим атомам (или говоря более простым языком, связь между атомами за счет пары электронов, являющихся общими для них). Образование ковалентной связи происходит исключительно среди атомов неметаллов, причем появляться она может как в атомах молекул, так и кристаллов.
Впервые ковалентная химическая связь была обнаружена в далеком 1916 году американских химиком Дж. Льюисом и некоторое время существовала в виде гипотезы, идеи, лишь затем была подтверждена экспериментально. Что же выяснили химики по ее поводу? А то, что электроотрицательность неметаллов бывает довольно большой и при химическом взаимодействии двух атомов перенос электронов от одного к другому может быть невозможным, именно в этот момент и происходит объединение электронов обоих атомов, между ними возникает самая настоящая ковалентная связь атомов.
Типы ковалентной связи
В целом есть два типа ковалентной связи:
- обменный,
- донорно-акцептный.
При обменном типе ковалентной связи между атомами каждый из соединяющихся атомов представляет на образование электронной связи по одному неспареному электрону. При этом электроны эти должны иметь противоположные заряды (спины).
Примером подобной ковалентной связи могут быть связи происходящие молекуле водорода. Когда атомы водорода сближаются, в их электронные облака проникают друг в друга, в науке это называется перекрыванием электронных облаков. Как следствие, электронная плотность между ядрами увеличивается, сами они притягиваются друг к другу, а энергия системы уменьшается. Тем не менее, при слишком близком приближении ядра начинают отталкиваться, и таким образом возникает некое оптимально расстояние между ними.
Более наглядно это показано на картинке.
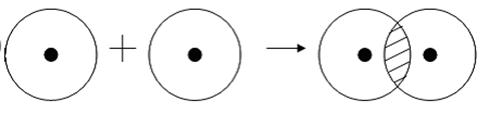
Что же касается донорно-акцепторного типа ковалентной связи, то он происходит когда одна частица, в данном случае донор, представляет для связи свою электронную пару, а вторая, акцептор – свободную орбиталь.
Также говоря о типах ковалентной связи можно выделить неполярную и полярную ковалентные связи, более подробно о них мы напишем ниже.
Ковалентная неполярная связь
Определение ковалентной неполярной связи просто, это связь, которая образуется между двумя одинаковыми атомами. Пример образование неполярной ковалентной связи смотрите ниже на схеме.
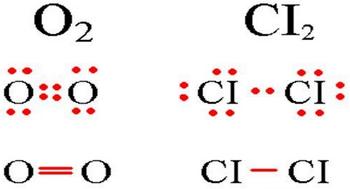
Схема ковалентной неполярной связи.
В молекулах при ковалентной неполярной связи общие электронные пары располагаются на равных расстояниях от ядер атомов. Например, в молекуле кислорода (на схеме выше), атомы приобретают восьми электронную конфигурацию, при этом они имеют четыре общие пары электронов.
Веществами с ковалентной неполярной связью обычно являются газы, жидкости или сравнительно низкоплавные тверды вещества.
Ковалентная полярная связь
Теперь же ответим на вопрос какая связь ковалентная полярная. Итак, ковалентная полярная связь образуется, когда ковалентно связанные атомы имеют разную электроотрицательность, и обобществленые электроны не принадлежат в равной степени двум атомам. Большую часть времени обобществленые электроны находятся ближе к одному атому, чем к другому. Примером ковалентной полярной связи могут служить связи, возникающие в молекуле хлороводорода, там обобществленые электроны, ответственные за образование ковалентной связи располагаются ближе к атому хлора, нежели водорода. А все дело в том, что электроотрицательность у хлора больше чем у водорода.

Так выглядит схема ковалентной полярной связи.
Ярким примером вещества с полярной ковалентной связью является вода.
Как определить ковалентную связь
Что же, теперь вы знаете ответ на вопрос как определить ковалентную полярную связь, и как неполярную, для этого достаточно знать свойства и химическую формулу молекул, если эта молекула состоит из атомов разных элементов, то связь будет полярной, если из одного элемента, то неполярной. Также важно помнить, что ковалентные связи в целом могут возникать только среди неметаллов, это обусловлено самим механизмом ковалентных связей, описанным выше.
Ковалентная связь, видео
И в завершение видео лекция о теме нашей статьи, ковалентной связи.

Автор: Павел Чайка, главный редактор журнала Познавайка
При написании статьи старался сделать ее максимально интересной, полезной и качественной. Буду благодарен за любую обратную связь и конструктивную критику в виде комментариев к статье. Также Ваше пожелание/вопрос/предложение можете написать на мою почту pavelchaika1983@gmail.com или в Фейсбук, с уважением автор.
Эта статья доступна на английском языке – Covalent Bond.
Источник
Задание №1
Из предложенного перечня выберите два соединения, в которых присутствует ионная химическая связь.
- 1. Ca(ClO2)2
- 2. HClO3
- 3. NH4Cl
- 4. HClO4
- 5. Cl2O7
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 13
Определить наличие ионного типа связи в соединении в подавляющем большинстве случаев можно по тому, что в состав его структурных единиц одновременно входят атомы типичного металла и атомы неметалла.
По этому признаку мы устанавливаем, что ионная связь имеется в соединении под номером 1 – Ca(ClO2)2, т.к. в его формуле можно увидеть атомы типичного металла кальция и атомы неметаллов – кислорода и хлора.
Однако, больше соединений, содержащих одновременно атомы металла и неметалла, в указанном списке нет.
Помимо указанного выше признака, о наличии ионной связи в соединении можно говорить, если в составе его структурной единицы содержится катион аммония (NH4+) или его органические аналоги – катионы алкиламмония RNH3+, диалкиламония R2NH2+, триалкиламмония R3NH+ или тетраалкиламмония R4N+, где R – некоторый углеводородный радикал. Например, ионный тип связи имеет место в соединении (CH3)4NCl между катионом (CH3)4+ и хлорид-ионом Cl−.
Среди указанных в задании соединений есть хлорид аммония, в нем ионная связь реализуется между катионом аммония NH4+ и хлорид-ионом Cl−.
Задание №2
Из предложенного перечня выберите два соединения, в которых тип химической связи такой же, как в молекуле фтора.
1) кислород
2) оксид азота (II)
3) бромоводород
4) иодид натрия
5) алмаз
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 15
Молекула фтора (F2) состоит из двух атомов одного химического элемента неметалла, поэтому химическая связь в данной молекуле ковалентная неполярная.
Ковалентная неполярная связь может быть реализована только между атомами одного и того же химического элемента неметалла.
Из предложенных вариантов ковалентный неполярный тип связи имеют только кислород и алмаз. Молекула кислорода является двухатомной, состоит из атомов одного химического элемента неметалла. Алмаз имеет атомное строение и в его структуре каждый атом углерода, являющегося неметаллом, связан с 4-мя другими атомами углерода.
Оксид азота (II) – вещество состоящее из молекул, образованных атомами двух разных неметаллов. Поскольку электроотрицательности разных атомов всегда различны, общая электронная пара в молекуле смещена к более электроотрицательному элементу, в данном случае к кислороду. Таким образом, связь в молекуле NO является ковалентной полярной.
Бромоводород также состоит из двухатомных молекул, состоящих из атомов водорода и брома. Общая электронная пара, образующая связь H-Br, смещена к более электроотрицательному атому брома. Химическая связь в молекуле HBr также является ковалентной полярной.
Иодид натрия – вещество ионного строения, образованное катионом металла и иодид-анионом. Связь в молекуле NaI образована за счет перехода электрона с 3s-орбитали атома натрия (атом натрия превращается в катион) на недозаполненную 5p-орбиталь атома иода (атом иода превращается в анион). Такая химическая связь называется ионной.
Задание №3
Из предложенного перечня выберите два вещества, между молекулами которых образуются водородные связи.
- 1. C2H6
- 2. C2H5OH
- 3. H2O
- 4. CH3OCH3
- 5. CH3COCH3
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 23
Пояснение:
Водородные связи имеют место в веществах молекулярного строения, в которых присутствуют ковалетные связи H-O, H-N, H-F. Т.е. ковалентные связи атома водорода с атомами трех химических элементов с наивысшей электроотрицательностью.
Таким образом, очевидно, водородные связи есть между молекулами:
1) воды
2) спиртов
3) фенолов
4) карбоновых кислот
5) аммиака
6) первичных и вторичных аминов
7) плавиковой кислоты
Задание №4
Из предложенного перечня выберите два соединения с ионной химической связью.
- 1. PCl3
- 2. CO2
- 3. NaCl
- 4. H2S
- 5. MgO
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 35
Пояснение:
Сделать вывод о наличии ионного типа связи в соединении в подавляющем большинстве случаев можно по тому, что в состав структурных единиц вещества одновременно входят атомы типичного металла и атомы неметалла.
По этому признаку мы устанавливаем, что ионная связь имеется в соединении под номером 3 (NaCl) и 5 (MgO).
Примечание*
Помимо указанного выше признака, о наличии ионной связи в соединении можно говорить, если в составе его структурной единицы содержится катион аммония (NH4+) или его органические аналоги – катионы алкиламмония RNH3+, диалкиламония R2NH2+, триалкиламмония R3NH+ или тетраалкиламмония R4N+, где R – некоторый углеводородный радикал. Например, ионный тип связи имеет место в соединении (CH3)4NCl между катионом (CH3)4+ и хлорид-ионом Cl−.
Задание №5
Из предложенного перечня выберите два вещества с одинаковым типом строения.
1) вода
2) алмаз
3) кварц
4) поваренная соль
5) золото
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 23
Задание №6
Из предложенного перечня выберите два соединения, у которых ковалентная связь образована по донорно-акцепторному механизму.
- 1. CH3NH2
- 2. CCl4
- 3. NH4Cl
- 4. CH3NH3Br
- 5. SO2Cl2
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 34
Задание №7
Из предложенного перечня выберите два соединения, которые имеют молекулярную кристаллическую решетку.
- 1. Cs2O
- 2. I2
- 3. KBr
- 4. NaI
- 5. HCl
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 25
Задание №8
Из предложенного перечня выберите два вещества немолекулярного строения.
1) фтор
2) кислород
3) белый фосфор
4) бор
5) кремний
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 45
Задание №9
Из предложенного перечня выберите два соединения с наиболее прочными химическими связями.
- 1. Cl2
- 2. Br2
- 3. O2
- 4. I2
- 5. N2
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 35
Задание №10
Из предложенного перечня выберите два соединения, в молекулах которых ковалентная связь образована одной общей электронной парой.
- 1. N2
- 2. Cl2
- 3. NO
- 4. HBr
- 5. O2
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 24
Задание №11
Из предложенного перечня выберите два вещества, в молекулах которых присутствует двойная связь между атомами углерода и кислорода.
1) этанол
2) фенол
3) формальдегид
4) уксусная кислота
5) глицерин
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 34
Задание №12
Из предложенного перечня выберите два вещества с наиболее полярными связями.
- 1. HCl
- 2. HF
- 3. H2O
- 4. H2S
- 5. HI
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 23
Задание №13
Из предложенного перечня выберите два вещества, в которых имеются и ковалентные полярные, и ионные связи.
- 1. NaCl
- 2. NaNO3
- 3. Na2SO4
- 4. Na
- 5. Na2O
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 23
Задание №14
Из предложенного перечня выберите два вещества с ионной связью.
1) кислород
2) вода
3) оксид углерода (IV)
4) хлорид натрия
5) оксид кальция
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 45
Задание №15
Из предложенного перечня выберите два вещества с таким же типом кристаллической решетки, как у алмаза.
1) кремнезем SiO2
2) оксид натрия Na2O
3) угарный газ CO
4) белый фосфор P4
5) кремний Si
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 15
Задание №16
Из предложенного перечня выберите два вещества с ионной связью.
- 1. NH4Cl
- 2. HCOONa
- 3. NH3
- 4. HCOOH
- 5. CO
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 12
Задание №17
Из предложенного перечня выберите два вещества с наибольшей длиной химической связи в молекуле.
- 1. HF
- 2. HCl
- 3. HBr
- 4. HI
- 5. H2O
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 34
Задание №18
Из предложенного перечня выберите два вещества, в молекулах которых есть одна π-связь.
- 1. SO2
- 2. HBr
- 3. HCOOH
- 4. H2
- 5. O2
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 35
Задание №19
Из предложенного перечня выберите два вещества с атомной кристаллической решеткой.
- 1. Cl2
- 2. B
- 3. Cu
- 4. Si
- 5. P4
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 24
Задание №20
Из предложенного перечня выберите два вещества, в молекулах которых есть одна тройная связь.
- 1. HCOOH
- 2. HCOH
- 3. C2H4
- 4. N2
- 5. C2H2
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 45
Пояснение:
Для того, чтобы найти правильный ответ, нарисуем структурные формулы соединений из представленного списка:
Таким образом, мы видим, что тройная связь имеется в молекулах азота и ацетилена. Т.е. правильные ответы 45
Задание №21
Из предложенного перечня выберите два вещества, в молекулах которых есть ковалентная неполярная связь.
1) Гидроксид натрия
2) Вода
3) Метанол
4) Этан
5) Пероксид водорода
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 45
Задание №22
Из предложенного перечня веществ выберите два вещества, которые имеют молекулярную кристаллическую решётку.
- 1. CO2
- 2. SiO2
- 3. NH3
- 4. NaH
- 5. PbO2
Запишите в поле ответа номера выбранных веществ.
Решение
Ответ: 13
Задание №23
Из предложенного перечня веществ выберите два вещества, для каждого из которых характерно наличие водородной связи между молекулами.
1) формальдегид
2) глицерин
3) бензол
4) уксусная кислота
5) толуол
Запишите в поле ответа номера выбранных веществ.
Решение
Ответ: 24
Задание №24
Из предложенного перечня веществ выберите два вещества, которые имеют атомную кристаллическую решётку.
1) белый фосфор
2) сера
3) графит
4) кремний
5) натрий
Запишите в поле ответа номера выбранных веществ.
Решение
Ответ: 34
Задание №25
Из предложенного перечня веществ выберите два соединения, в которых одна из ковалентных связей образована по донорно-акцепторному механизму.
- 1. LiOH
- 2. Li3PO4
- 3. (NH4)2HPO4
- 4. NH4F
- 5. H3PO4
Запишите в поле ответа номера выбранных веществ.
Решение
Ответ: 34
Задание №26
Из предложенного перечня веществ выберите два соединения, в которых присутствует ковалентная полярная химическая связь.
1) оксид кремния
2) оксид лития
3) хлорид лития
4) силикат лития
5) кремний
Запишите в поле ответа номера выбранных веществ.
Решение
Ответ: 14
Задание №27
Из предложенного перечня веществ выберите два вещества, в которых присутствует ионная химическая связь.
- 1. H2SO4
- 2. KNO3
- 3. PCl3
- 4. KCl
- 5. H3BO3
Запишите в поле ответа номера выбранных веществ.
Решение
Ответ: 24
Задание №28
Из предложенного перечня веществ выберите два соединения, в которых присутствует ионная связь.
1) хлороводород
2) хлорид натрия
3) оксид серы(IV)
4) аммиак
5) оксид натрия
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 25
Задание №29
Из предложенного перечня веществ выберите два соединения, в которых присутствует ковалентная неполярная связь.
1) аммиак
2) иод
3) кислород
4) вода
5) метан
Запишите в поле ответа номера выбранных соединений.
Решение
Ответ: 23
Источник
